la terapia inhalada es esencial en la fibrosis quística; sin embargo, los inhaladores presentan un impacto medioambiental significativo derivado de los gases de efecto invernadero (GEI) emitidos. El impacto medioambiental de un producto se estima mediante su huella de carbono (HC). Los inhaladores de cartucho presurizado (pMDI) presentan mayor HC que los inhaladores de polvo seco (DPI) y de nube de vapor suave (SMI) al incorporar GEI.
Los objetivos del estudio son analizar el consumo de inhaladores (broncodilatadores agonistas β2-adrenérgicos, anticolinérgicos y/o corticoides) en una unidad de fibrosis quística y estimar la HC generada.
Métodose determinó retrospectivamente (enero de 2018-diciembre de 2023) el consumo y la HC (tCO2eq) por tipo de inhalador. Se evaluó la tendencia de consumo y la HC mediante regresión lineal.
Resultadosse dispensaron anualmente 1.529 (1.279–1.613) pMDI, 1.055 (855–1.333) DPI y 28 (20–42) SMI, representando el 55,97; 42,33 y 1,70%, respectivamente. Se observó una tendencia positiva estadísticamente significativa del consumo de SMI. La HC mediana anual fue: pMDI 38,3 (31,2–40,3) tCO2eq, DPI 0,8 (0,6–0,9) tCO2eq y SMI 0,02 (0,02-0,03) tCO2eq, representando, respectivamente el 97,86; 2,04 y 0,10%.
Conclusioneslos pMDI fueron los inhaladores con mayor consumo y HC, aunque parece que su consumo tiende a disminuir, incrementándose el de SMI.
Inhaled therapy is essential in cystic fibrosis; however, inhalers have a significant environmental impact due to the greenhouse gases (GHGs) emitted. The environmental impact of a product is estimated by its carbon footprint (CF). Pressurized metered-dose inhalers (pMDIs) have a higher CF than dry powder inhalers (DPIs) and soft mist inhalers (SMIs) due to the incorporation of GHGs.
The objectives are to analyze the consumption of inhalers (β2-adrenergic agonist bronchodilators, anticholinergics, and/or corticosteroids) in a cystic fibrosis unit and estimate the generated CF.
MethodRetrospective determination (January 2018–December 2023) of consumption and CF (tCO2eq) by type of inhaler was conducted. Consumption and CF trends were evaluated using lineal regression.
ResultsAnnually, 1,529 (1,279–1,613) pMDIs, 1,055 (855–1,333) DPIs, and 28 (20–42) SMIs were dispensed, representing 55.97%, 42.33%, and 1.70%, respectively. A statistically significant positive trend in the consumption of SMIs was observed. The median annual CF was: pMDI 38.3 (31.2–40.3) tCO2eq, DPIs 0.8 (0.6–0.9) tCO2eq, and SMIs 0.02 (0.02-0.03) tCO2eq, representing 97.86, 2.04, and 0.10%, respectively.
ConclusionspMDIs were the inhalers with the highest consumption and CF, although their consumption appears to be decreasing, with an increase in the consumption of SMIs.
La fibrosis quística (FQ) representa la enfermedad rara autosómica recesiva más prevalente en la población caucásica. Debido a que las complicaciones respiratorias son la principal causa de mortalidad, la terapia inhalada cumple un papel esencial1,2. No obstante, su efectividad depende de factores como la técnica de inhalación y la adherencia terapéutica. En FQ existe una significativa falta de adherencia derivada de la elevada complejidad del plan farmacoterapéutico y su impacto en la vida diaria. Por tanto, resulta esencial considerar las preferencias del paciente al instaurar la terapia1,2. Otro inconveniente es el impacto medioambiental de los dispositivos de administración.
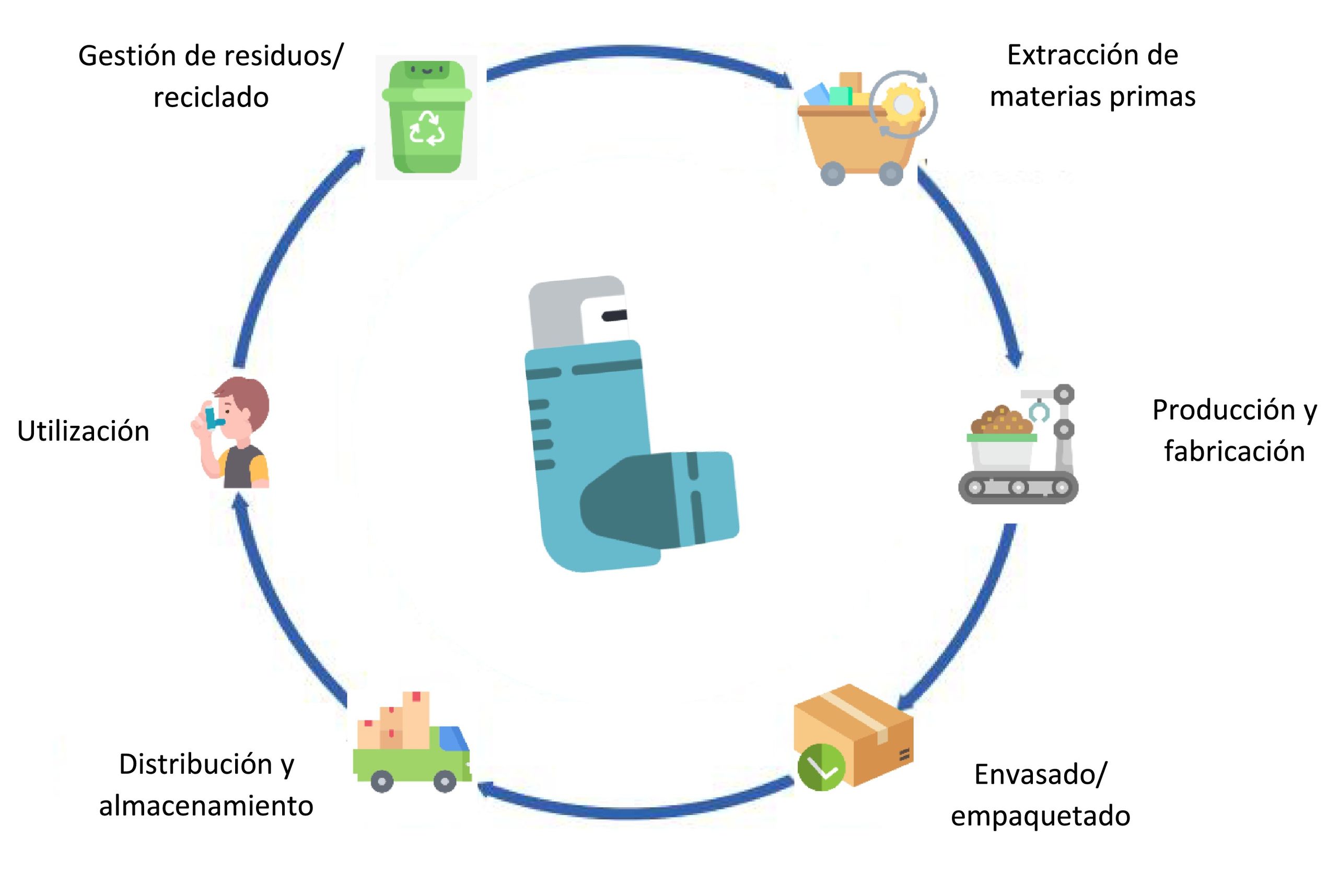
El término «cambio climático» incluye el calentamiento global causado por los gases de efecto invernadero (GEI). El impacto medioambiental de un producto se determina mediante su huella de carbono (HC), definida como los GEI emitidos durante su ciclo de vida (fig. 1). Su valor se expresa empleando como referencia el CO2, siendo la tonelada de CO2 equivalente (tCO2eq) la unidad de medida más empleada, e indica su potencial de calentamiento global (PCG)3,4.
Se distinguen 3 tipos de inhaladores: cartucho presurizado (pMDI), polvo seco (DPI) y nube de vapor suave (SMI)4. Los pMDI incorporan gases propelentes hidrofluorocarbonados (HFC) para la liberación del fármaco, GEI con alto PCG que les confieren una elevada HC4,5. Aunque los pMDI suponen menos del 0,1% de los GEI emitidos mundialmente, cada vez son más las iniciativas para reducir su uso4,5. En 2019 en Europa, los pMDI fueron responsables de más del 90% de emisiones, siendo los broncodilatadores agonistas β2-adrenérgicos de acción corta (SABA) los más empleados4. La Agencia Española de Medicamentos y Productos Sanitarios (AEMPS) reportó una prevalencia de uso de pMDI del 52%4,6.
Los objetivos del estudio son analizar el consumo de inhaladores en la unidad de pacientes FQ (UFQ) del Servicio de Farmacia Hospitalaria (SFH) de un centro de referencia nacional y evaluar su impacto medioambiental mediante el cálculo de la HC.
MétodosEstudio retrospectivo realizado entre enero de 2018 y diciembre de 2023 en la UFQ del SFH de un hospital terciario de referencia nacional en FQ. Se incluyeron todos los pacientes en tratamiento inhalado con broncodilatadores agonistas β2-adrenérgicos, anticolinérgicos y/o corticoides. El estudio fue aprobado por el Comité de Ética de Investigación Clínica con medicamentos referente.
Consumo de inhaladoresSe determinó el consumo de cada inhalador a partir las dispensaciones registradas en el programa de prescripción electrónica (Silicon® GRIFOLS S.A.). Se clasificaron para su análisis por grupo, identificándose las especialidades más dispensadas de cada uno.
Estimación de la huella de carbonoSe calculó la HC generada por especialidad y tipo de dispositivo, a partir de los consumos y valores de referencia de HC publicados por el National Health Service (NHS) de Reino Unido (material suplementario)7.
Se realizó estadística descriptiva de los resultados; expresándose como valor absoluto, porcentaje, media ± desviación estándar o mediana (rango intercuartílico) según categoría y distribución de los valores. Para evaluar la tendencia de consumo y HC se realizó análisis de regresión lineal, empleando StataCorp.2019 (Stata Statistical Software: Release 16. College Station, TX:StataCorp LLC).
ResultadosSe incluyeron 395 pacientes (253 ± 21 pacientes/año) en tratamiento con broncodilatadores agonistas β2-adrenérgicos, anticolinérgicos y/o corticoides inhalados (31 especialidades farmacéuticas), un 66,5 ± 4,4% de los pacientes de la UFQ.
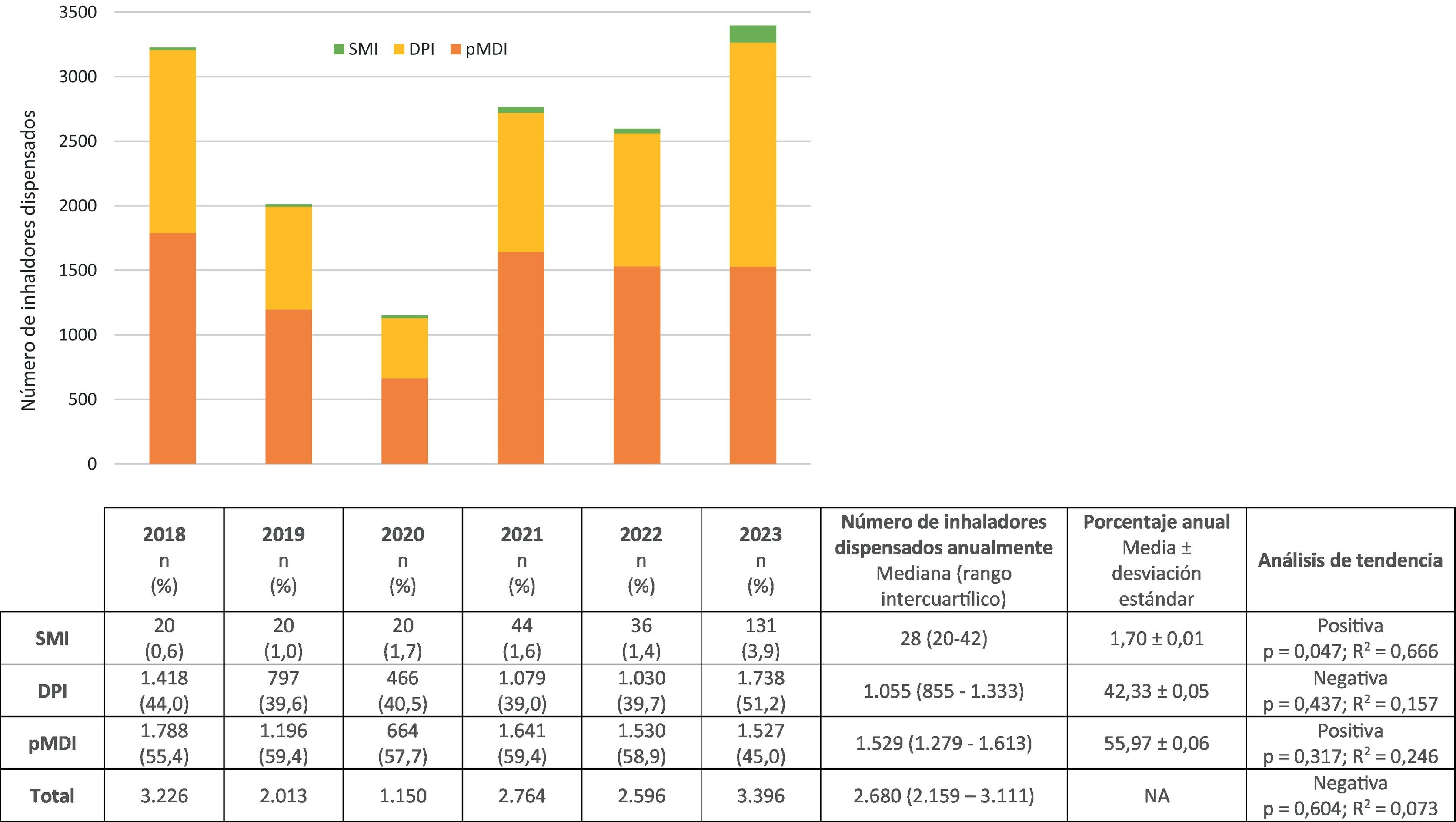
Consumo de inhaladoresEn la figura 2 se recoge el consumo anual y total por tipo de inhalador y global, así como los resultados estadísticos. Entre los pMDI, destacaron salbutamol Aldo-Unión EFG®, 100 μg/inh (41,29 ± 0,05%) y Atroaldo® (ipratropio) 20 μg/inh (7,91 ± 0,02%); y entre los DPI, Relvar Ellipta® (fluticasona/vilanterol) 92/22 μg/inh (17,32 ± 0,02%), Symbicort Turbuhaler® (budesonida/formoterol) 160/4,5 μg/inh (8,80 ± 0,08%) y Spiriva® (tiotropio) 18 μg/inh (6,15 ± 0,03%).
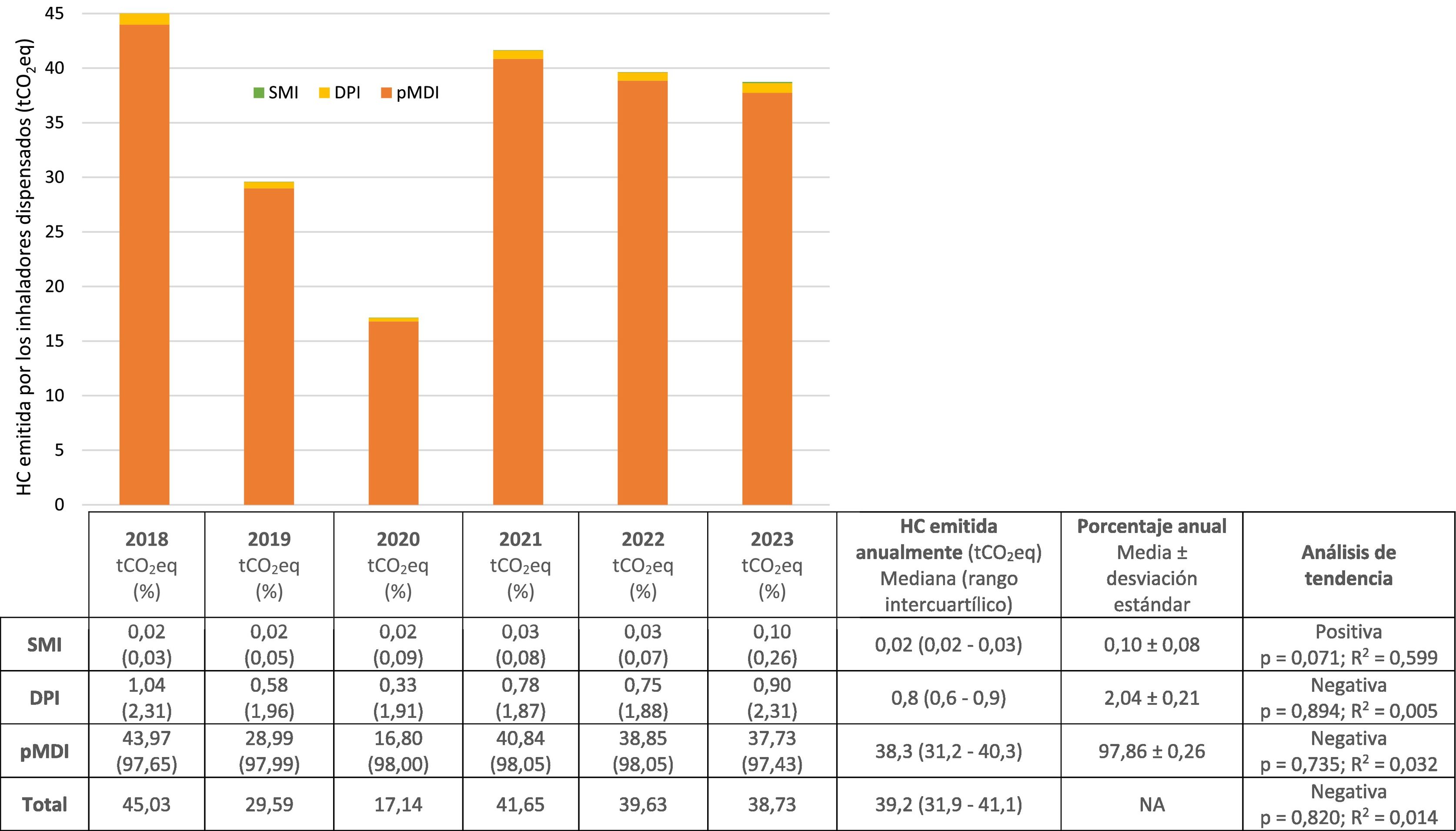
Estimación de la huella de carbonoEn la figura 3 se recoge la HC anual y total por tipo de inhalador y global, así como los resultados estadísticos. Los pMDI con HC superiores fueron salbutamol Aldo-Unión EFG® 100 μg/inh (32,1 [25,9–33,3] tCO2eq, 83,82 ± 0,02%) y Atroaldo® (ipratropio) 20 μg/inh (3,2 [2,1–3,7]) tCO2eq, 8,35 ± 0,02%). Entre los DPI destacaron Relvar Ellipta® (fluticasona/vilanterol) 92/22 μg/inh (0,37 [0,29–0,39] tCO2eq, 45,46 ± 0,05%), Symbicort Turbuhaler® (budesonida/formoterol) 160/4,5 μg/inh (0,13 [0,08–0,14] tCO2eq, 16,76 ± 0,08%) y Spiriva® (tiotropio) 18 μg/inh (0,04 [0,03–0,05] tCO2eq; 8,92 ± 0,09%).
Huella de carbono emitida por los dispositivos de inhalación dispensados entre 2018 y 2023 en la unidad de pacientes de fibrosis quística.
DPI: inhalador de polvo seco; HC: huella de carbono; NA: no aplica; pMDI: inhalador de cartucho presurizado; SMI: inhalador de nube de vapor suave; tCO2eq: tonelada de CO2 equivalente.
El 5% de la HC de un país es causada por los sistemas sanitarios; siendo los gases anestésicos y los pMDI responsables del 5% de dichas emisiones. Existe un interés creciente sobre el impacto medioambiental de los inhaladores y, aunque los pMDI son responsables de un bajo porcentaje de las emisiones, las iniciativas para reducir su HC están en constante desarrollo4,5.
Las terapias inhaladas cumplen un papel imprescindible en FQ, un hecho reflejado en el presente estudio con el elevado porcentaje de pacientes con tratamiento inhalado1,2. Por ende, los autores consideramos que se trata de una población con gran posibilidad de actuación, junto con la cronicidad de los tratamientos.
Los resultados obtenidos coinciden con los datos de la AEMPS, pues los pMDI representaron más del 50% de los dispositivos empleados6. Sin embargo, se observó un menor consumo de pMDI en 2023 y una tendencia creciente estadísticamente significativa del consumo de SMI. El bajo consumo global en 2020, viene explicado por la pandemia SARS-CoV-2; el confinamiento y las medidas de protección condujeron al consumo de medicación acumulada en domicilio, una reducción de las infecciones respiratorias y, consecuentemente, una menor necesidad de tratamientos.
La HC generada por pMDI, DPI y SMI en España en 2020 supuso el 0,0909; 0,0056 y 0,0005% de las emisiones totales, respectivamente8. Los resultados de nuestro estudio condujeron a las mismas conclusiones, pues los pMDI generaron mayor HC. Igualmente, coinciden con los resultados de Pernigotti et al.4, pues los pMDI son responsables de aproximadamente el 98% de la HC de la UFQ, destacando los SABA. Puesto que la sustitución de un pMDI por un DPI o SMI reduciría la HC un 97%, diferentes organizaciones y sociedades científicas recomiendan priorizar los DPI y SMI. Sin embargo, advierten de que un cambio inadecuado de dispositivo podría conllevar un impacto clínico negativo y una baja adherencia. Por tanto, la eficacia, la seguridad y las preferencias del paciente deben ser los factores prioritarios al seleccionar el inhalador6,8–10. En el presente estudio se observó que la HC generada por pMDI y DPI, así como la HC total de la unidad tendieron a disminuir, mientras que la HC de los SMI tendió a incrementarse. Aunque ninguno de los resultados fue estadísticamente significativo, en el caso de SMI podría adquirir potencia estadística si se mantiene la tendencia observada.
La falta de adherencia a los tratamientos inhalados en FQ constituye una de las principales limitaciones en su efectividad. La complejidad terapéutica, la cronicidad de la enfermedad y las terapias y el tiempo requerido para su administración, conllevan un significativo impacto en la vida de los pacientes. Para conseguir un adecuado control clínico y una correcta adherencia, es fundamental que el dispositivo se ajuste al estilo de vida del paciente4.
Asimismo, un cumplimiento inadecuado conlleva el uso de tratamientos de rescate. Aunque las guías destacan los riesgos asociados al uso excesivo de SABA en las exacerbaciones, en la práctica clínica existe un sobreuso, principalmente, de salbutamol en pMDI. Se estimó que un pMDI del salbutamol emite una HC equivalente a la emitida por un coche al recorrer 300 km (28 kgCO2eq)11. El uso de salbutamol de rescate en España, Italia, Francia, Alemania y Reino Unido produce 1.791.312 tCO2eq anuales5. Una administración adecuada, la optimización terapéutica y el uso de SABA correcto, reduciría las emisiones significativamente4.
Otro punto estratégico es la gestión de residuos; el estudio AIRE concluye que menos del 50% de los pacientes recicla los dispositivos en el punto del sistema integrado de gestión y recogida de envases (SIGRE)12; reflejando la necesidad de concienciar a los pacientes sobre la importancia de la correcta gestión de los residuos, así como de reducir su producción6.
Pernigotti et al.4 realizaron un estudio predictivo de los resultados esperados al aplicar diferentes medidas sostenibles durante 10 años. La sustitución de pMDI por DPI/SMI reduciría las emisiones un 68%; el uso de HFC con menor PCG un 78–89% y la optimización terapéutica un 17–48%.
Tras la evaluación de los resultados y teniendo en cuenta el uso indispensable de terapia inhalada en FQ, el SFH planteó posibles medidas estratégicas a desarrollar en la UFQ, las cuales serán presentadas a los referentes en FQ del hospital con el fin de establecer un plan de trabajo (tabla 1). Las modificaciones del tratamiento se realizarán consensuadamente entre equipo médico, farmacéutico y paciente, garantizando eficacia, seguridad y adherencia. Puesto que, según la Circular 8/91 del Insalud de 23 de abril de 1991, los SFH son responsables de la dispensación de los tratamientos a pacientes FQ, será posible un seguimiento estrecho y valoración de los resultados tras su implantación.
Posibles medidas estratégicas propuestas para reducir el impacto ambiental de las terapias inhaladas en la unidad
| Medidas estratégicas para reducir el impacto ambiental de las terapias inhaladas en la UFQ |
|
DPI: inhaladores de polvo seco; PCG potencial de calentamiento global; pMDI: inhaladores de cartucho presurizado; SABA: agonistas β2-adrenérgicos de acción corta; SMI: inhaladores de nube de vapor suave; UFQ: unidad de pacientes de fibrosis quística.
La principal limitación del estudio es su carácter retrospectivo, que puede conducir a errores en la recogida de datos. Asimismo, los datos de consumo se basan en los dispositivos dispensados desde la UFQ, pudiendo no coincidir con los dispositivos administrados.
Se concluye que los pMDI fueron los dispositivos de inhalación más empleados y que generaron mayor HC, destacando los SABA, aunque parece su consumo tiende a disminuir, incrementándose el de SMI. Además, pone de manifiesto la necesidad de desarrollar estrategias sostenibles para reducir el impacto medioambiental de los inhaladores.
Aportación a la literatura científicaActualmente, los inhaladores presentan un impacto medioambiental significativo resultante de la emisión de gases de efecto invernadero, que contribuye al calentamiento global. Sin embargo, los tratamientos administrados mediante vía inhalatoria cumplen un papel fundamental e imprescindible en la población con fibrosis quística. Por ello, constituyen una población diana con gran capacidad de actuación para la implantación de medidas estratégicas encaminadas a reducir el impacto medioambiental originado por los dispositivos de administración. Se trata del primer estudio publicado que evalúa el impacto medioambiental de las terapias inhaladas empleadas por pacientes con fibrosis quística en España. El estudio establece un punto de partida para el desarrollo de estrategias sostenibles en la unidad.
FinanciaciónLos autores declaran no haber recibido financiación para la realización de este trabajo.
Conflicto de interesesLos autores declaran que no tienen ningún conflicto de intereses.
Responsabilidad y cesión de derechosTodos los autores aceptamos la responsabilidad definida por el Comité Internacional de Editores de Revistas Médicas (disponible en: http://www.icmje.org/). Los autores cedemos, en el supuesto de publicación, de forma exclusiva los derechos de reproducción, distribución, traducción y comunicación pública (por cualquier medio o soporte sonoro, audiovisual o electrónico) de nuestro trabajo a Farmacia Hospitalaria y por extensión a la SEFH.
Declaración de contribución de autoría CRediTLaura Gómez-Ganda: Writing – review & editing, Writing – original draft, Visualization, Validation, Supervision, Methodology, Formal analysis, Data curation, Conceptualization. Beatriz García-Palop: Writing – review & editing, Writing – original draft, Supervision, Data curation, Conceptualization. Arnau Mariscal-Puig: Validation, Methodology, Investigation, Formal analysis, Data curation. Alejandro Ábalos-Camacho: Validation, Methodology, Data curation, Conceptualization. Aurora Fernández-Polo: Visualization, Validation, Supervision, Methodology, Investigation, Formal analysis, Data curation, Conceptualization.