describir la experiencia de uso de la terapia de infusión de antibióticos domiciliaria mediante bombas de infusión elastoméricas, administrada a pacientes ingresados en la unidad de hospitalización a domicilio de un hospital de tercer nivel durante 3 años y analizar la evolución clínica y la mortalidad.
Métodosestudio observacional retrospectivo mediante la revisión de las historias clínicas de los pacientes incluidos. Se obtuvo información sobre antecedentes personales, terapia antimicrobiana recibida y evolución clínica. Análisis estadístico realizado mediante el software SPSS® 19.
Resultadosse incluyeron 81 pacientes, 61,7% hombres, con una media de edad de 73,5 ± 17,5 años. Las comorbilidades más frecuentes fueron diabetes mellitus (30,9%) y enfermedad renal crónica (28,4%). Los pacientes recibieron de media 11,9 ± 8,5 días de antibiótico en bombas de infusión elastoméricas. El principal foco infeccioso fue el respiratorio (27,2%), seguido de bacteriemia (16%) e infecciones de la piel y las partes blandas (12,3%). El 65,4% de las infecciones fueron monomicrobianas, siendo la Pseudomonas aeruginosa el principal microorganismo implicado (39,6%). El antimicrobiano más utilizado fue piperacilina/tazobactam (33,3%). El 85,2% de los pacientes presentó buena evolución clínica, pero la tasa de mortalidad en los 30 días posteriores a la finalización del tratamiento fue de 24,7%. En el análisis univariante, se asociaron a una peor evolución clínica los antecedentes de neoplasia en los últimos 5 años (p = 0,01) y haber recibido menos días de antiobioterapia previo al inicio del tratamiento antibiótico domiciliario en infusor (p = 0,04). La edad mayor de 80 años se asoció a mejor evolución (p = 0,03). Se asoció a mayor mortalidad el diagnóstico de insuficiencia cardiaca (p = 0,026) y a menor mortalidad los pacientes procedentes de servicios quirúrgicos (p = 0,047). En el análisis multivariante, la presencia de neoplasia se asoció a una evolución desfavorable (p = 0,012) y la insuficiencia cardiaca, a una mayor mortalidad (p = 0,027).
Conclusionesla terapia antibiótica domiciliaria en bombas de infusión elastoméricas es una alternativa en pacientes que necesitan tratamiento intravenoso prolongado, sin ser condicionante para la inclusión en estos programas la edad. No obstante, la presencia de ciertas comorbilidades puede afectar negativamente a la evolución clínica y mortalidad de los pacientes.
To describe the experience of home antibiotic infusion therapy using elastomeric infusion pumps, administered to patients admitted to the Home Hospitalization Unit of a tertiary hospital for three years and to analyse clinical evolution and mortality.
MethodRetrospective observational study. The medical history of the patients included in the study was reviewed. Information was obtained on personal history, antimicrobial therapy received and clinical evolution. Statistical analysis was performed using SPSS® 19 software.
ResultsEighty-one patients were included, 61.7% men, with a mean age of 73.5 ± 17.5 years. The most frequent comorbidities were diabetes mellitus (30.9%) and chronic kidney disease (28.4%). Patients received a mean of 11.9 ± 8.5 days of antibiotic treatment in an elastomeric infusion pump. The main focus of infection was respiratory (27.2%), followed by bacteremia (16%) and skin and soft tissue infections (12.3%). Of the infections, 65.4% were monomicrobial, with Pseudomonas aeruginosa being the main microorganism involved (39.6%). The most commonly used antimicrobial was piperacillin/tazobactam (33.3%). The clinical course was good in 85.2% of the patients, but the mortality rate in the 30 days following the end of treatment was 24.7%. In the univariate analysis, a history of neoplasia in the last 5 years (p = 0.01) and having received fewer days of antibiotic therapy prior to the start of outpatient antimicrobial therapy in infusion pump (p = 0.04) were associated with worse clinical outcome.
Age over 80 years was associated with better outcome (p = 0.03). The diagnosis of heart failure was associated with higher mortality (p = 0.026) and patients from surgical services, with lower mortality (p = 0.047). In the multivariate analysis, the presence of neoplasia was associated with unfavorable evolution (p = 0.012) and heart failure with higher mortality (p = 0.027).
ConclusionsOutpatient antimicrobial therapy in elastomeric infusion pumps is an alternative in patients requiring prolonged intravenous treatment, and age is not a conditioning factor for inclusion in these programs. However, the presence of certain comorbidities can negatively affect the clinical course and mortality of patients.
Desde hace décadas, existe un gran interés por diseñar programas que permitan el tratamiento en el domicilio del paciente de enfermedades que, tradicionalmente, requerían ingreso hospitalario convencional en plantas de hospitalización. Un ejemplo de esto es el desarrollo de los programas de tratamiento antibiótico domiciliario intravenoso (TADE).
El TADE o su acrónimo inglés, OPAT (outpatient parenteral antimicrobial therapy), consiste en la administración de antiobioterapia por vía parenteral en el domicilio del paciente, con una duración de al menos 2 dosis en días diferentes1. Desde su aparición en la década de los 702, este tipo de terapia ha ganado un gran peso en el tratamiento de pacientes que requieren terapia antibiótica prolongada3.
Un elemento clave en el éxito de este programa radica en la acertada elección de la modalidad de administración. Los antimicrobianos más utilizados son los de administración en dosis única diaria. En el caso de fármacos que requieren más de una dosis al día, se hace muy interesante la administración en bombas de infusión elastoméricas4. Estos sistemas son dispositivos estériles, transparentes, en cuyo interior se encuentra un globo o depósito que permite la liberación a velocidad constante del fármaco cargado. Además, son dispositivos ligeros que no requieren una fuente de alimentación externa, permitiendo así una total movilidad del paciente5. El flujo de las bombas de infusión elastoméricas puede verse afectado por diversos factores como la variación de la temperatura, viscosidad, posición del dispositivo respecto al acceso vascular del paciente, concentración del antibiótico en la disolución, entre otros6–8.
El diseño de estos dispositivos ha supuesto un gran avance en el TADE. Los principales usos de estos sistemas portátiles de infusión continua son la administración domiciliaria de quimioterapia, tratamiento sintomático en pacientes paliativos, analgesia controlada por el paciente y antiobioterapia9. En el caso de la administración de antibióticos, la infusión continua ha demostrado ser una estrategia efectiva para optimizar la farmacocinética y farmacodinamia de fármacos tiempo-dependientes, como en el caso de los betalactámicos. El fundamento de la efectividad de esta familia de antibióticos está directamente relacionado con el tiempo en el que la concentración del fármaco supera la concentración mínima inhibitoria (CMI) del patógeno10,11. Por tanto, la prolongación del tiempo de infusión proporciona niveles séricos más constantes manteniendo las concentraciones plasmáticas del fármaco por encima de la CMI durante un período prolongado, mejorando la efectividad y la probabilidad de éxito en el tratamiento12.
En nuestro país, esta forma de terapia se ha desarrollado de forma heterogénea en función de las necesidades y recursos de cada zona. En nuestra comunidad autónoma, se lleva a cabo habitualmente por las unidades de hospitalización a domicilio (HADO), de hecho, la Sociedad Española de Hospitalización a Domicilio ha desarrollado guías clínicas para la administración del TADE4.
El uso del TADE tiene diversas ventajas, como evitar estancias prolongadas en el hospital, reduciendo el riesgo de infecciones nosocomiales13, además de ser una opción de tratamiento coste-eficaz14. No obstante, también tiene sus limitaciones, como la necesidad de que el paciente deba encontrarse en una situación clínica estable, tener un adecuado soporte familiar, disponibilidad de comunicación telefónica y, en el caso de nuestro centro, residir dentro del área de influencia del servicio de HADO15.
De este gran desarrollo del TADE surge el presente estudio, con el objetivo de describir la experiencia del uso de la terapia de infusión domiciliaria de antibióticos mediante bombas de infusión elastoméricas, administrada a pacientes ingresados en la unidad de HADO de un hospital de tercer nivel durante 3 años, además de buscar posibles variables que nos ayuden a predecir la evolución clínica y la mortalidad de los pacientes.
MétodoEstudio observacional retrospectivo mediante la revisión de las historias clínicas de los pacientes con TADE en bombas de infusión elastoméricas en el Complejo Hospitalario Universitario de Lugo, de enero de 2019 a diciembre de 2022.
Se incluyeron todos los pacientes pediátricos y adultos que tras ingreso hospitalario en las unidades convencionales de hospitalización fueron trasladados a la unidad de HADO para continuar terapia antibiótica en bombas de infusión elastoméricas. No fue definido ningún criterio de exclusión.
Se registraron datos sociodemográficos (edad y sexo) y datos clínicos (servicio de procedencia, comorbilidades, localización, tipo y evolución clínica de la infección, microorganismo aislado, tipo y duración de la antiobioterapia, acceso vascular utilizado y complicaciones relacionadas con el tratamiento).
Las comorbilidades recogidas fueron antecedentes de infarto agudo de miocardio, insuficiencia cardíaca (IC), enfermedad cerebrovascular, arteriopatía periférica, deterioro cognitivo, enfermedad pulmonar obstructiva crónica (EPOC), diabetes mellitus (DM), enfermedad renal crónica (ERC), definida como la presencia de un filtrado glomerular <60 ml/min/m2, hepatopatía, infección por el virus de la inmunodeficiencia humana (VIH) y la historia actual o en los últimos 5 años de neoplasia. Se calculó el índice de Charlson, ajustado por edad, para tener una medida del grado de comorbilidad, así como para analizar su impacto en la evolución clínica y mortalidad.
Una vez finalizado el TADE para cada paciente y mediante la consulta de la historia clínica, se recogió la situación clínica al ingreso, la evolución y la resolución de la infección o no al alta de la unidad de HADO. Estos datos se volvieron a recoger 30 días después para valorar la mortalidad. En las visitas de seguimiento programadas por parte del equipo de HADO se realizaron los exámenes físicos y analíticos (presión arterial, temperatura, leucocitosis, neutrofilia, proteína C reactiva, procalcitonina, etc.) necesarios para poder evaluar la evolución de la infección. Se consideró buena evolución clínica la ausencia o desaparición de la fiebre, signos o síntomas de infección, sin reingreso hospitalario no planificado y sin fallecimiento en el mes siguiente al cese del TADE. Se consideró mortalidad el fallecimiento del paciente en los 30 días posteriores a finalizar el tratamiento, estuviese o no relacionada con la infección tratada.
Se utilizaron diferentes bombas de infusión elastoméricas (Dosi-Fuser® Leventon 150 ml/24 horas, Dosi-Fuser® Leventon 250 ml/12 horas, Accufuser® Woo Young Medical 300 ml/24 horas y Accufuser® Woo Young Medical 300 ml velocidad variable) en función del antibiótico a administrar y del volumen necesario para la dilución del mismo, y se prepararon en cabinas de flujo laminar en el servicio de farmacia del hospital. El TADE en bombas de infusión elastoméricas se inició una hora después de una dosis de carga o una hora después de la última dosis intermitente administrada en el hospital. En el caso de infusores de 24 horas fue el equipo de HADO el encargado del cambio del infusor diario. Sin embargo, en infusores de 12 horas, en algún caso, era el familiar del paciente el encargado de hacer el cambio de infusor (autoadministración).
Se creó una base de datos en Microsoft Excel© con los datos obtenidos para su posterior análisis estadístico mediante el software SPSS® 19. Las variables cuantitativas se expresaron como media ± desviación típica (DT) y las variables cualitativas como valor absoluto y porcentaje. En el análisis univariante, se realizó la comparación de 2 medias por medio del test de la T de Student y/o test de Mann-Whitney. Se consideró como significativo un valor de p ≤ 0,05. Para las variables cualitativas se calcularon los odds ratio (OR) con su IC 95%. Posteriormente, se realizó un análisis multivariante mediante regresiones logísticas, para estudiar el grado de asociación de la evolución clínica y mortalidad con las variables significativas resultantes en el análisis univariante y con aquellas relevantes desde un punto de vista clínico que pudiesen influir en el resultado final, y se calcularon los hazard ratio (HR) con su IC 95%.
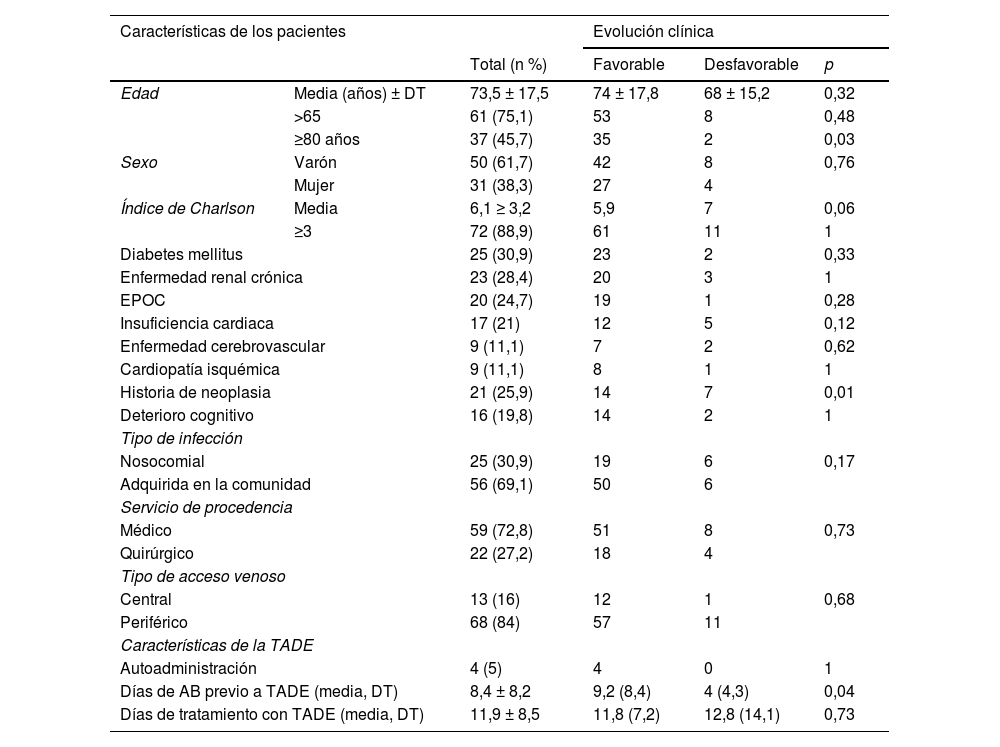
ResultadosSe incluyeron 81 pacientes con tratamiento antibiótico en bombas de infusión elastoméricas. La media de edad fue de 73,5 ± 17,5 años (rango de edad: 6-102 años). El 61,7% de los pacientes eran varones. Las principales características de los pacientes incluidos se muestran en la tabla 1.
Características de los pacientes y su relación con la evolución clínica
| Características de los pacientes | Evolución clínica | ||||
|---|---|---|---|---|---|
| Total (n %) | Favorable | Desfavorable | p | ||
| Edad | Media (años) ± DT | 73,5 ± 17,5 | 74 ± 17,8 | 68 ± 15,2 | 0,32 |
| >65 | 61 (75,1) | 53 | 8 | 0,48 | |
| ≥80 años | 37 (45,7) | 35 | 2 | 0,03 | |
| Sexo | Varón | 50 (61,7) | 42 | 8 | 0,76 |
| Mujer | 31 (38,3) | 27 | 4 | ||
| Índice de Charlson | Media | 6,1 ≥ 3,2 | 5,9 | 7 | 0,06 |
| ≥3 | 72 (88,9) | 61 | 11 | 1 | |
| Diabetes mellitus | 25 (30,9) | 23 | 2 | 0,33 | |
| Enfermedad renal crónica | 23 (28,4) | 20 | 3 | 1 | |
| EPOC | 20 (24,7) | 19 | 1 | 0,28 | |
| Insuficiencia cardiaca | 17 (21) | 12 | 5 | 0,12 | |
| Enfermedad cerebrovascular | 9 (11,1) | 7 | 2 | 0,62 | |
| Cardiopatía isquémica | 9 (11,1) | 8 | 1 | 1 | |
| Historia de neoplasia | 21 (25,9) | 14 | 7 | 0,01 | |
| Deterioro cognitivo | 16 (19,8) | 14 | 2 | 1 | |
| Tipo de infección | |||||
| Nosocomial | 25 (30,9) | 19 | 6 | 0,17 | |
| Adquirida en la comunidad | 56 (69,1) | 50 | 6 | ||
| Servicio de procedencia | |||||
| Médico | 59 (72,8) | 51 | 8 | 0,73 | |
| Quirúrgico | 22 (27,2) | 18 | 4 | ||
| Tipo de acceso venoso | |||||
| Central | 13 (16) | 12 | 1 | 0,68 | |
| Periférico | 68 (84) | 57 | 11 | ||
| Características de la TADE | |||||
| Autoadministración | 4 (5) | 4 | 0 | 1 | |
| Días de AB previo a TADE (media, DT) | 8,4 ± 8,2 | 9,2 (8,4) | 4 (4,3) | 0,04 | |
| Días de tratamiento con TADE (media, DT) | 11,9 ± 8,5 | 11,8 (7,2) | 12,8 (14,1) | 0,73 | |
AB: antibiótico; DT: desviación típica; EPOC: enfermedad pulmonar obstructiva crónica; TADE: tratamiento antibiótico domiciliario intravenoso.
En cuanto al servicio de procedencia; 59 pacientes (72,8%) procedían de servicios médicos y 22 (27,2%) de servicios quirúrgicos.
Las comorbilidades más frecuentes fueron DM (30,9%), ERC (28,4%), historia de enfermedad neoplásica en los últimos 5 años (25,9%) y EPOC (24,7%). La media del índice de Charlson fue de 6,1; presentando el 88,9% de los pacientes un índice de Charlson de 3 o más puntos.
El 69,1% de las infecciones fueron adquiridas en la comunidad, siendo el principal foco de infección el respiratorio (27,2%) seguido de bacteriemia (16%), infección de la piel y las partes blandas (12,3%) e infección del tracto urinario (ITU) (11,1%). En el 19,8% de los casos el tratamiento fue empírico, sin aislamiento microbiológico, frente al 80,2% donde el tratamiento era dirigido. Mayoritariamente se aisló un único microorganismo (65,4%), solo 12 pacientes (14,8%) presentaron infección polimicrobiana. Pseudomonas aeruginosa fue el microorganismo aislado con mayor frecuencia (39,6%) seguido de enterobacterias (23,6%). Dentro de estas últimas, se aisló Escherichia coli en 9 pacientes, 5 de los cuales eran cepas productoras de betalactamasas de espectro extendido.
El antimicrobiano más frecuentemente administrado fue piperacilina/tazobactam (33,3%), seguido de ceftazidima (24,7%) y cefazolina (16%) (tabla 2). Los pacientes habían recibido una media de 8,4 ± 8,2 días de antiobioterapia previa al inicio del TADE y posteriormente recibieron una media de 11,9 ± 8,5 días de terapia domiciliaria en bomba de infusión elastomérica. La duración media del tratamiento antibiótico, tanto empírico como dirigido, fue de aproximadamente 20 días. Teniendo en cuenta únicamente las infecciones intraabdominales, osteoarticulares y endocarditis, la media de días de antiobioterapia fue de 36,2 ± 11 días.
Características de las infecciones tratadas
| Aislamiento microbiológico | n (%) | |
|---|---|---|
| Polimicrobianas | 12 | |
| Sin aislamiento | 16 | |
| Monomicrobianas | 53 | |
| Enterobacterias | Klebsiella pneumoniae | 4 |
| Escherichia coli | 2 | |
| Morganella morganii | 2 | |
| Enterobacter aerogenes | 1 | |
| Pseudomonas aeruginosa | 24 | |
| Staphylococcus aureus sensible a meticilina | 11 | |
| Staphylococcus aureus resistente a meticilina | 1 | |
| Enterococcus faecalis | 4 | |
| Staphylococcus coagulasa-negativos | 2 | |
| Otros | 3 | |
| Antibiótico administrado | ||
| Ampicilina | 6 (7,4) | |
| Piperacilina/tazobactam | 27 (33,3) | |
| Cefazolina | 13 (16) | |
| Ceftazidima | 20 (24,7) | |
| Cefepima | 3 (3,7) | |
| Ceftazidima/avibactam | 3 (3,7) | |
| Ceftarolina | 1 (1,2) | |
| Meropenem | 8 (10) | |
| Localización de la infección | ||
| Respiratoria | 22 (27,2) | |
| Bacteriemia | 13 (16) | |
| Piel y partes blandas | 10 (12,3) | |
| Urinaria | 9 (11,1) | |
| Endocarditis | 8 (9,9) | |
| Osteoarticular | 6 (7,4) | |
| Intraabdominal | 3 (3,7) | |
| Sistema nervioso central | 1 (1,2) | |
| Otras | 9 (11,1) | |
La principal vía de administración fue a través de un acceso venoso periférico (84%), seguido de catéter venoso central de inserción periférica (PICC) (12,3%) y de reservorio (3,7%). La autoadministración del antibiótico fue realizada por un 4,9% de los pacientes. El 16% de los pacientes presentó complicaciones derivadas del acceso venoso, siendo la mayoría pérdida de vía (n = 5) o extravasación (n = 5) y se reportaron 2 casos de flebitis, todos ellos leves.
El 85,2% de los pacientes presentó una buena evolución de su infección. Cuando analizamos este dato por rango de edad, el 94% de los pacientes mayores de 80 años presentaron buena evolución. Sin embargo, este porcentaje disminuyó hasta un 86% cuando se analizaron todos los pacientes mayores de 65 años. El 50% de los pacientes con mala evolución clínica presentaban infección nosocomial y en el 41,6% la terapia antibiótica fue empírica. La media de días de antiobioterapia previa a la colocación del infusor en el grupo de pacientes con mala evolución clínica fue de 4 días.
Tan solo un paciente presentó complicaciones derivadas de la terapia antimicrobiana (nefrotoxicidad), que requirió ajuste de dosis. La tasa de mortalidad a 30 días tras la finalización del tratamiento antibiótico fue de casi un 25% y la tasa de reingresos a los 30 días del 22,2%.
En el análisis univariante, se asociaron a peor evolución clínica la historia de neoplasia en los últimos 5 años (OR 5,50; IC 95% [1,51-19,96]; p = 0,01) y haber recibido menos días de antiobioterapia previo al inicio del TADE (OR 3,50; IC 95% [1,46-12,32]; p = 0,04). Se asoció a mejor evolución clínica la edad mayor de 80 años (OR 0,19; IC 95% [0,40-0,95]; p = 0,03). La comorbilidad asociada a mayor mortalidad fue la IC (OR 4,10; IC 95% [1,46-13,79]; p = 0,026). Aquellos pacientes procedentes de servicios quirúrgicos tuvieron menor mortalidad (OR 0,76; IC 95% [0,62-0,95]; p = 0,047).
En el análisis multivariante, solo los antecedentes de neoplasia se asociaron a evolución desfavorable (HR 5,35; IC 95% [1,45-19,74]; p = 0,012) y la presencia de IC a mayor mortalidad (HR 3,80; IC 95% [1,23-12,05]; p = 0,027).
DiscusiónLos programas de TADE se llevaron a cabo por primera vez en los años 70 en Estados Unidos1. Desde ese momento, han ido creciendo y evolucionando, con beneficios evidentes tanto para los pacientes como para los sistemas sanitarios. Dentro de esta modalidad de terapia, el uso de bombas de infusión elastoméricas es muy interesante para la administración de antibióticos, sobre todo aquellos tiempo-dependientes11.
En nuestro estudio se observó que múltiples infecciones fueron subsidiarias de este tipo de tratamiento, siendo el respiratorio el principal foco tratado en nuestros pacientes. Este dato concuerda con los resultados publicados en otros estudios realizados en zonas cercanas a nuestro centro16, aunque se observó una mayor incidencia de bacteriemias y menor de ITU.
En cuanto a los resultados microbiológicos, los datos también concuerdan con otras publicaciones, en las que el principal microorganismo aislado es Pseudomonas aeruginosa y el principal antibiótico utilizado piperacilina/tazobactam17. Teniendo en cuenta que carecemos prácticamente de alternativas de tratamiento por vía oral para este patógeno, además de las crecientes resistencias a quinolonas18, resulta lógico que este sea el antimicrobiano usado mayoritariamente.
La duración media total de tratamiento antibiótico fue en torno a 20 días, teniendo en cuenta tanto de tratamiento antibiótico empírico como el dirigido. Considerando las recomendaciones de las guías en patología infecciosa para alguna de las enfermedades diagnosticadas en nuestros pacientes (infección respiratoria, ITU o bacteriemia) puede parecer que el tratamiento se alargó más de lo necesario, pero se debe tener en cuenta que es una media y esta se ve sustancialmente aumentada debido a infecciones complicadas (como por ejemplo, neumonías necrosantes o infecciones intraabdominales) y a los casos de endocarditis e infecciones osteoarticulares, donde la duración de tratamiento recomendada es de 4 a 6 semanas19.
Una característica fundamental en nuestra muestra, tal y como reflejan los resultados, era que se trataba de una población envejecida, con un 45% de pacientes mayores de 80 años. Esto contrasta con otros estudios en los que el porcentaje de la población por debajo de los 70 años es sustancialmente mayor20. A pesar de tratarse de una población envejecida y una elevada carga de comorbilidades, un alto porcentaje de pacientes presentó buena evolución clínica, aunque la tasa de reingresos a 30 días fue mayor que en otros estudios con poblaciones similares16. Esta variabilidad puede deberse a una limitación en nuestro estudio, ya que no fue analizada la causa de reingreso, no diferenciando si se producía por el proceso infeccioso inicial u otra causa. De hecho, existen estudios en los que se observa que solo el 30% de los pacientes con TADE que reingresan, lo hacen debido a un empeoramiento de la infección tratada21.
Llama la atención que se haya observado una peor evolución clínica en pacientes con edades comprendidas entre 65 y 80 años que en aquellos mayores de 80 años. En este aspecto no existe concordancia con otros estudios, donde se observa una peor evolución en franjas de mayor edad21, mientras que en otros no se observa dicha asociación22 en los pacientes tratados con TADE. Probablemente esta discordancia sea multifactorial. En primer lugar, la media del índice de Charlson fue mayor en el subgrupo con peor evolución clínica (7,8) frente a la media global (6,1). Por otra parte, un alto porcentaje de pacientes presentaron infecciones de origen nosocomial y recibieron tratamiento de forma empírica. En último lugar, la media de días de tratamiento antibiótico previo a la colocación del infusor en el grupo de pacientes con mala evolución de la infección fue mucho menor (4 versus 8,4 días) pudiendo no haberse detectado precozmente complicaciones derivadas de la infección, ya que la frecuencia de observación del paciente por personal sanitario es menor en la unidad de HADO.
En cuanto a las variables de interés para predecir la evolución de la infección, en general, nuestros resultados concuerdan con la evidencia disponible, encontrando peor evolución en aquellos individuos con historia actual o en los últimos 5 años de neoplasia23. Destaca en nuestro estudio, que aquellos pacientes procedentes de servicios médicos tuvieron mayor tasa de mortalidad. Esto puede ser debido a que, en nuestro centro, existe asistencia compartida entre el servicio de enfermedades infecciosas y los servicios quirúrgicos, optimizando el tratamiento antibiótico. Además, entre los servicios médicos que han prescrito este tipo de terapia, se encuentra un porcentaje importante de pacientes procedentes del servicio de cuidados paliativos.
La tasa de mortalidad a los 30 días fue elevada, al ser de casi un 25%, pero se debe tener en cuenta que casi un 90% de los pacientes tenían un índice de Charlson ≥3, un 25,9% tenían antecedente de neoplasia previa y un 45,7% procedían del servicio de cuidados paliativos.
Como limitaciones en nuestro estudio, comentar, en primer lugar, su diseño. Para confirmar nuestros resultados y obtener datos más consistentes, deberíamos realizar un estudio de carácter prospectivo y aleatorizado. El tamaño muestral puede ser considerado otra limitación y la explicación a no haber obtenido asociaciones estadísticamente significativas entre determinadas comorbilidades y la evolución y/o mortalidad, encontradas en otros estudios24.
Por último, otro aspecto importante que no se ha tenido en cuenta en este estudio es la vigilancia de ciertas condiciones que afectan al flujo de las bombas de infusión elastoméricas. Un mal control de las mismas puede conllevar a la infradosificación con posibilidad de fracaso terapéutico, aumento de los reingresos hospitalarios y aparición de resistencias a los antibióticos8.
Sería interesante, además, incluir en próximos estudios de este tipo de terapia, tanto el grado de satisfacción como los resultados reportados por los pacientes y familiares mediante la realización, por ejemplo, de encuestas de calidad de vida, además de la realización de un análisis de costes, comparando los costes de esta modalidad de tratamiento con los derivados de una hospitalización convencional16.
Como conclusiones, el uso de bombas de infusión elastoméricas en los programas TADE ha supuesto un enorme avance, permitiendo el manejo terapéutico de infecciones a nivel ambulatorio y siendo una alternativa a considerar en pacientes que necesitan tratamiento antibiótico prolongado por vía intravenosa. Está ampliamente descrito en la bibliografía que esta modalidad cuenta con numerosas ventajas, como mayor comodidad, mejor calidad de vida de los pacientes y cuidadores, reducción de costes y de las complicaciones relacionadas con la hospitalización sin comprometer la eficacia del tratamiento. Además, como hemos observado, puede ser una alternativa útil y eficaz en la población envejecida. No obstante, debemos tener en cuenta que ciertas enfermedades o condiciones pueden afectar de forma negativa a la evolución clínica y mortalidad de los pacientes tratados con TADE en bombas de infusión elastoméricas.
Aportación a la literatura científicaEste estudio muestra datos de eficacia y seguridad en la práctica clínica acerca del TADE en bombas de infusión elastoméricas en un hospital de tercer nivel.
Nuestro estudio aporta nueva evidencia al demostrar que se trata de una buena alternativa en el manejo de pacientes que requieren tratamiento antibiótico por vía intravenosa durante un período de tiempo prolongado, con numerosas ventajas tanto para el propio paciente como para el sistema sanitario.
Responsabilidades éticasLos autores de este trabajo han cumplido con las normas éticas necesarias para su realización.
Se dispone de la aprobación del Comité de Ética de la Investigación de Santiago-Lugo. Código de registro 2019/245.
FinanciaciónEl presente trabajo se ha desarrollado sin financiación.
Conflicto de interesesLos autores declaran no tener conflictos de intereses.
AgradecimientosA Ramón Rabuñal Rey por su colaboración en este trabajo durante el análisis estadístico y la interpretación de los resultados.
Declaración de autoríaTodos los autores han realizado contribuciones sustanciales en cada uno de los siguientes aspectos: adquisición y análisis de datos, el borrador del artículo o la revisión crítica del contenido intelectual y la aprobación definitiva de la versión que se presenta. Sara Ferro Rodríguez ha contribuido a la redacción, revisión y edición del manuscrito, software, recursos, administración del proyecto, metodología, investigación, recopilación de datos y conceptualización. Yelco Chantres Legaspi a la redacción, revisión y edición del manuscrito, software, administración del proyecto, metodología, investigación, curación de datos y conceptualización. Eva María Romay Lema, Blanca Ayuso García, Andrea Barcia Losada y Cristina Rodríguez Díaz contribuyeron a la visualización, validación y supervisión. Paloma Castellano Copa en la redacción, revisión y edición, visualización, validación, supervisión, software, recursos, metodología, investigación y análisis formal. Pedro Peinó Camba a la visualización y validación.