evaluar la calidad de vida de los pacientes con las enfermedades inflamatorias inmunomediadas más prevalentes en España: enfermedad inflamatoria intestinal (EII), psoriasis (Ps), artritis psoriásica (AP), artritis reumatoide (AR) y espondiloartropatías (EspA), y determinar los factores que influyen en su calidad de vida.
Métodosel estudio SACVINFA consistió en un estudio observacional realizado en 4 hospitales de Madrid. Se analizó una cohorte transversal de pacientes adultos diagnosticados de una enfermedad inflamatoria inmunomediada que acudían al servicio de farmacia. La calidad de vida se evaluó mediante el cuestionario EQ-5D-5L (movilidad, autocuidado, actividades habituales, dolor/malestar y ansiedad/depresión) y mediante cuestionarios específicos: SIBDQ-9, DLQI, PsAQoL, QoL-RA y ASQoL.
Resultadosse analizaron un total de 578 pacientes (EII = 25,3%; Ps = 19,7%; EspA = 18,7%; AR = 18,5%; AP = 17,8%). La edad media (DE) fue de 49,8 (12,3) años y el 50,7% eran varones. La puntuación media (DE) para el EQ-5D-5L global fue 0,771 (0,2) y la puntuación media (DE) de la escala visual analógica fue 71,5 (20,0). El tipo de enfermedades inflamatorias inmunomediadas se asoció con diferencias en la calidad de vida, mostrando psoriasis y enfermedad inflamatoria intestinal con valores más altos de EQ-5D-5L que artritis psoriásica, artritis reumatoide y espondiloartropatías, p < 0,05 en todas las comparaciones. Los pacientes con AR, EII y Ps alcanzaron el 70% de la puntuación máxima, mientras que los pacientes con AP y EspA no llegaron al 50% de la puntuación máxima posible.
El sexo femenino, un estado de la enfermedad moderada/grave, una mayor edad y un mayor número de tratamientos previos se correlacionaron con una peor calidad de vida. Sin embargo, la persistencia al tratamiento actual se correlacionó con una mejor calidad de vida.
Conclusioneslos pacientes con enfermedades inflamatorias inmunomediadas tienen afectada la calidad de vida, principalmente en la dimensión dolor/malestar, especialmente en aquellas enfermedades inflamatorias inmunomediadas con componente reumatológico.
To evaluate health-related quality of life perceived by patients with the most prevalent immune-mediated inflammatory diseases in Spain: inflammatory bowel disease (IBD), psoriasis (Ps), psoriatic arthritis (AP), rheumatoid arthritis (RA), and spondyloarthropathies (SpAs), and to determine the factors that influence patient quality of life.
MethodsThe SACVINFA study (SA = satisfaction, CV = quality of life, IN = immune-mediated, FA = pharmacy) consisted of an observational study conducted in 4 hospitals in the Community of Madrid. A cross-sectional analysis was made of adult patients diagnosed with an immune-mediated inflammatory disease who attended the Pharmacy Service. Quality of life was assessed using the EQ-5D-5L questionnaire (mobility, self-care, usual activities, pain/discomfort and anxiety/depression) and specific questionnaires: SIBDQ-9, DLQI, PsAQoL, QoL-RA and ASQoL.
ResultsA total of 578 patients were analyzed (inflammatory bowel disease = 25.3%; psoriasis = 19.7%; spondyloarthropathies = 18.7%; rheumatoid arthritis = 18.5%; psoriatic arthritis = 17.8%). The mean age (SD) was 49.8 (12.3) years and 50.7% were male. The average score (SD) for the global EQ-5D- 5 L was 0.771 (0.2) and the mean (SD) visual analogue scale score was 71.5 (20.0). Type of immune-mediated inflammatory diseases was associated with differences in quality of life showing psoriasis and inflammatory bowel disease higher values of EQ-5D-5L than psoriatic arthritis, rheumatoid arthritis and spondyloarthropathies, p < 0,05 in all comparisons. Patients with RA, IBD, and Ps achieved 70% of the maximum score, while patients with PsA and SpAs did not reach 50% of the maximum possible score.
Female gender, a state of moderate/severe disease severity, an older age and a higher number of previous treatments were correlated with worse quality of life. Conversely, persistence to current treatment correlated with better quality of life.
ConclusionsPatients with immune-mediated inflammatory diseases have markedly affected quality of life, mainly in the pain/discomfort dimension, especially in those immune-mediated inflammatory diseases with a rheumatological component.
El término «enfermedades inflamatorias mediadas por inmunidad» (EIMI) engloba una serie de enfermedades crónicas clínicamente heterogéneas que comparten diversos mecanismos patogénicos y se ven afectadas tanto por factores genéticos como ambientales1. Las enfermedades más prevalentes que constituyen este grupo son la enfermedad inflamatoria intestinal (EII), la psoriasis (Ps), la artritis psoriásica (AP), la artritis reumatoide (AR) y la espondiloartropatía (EspA) (espondilitis anquilosante o indiferenciada). En España, la prevalencia global de las EIMI en mayores de 16 años es del 6,4%2 y afecta a cerca de 3 millones de personas3.
Es bastante frecuente que una misma persona padezca varias EIMI y también es habitual la agregación familiar de múltiples EIMI1, lo que se traduce en un mayor impacto de la enfermedad al verse afectados varios miembros de una misma familia1. Además, las personas con EIMI presentan mayor riesgo de desarrollar comorbilidades y complicaciones derivadas de los efectos crónicos de la inflamación, tales como enfermedades cardiovasculares, síndrome metabólico, diabetes, depresión, hígado graso o trastornos renales, lo que complica el manejo de dichas enfermedades. Por ello, los pacientes con EIMI presentan una morbilidad y grado de discapacidad elevados, que reduce considerablemente su calidad de vida asociada con la salud (CVAS)1. Las personas con EIMI tienen mermada la capacidad para realizar actividades cotidianas4. Por lo tanto, su estado de ánimo y bienestar psicológico pueden afectar a las relaciones sociales y familiares5; en consecuencia, muchas personas no pueden trabajar o requieren una reducción de la jornada laboral6. Teniendo en cuenta todo lo anterior, estas enfermedades tienen un elevado impacto en la sociedad y en la calidad de vida de los individuos que las padecen.
Existen varios métodos para evaluar la CVAS. El EQ-5D-5L es un instrumento genérico para evaluar la CVAS de pacientes, basado en preferencias y que ha demostrado una elevada validez y fiabilidad en diversas enfermedades crónicas7. Además de los instrumentos genéricos, existen cuestionarios específicos que evalúan la CVAS de cada EIMI de forma individual. Conocer la CVAS de los pacientes crónicos es una estrategia que favorece la adaptación de los servicios asistenciales a las necesidades de los pacientes. Por ello, el objetivo de este estudio fue evaluar la CVAS en pacientes con al menos una de las 5 EIMI con mayor prevalencia en España (EII, Ps, AP, AR y EspA) y analizar la influencia de las características sociodemográficas y clínicas en la CVAS de dichos pacientes. No obstante, el estudio SACVINFA también tenía otros objetivos, como evaluar la satisfacción de los pacientes con la atención sanitaria recibida8.
MétodosDiseño del estudioEl estudio SACVINFA (por sus siglas en español SA = satisfacción, CV = calidad de vida, IN = inmunomediada, FA = farmacia) fue un estudio observacional, transversal y multicéntrico basado en evidencias del mundo real realizado por los servicios de farmacia de 4 hospitales del Sistema Nacional de Salud de la Comunidad de Madrid.
El estudio fue aprobado por el Comité Ético de Investigación Farmacéutica del Hospital Universitario Gregorio Marañón y se realizó de acuerdo con la Declaración de Helsinki sobre investigación médica en humanos.
Población de estudioLos criterios de inclusión fueron los siguientes: edad mínima de 18 años y con diagnóstico, como mínimo, de una de las siguientes enfermedades: EII (enfermedad de Crohn y colitis ulcerosa), Ps, AP, AR o EspA; tratamiento con terapias biológicas y un mínimo de 3 visitas al servicio de farmacia para recoger la terapia biológica. Los criterios de exclusión fueron los siguientes: falta de predisposición o capacidad para cumplir con los procedimientos del estudio y el seguimiento, participación actual en un ensayo clínico o incapacidad para entender el español.
VariablesLos datos se obtuvieron entre enero de 2020 y marzo de 2021. Se registraron en un cuaderno de recogida de datos (CRD) y en un diario del paciente, ambos en formato electrónico y alojados en Google Forms. Los investigadores de cada centro cumplimentaron el CRD con los datos obtenidos de las historias clínicas y los registros informáticos del centro, que incluían datos sociodemográficos (edad y sexo), clínicos (enfermedad principal y adicionales, grado de intensidad la enfermedad principal [leve/moderada/intensa], según las escalas clínicas utilizadas en cada enfermedad y el tiempo transcurrido desde el diagnóstico), datos farmacoterapéuticos (terapia biológica actual según la clasificación ATC y vía de administración, posología), la duración de la terapia biológica actual, el tiempo transcurrido desde el inicio del primer tratamiento, el número de terapias biológicas previas y la frecuencia de la dispensación. Todas estas variables se recogieron de forma retrospectiva.
Cuestionarios utilizadosLos pacientes cumplimentaron el diario electrónico del paciente compuesto por 3 cuestionarios: 2 sobre CVAS (el EuroQol-5D-5L genérico y un cuestionario específico para cada EIMI del estudio) y otro sobre la adherencia al tratamiento (test de Morisky-Green).
El cuestionario EQ-5D, desarrollado por el Grupo EuroQol (disponible en www.euroqol.org), es un instrumento genérico y estandarizado desarrollado para describir y evaluar la CVAS9,10. La versión utilizada en este proyecto fue el EQ-5D-5L y consta de 2 partes: el sistema descriptivo del EQ-5D-5L y una escala visual analógica (EVA). El sistema descriptivo EQ-5D-5L comprende 5 dimensiones (movilidad, autocuidado, actividades cotidianas, dolor y malestar y ansiedad/depresión) con una escala Likert de 5 niveles de respuesta y una puntuación asignada del 1 al 5 (1 = sin problemas, 2 = problemas leves, 3 = problemas moderados, 4 = problemas graves y 5 = problemas extremos o debilitantes). Las puntuaciones de las 5 dimensiones se utilizan posteriormente para calcular una puntuación de utilidad general, que oscila entre 0 (peor) y 1 (mejor, sin problemas en ninguna de las dimensiones). En la EVA, los pacientes informan de lo que consideran su estado de salud en una escala de 0 a 100, siendo 0 el peor estado de salud y 100 el mejor9,11.
Los cuestionarios utilizados para cada enfermedad individual fueron los siguientes: 1) el PsAQoL (Psoriatic Arthritis Quality of Life) para la AP12, que consta de 20 preguntas dicotómicas (sí = 1/no = 0). Puntuación global: suma total de las puntuaciones de las preguntas individuales, intervalo 0–20. Cuanto mayor es el número de respuestas positivas, peor es la CVAS; 2) la QoL-RA (Quality of Life-Rheumatoid Arthritis) para la AR13 se compone de 8 preguntas evaluadas con una escala numérica visual de 1 (muy mala calidad de vida) a 10 (excelente). Su valor total se calcula mediante la media de los valores de sus componentes; 3) la ASQoL (Ankylosing Spondylitis Quality of Life) para la EspA14, que consta de 18 preguntas dicotómicas (sí = 1/no = 0). La puntuación total se obtiene como la suma de las puntuaciones de cada pregunta, intervalo 0 (la mejor CVAS) a 18 (la peor CVAS); 4) el SIBDQ-9 (Short Inflammatory Bowel Disease Questionnaire) para EII15, que consta de 9 preguntas con 7 respuestas posibles comprendidas entre 1 (todo el tiempo) y 7 (nunca). La puntuación directa se obtiene sumando la puntuación de cada ítem, intervalo 9–63. Esta puntuación directa se transforma después en una escala de 0 (puntuación directa 9 = peor calidad de vida) a 100 (puntuación directa 63 = mejor calidad de vida), y 5) el DLQI (Dermatology Life Quality Index) para Ps16 que se compone de 10 preguntas referidas a los últimos 7 días. Se responde mediante una escala Likert con 4 respuestas posibles: «nada», «un poco», «bastante» o «mucho». La suma de las puntuaciones proporciona un valor agregado simple entre 0 y 30, y el resultado puede presentarse como un porcentaje del impacto de la afección dermatológica en la calidad de vida del paciente. Cuanto mayor es la puntuación, mayor es el impacto en la CVAS.
El test de adherencia de Morisky-Green consta de 4 preguntas de contraste con respuesta dicotómica (sí/no), que reflejan el comportamiento del paciente respecto al cumplimiento terapéutico. Además, es útil para aportar información sobre las causas del incumplimiento, con una elevada especificidad, un alto valor predictivo positivo y pocos requisitos socioculturales para su comprensión16. Se considera que un paciente presenta adherencia al tratamiento cuando responde a las 4 preguntas en el siguiente orden no/sí/no/no17,18.
Todos los cuestionarios se entregaron a los pacientes durante el periodo del estudio y se recogieron de forma prospectiva.
Análisis estadísticoLa muestra incluyó a todos los pacientes que cumplieron los criterios de selección durante el periodo de estudio. Para determinar posibles variables de confusión, se realizó un subanálisis para cada enfermedad y se analizó cómo influían las características sociodemográficas y clínicas en los resultados de la calidad de vida. En el análisis no se tuvieron en cuenta los datos ausentes.
Para los análisis descriptivos se calcularon las medias y la desviación estándar con las variables cuantitativas y las frecuencias y porcentajes con las variables cualitativas. Se incluyeron los valores mínimo y máximo de los cuestionarios de CVAS específicos para cada enfermedad. Las comparaciones bivariantes de los resultados del cuestionario EQ-5D-5L entre sexos y la adherencia para cada enfermedad se realizaron mediante la prueba t de Student. Para la comparación de la puntuación EQ-5D-5L por cada enfermedad con diferentes variables cuantitativas se utilizó el coeficiente de correlación de Pearson. La comparación de puntuaciones EQ-5D-5L entre las distintas enfermedades se evaluaron con ANOVA y la prueba post hoc de Games-Howell, si se violaba la homocedasticidad, o con la prueba de Scheffé, en caso contrario. En todas las comparaciones se asumió que se cumplía el criterio de normalidad debido al elevado tamaño muestral y se aplicó un valor p igual o inferior a 0,05 para rechazar la hipótesis nula. Los cálculos se realizaron con la versión 4.0.5 del programa informático R.
ResultadosSe seleccionaron un total de 596 pacientes en los 4 centros participantes, de los cuales 18 fueron excluidos (7 por no cumplir los criterios de inclusión y 11 por rechazar completar el diario del paciente), así que el total de pacientes incluidos en el análisis definitivo fue 578 (AP = 17,8%, AR = 18,5%, EspA = 18,7%, EII = 25,3%, Ps = 19,7%).
Las características sociodemográficas y clínicas de los pacientes incluidos en el estudio y la adherencia comunicada por los pacientes se muestran en la tabla 1 complementaria. La edad media y la desviación estándar (DE) de todos los pacientes fue de 49,8 (12,3) años. El 50,7% de los participantes eran hombres. La enfermedad con mayor diferencia entre sexos fue la AR, en la que el 81,3% eran mujeres. La media (DE) en el tratamiento biológico actual era de 4,2 (3,5) años. Al 92,0% de los pacientes se les administró el tratamiento por vía subcutánea. El 60,9% de los pacientes recibían inhibidores del factor de necrosis tumoral alfa (TNF-α). El 42,9% de todos los pacientes presentaban remisión de su enfermedad principal, en el 33,4% era leve y en el 23,7% la enfermedad era moderada/intensa. Además, el 8,3% de los pacientes presentaba una segunda enfermedad, y el 0,3%, 2 enfermedades adicionales. Los pacientes con AP eran más propensos a tener una enfermedad moderada/intensa (34,0%) y a presentar una enfermedad adicional. Por el contrario, los pacientes con Ps tenían menos probabilidades de presentar enfermedad moderada/intensa (1,8%). Según los datos reportados, más del 70% de todos los pacientes presentaba adherencia a tratamiento, y los pacientes con AP fueron el grupo con más cumplimiento (76,8%) y los pacientes con AR (63,1%) el que presentó menos adherencia.
Las características sociodemográficas y clínicas de los pacientes incluidos en el estudio y la adherencia comunicada por los pacientes se muestran en la tabla 1 complementaria. La edad media y la desviación estándar (DE) de todos los pacientes fue de 49,8 (12,3) años. El 50,7% de los participantes eran hombres. La enfermedad con mayor diferencia entre sexos fue la AR, en la que el 81,3% eran mujeres. La media (DE) en el tratamiento biológico actual era de 4,2 (3,5) años. Al 92,0% de los pacientes se les administró el tratamiento por vía subcutánea. El 60,9% de los pacientes recibían inhibidores del factor de necrosis tumoral alfa (TNF-α). El 42,9% de todos los pacientes presentaban remisión de su enfermedad principal, en el 33,4% era leve y en el 23,7% la enfermedad era moderada/intensa. Además, el 8,3% de los pacientes presentaba una segunda enfermedad, y el 0,3%, 2 enfermedades adicionales. Los pacientes con AP eran más propensos a tener una enfermedad moderada/intensa (34,0%) y a presentar una enfermedad adicional. Por el contrario, los pacientes con Ps tenían menos probabilidades de presentar enfermedad moderada/intensa (1,8%). Según los datos reportados, más del 70% de todos los pacientes presentaba adherencia a tratamiento, y los pacientes con AP fueron el grupo con más cumplimiento (76,8%) y los pacientes con AR (63,1%) el que presentó menos adherencia.
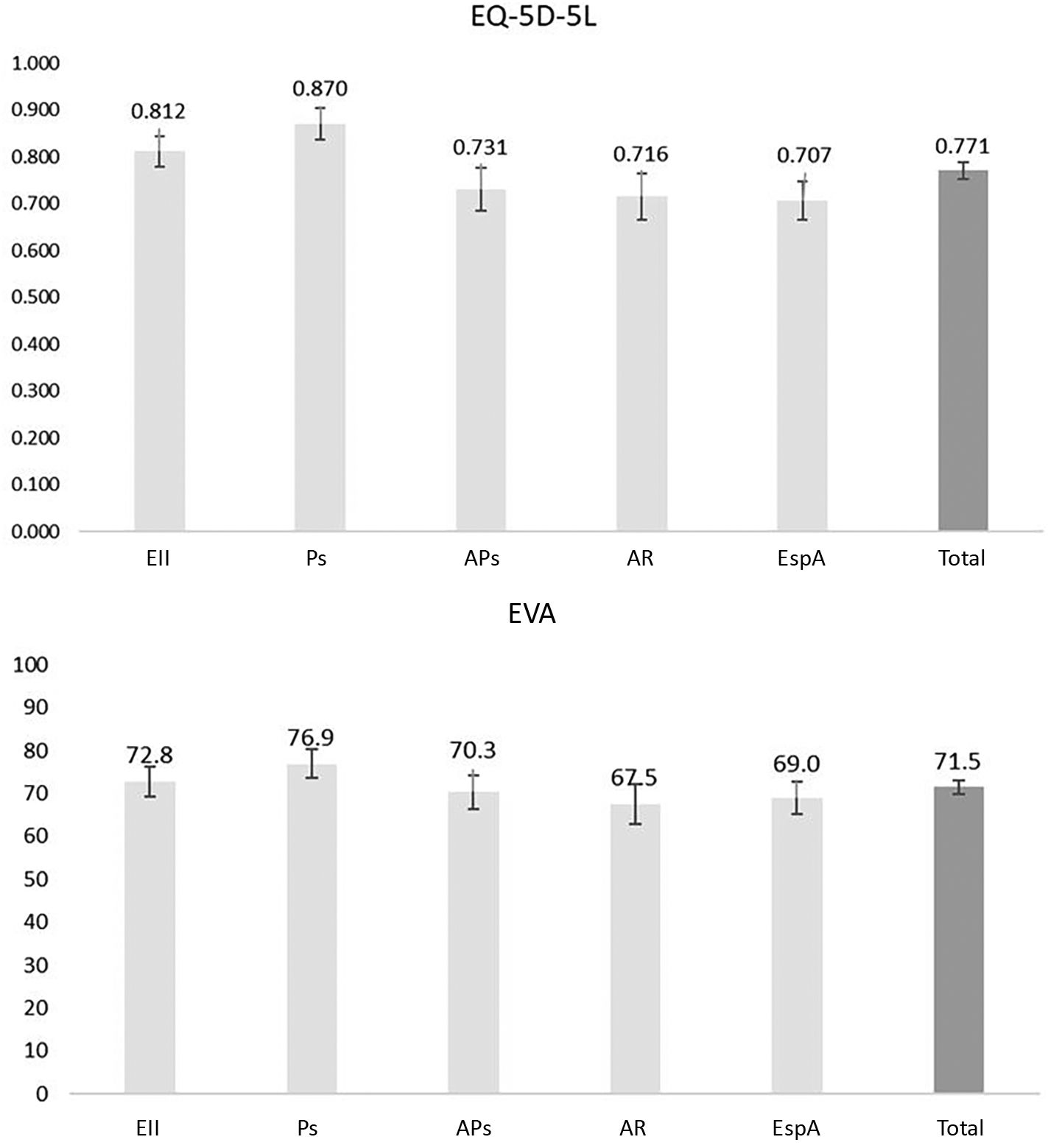
En la figura 1 se muestran las puntuaciones generales del cuestionario EQ-5D-5L. La puntuación general media (DE) de todos los pacientes fue de 0,77 (0,22). Se observaron diferencias significativas entre las enfermedades con mayor puntuación (media [DE]: Ps 0,87 [0,17] y EII 0,81 [0,20]) y menor puntuación (media [DE]: EspA 0,71 [0,21]; AR 0,72 [0,25] y AP 0,73 [0,24]). En cuanto a la EVA, los pacientes con Ps presentaban la puntuación media (DE) más alta, 76,9 (17,6), y los pacientes con AR la puntuación media (DE) más baja, 67,5 (22,5). La diferencia entre estos grupos fue estadísticamente significativa (p = 0,024).
Puntuaciones medias de EQ-5D-5L y EVA.
AP: artritis psoriásica; AR: artritis reumatoide; EII: enfermedad inflamatoria intestinal; EspA: espondilitis anquilosante; EVA: escala analógica visual; Ps: psoriasis.
EQ-5D-5L: Se observaron diferencias estadísticamente significativas en las puntuaciones de pacientes para las siguientes comparaciones por pares: EII vs. AP (p = 0,040); EII vs. AR (p = 0,011); EII vs. EspA (p = 0,001); Ps frente a AP (p < 0,001); Ps vs. AR (p < 0,001); Ps vs. EspA (p < 0,001).
EVA: Se observaron diferencias significativas en las puntuaciones de los pacientes con Ps frente a AR (p = 0,024).
Al evaluar la relación entre las características sociodemográficas y clínicas basales, y las puntuaciones medias de todos los pacientes obtenidas en el EQ-5D-5L, se observó que el sexo, la intensidad de la enfermedad, la edad del paciente, el número de tratamientos previos y la duración de la terapia biológica actual se asociaban con diferencias estadísticamente significativas en la CVAS de los pacientes (tabla 2 complementaria). Las pacientes femeninas notificaron puntuaciones más bajas en el EQ-5D-5L que los participantes masculinos y la diferencia fue estadísticamente significativa para todas las enfermedades (mujeres: 0,74; hombres 0,80; p = 0,002) y para EspA (mujeres: 0,63; hombres 0,75; p = 0,007). Respecto a la intensidad de la enfermedad todos los pacientes con enfermedad moderada/intensa notificaron de una CVAS peor que aquellos en remisión o con enfermedad leve (p < 0,001 para ambos) (tabla 2 complementaria).
Al evaluar la relación entre las características sociodemográficas y clínicas basales, y las puntuaciones medias de todos los pacientes obtenidas en el EQ-5D-5L, se observó que el sexo, la intensidad de la enfermedad, la edad del paciente, el número de tratamientos previos y la duración de la terapia biológica actual se asociaban con diferencias estadísticamente significativas en la CVAS de los pacientes (tabla 2 complementaria). Las pacientes femeninas notificaron puntuaciones más bajas en el EQ-5D-5L que los participantes masculinos y la diferencia fue estadísticamente significativa para todas las enfermedades (mujeres: 0,74; hombres 0,80; p = 0,002) y para EspA (mujeres: 0,63; hombres 0,75; p = 0,007). Respecto a la intensidad de la enfermedad todos los pacientes con enfermedad moderada/intensa notificaron de una CVAS peor que aquellos en remisión o con enfermedad leve (p < 0,001 para ambos) (tabla 2 complementaria).
En cuanto a la relación entre la CVAS y la edad del paciente, la edad estaba inversamente relacionada de forma significativa con la CVAS en la muestra total (p < 0,001) y en los pacientes con AR (p = 0,004). Asimismo, cuanto mayor era el número de tratamientos anteriores al actual, peor era la CVAS en todos los pacientes, (p < 0,001). Esto también se observó en todas las EIMI, salvo en la Ps. Por el contrario, en todos los pacientes se observó una correlación positiva entre la duración de la terapia biológica actual y la CVAS: a mayor persistencia, mayor CVAS (p = 0,005). Esta correlación también se observó en los pacientes con EII y Ps (p = 0,012 y p = 0,049, respectivamente) (tabla 2 complementaria).
En cuanto a la relación entre la CVAS y la edad del paciente, la edad estaba inversamente relacionada de forma significativa con la CVAS en la muestra total (p < 0,001) y en los pacientes con AR (p = 0,004). Asimismo, cuanto mayor era el número de tratamientos anteriores al actual, peor era la CVAS en todos los pacientes, (p < 0,001). Esto también se observó en todas las EIMI, salvo en la Ps. Por el contrario, en todos los pacientes se observó una correlación positiva entre la duración de la terapia biológica actual y la CVAS: a mayor persistencia, mayor CVAS (p = 0,005). Esta correlación también se observó en los pacientes con EII y Ps (p = 0,012 y p = 0,049, respectivamente) (tabla 2 complementaria).
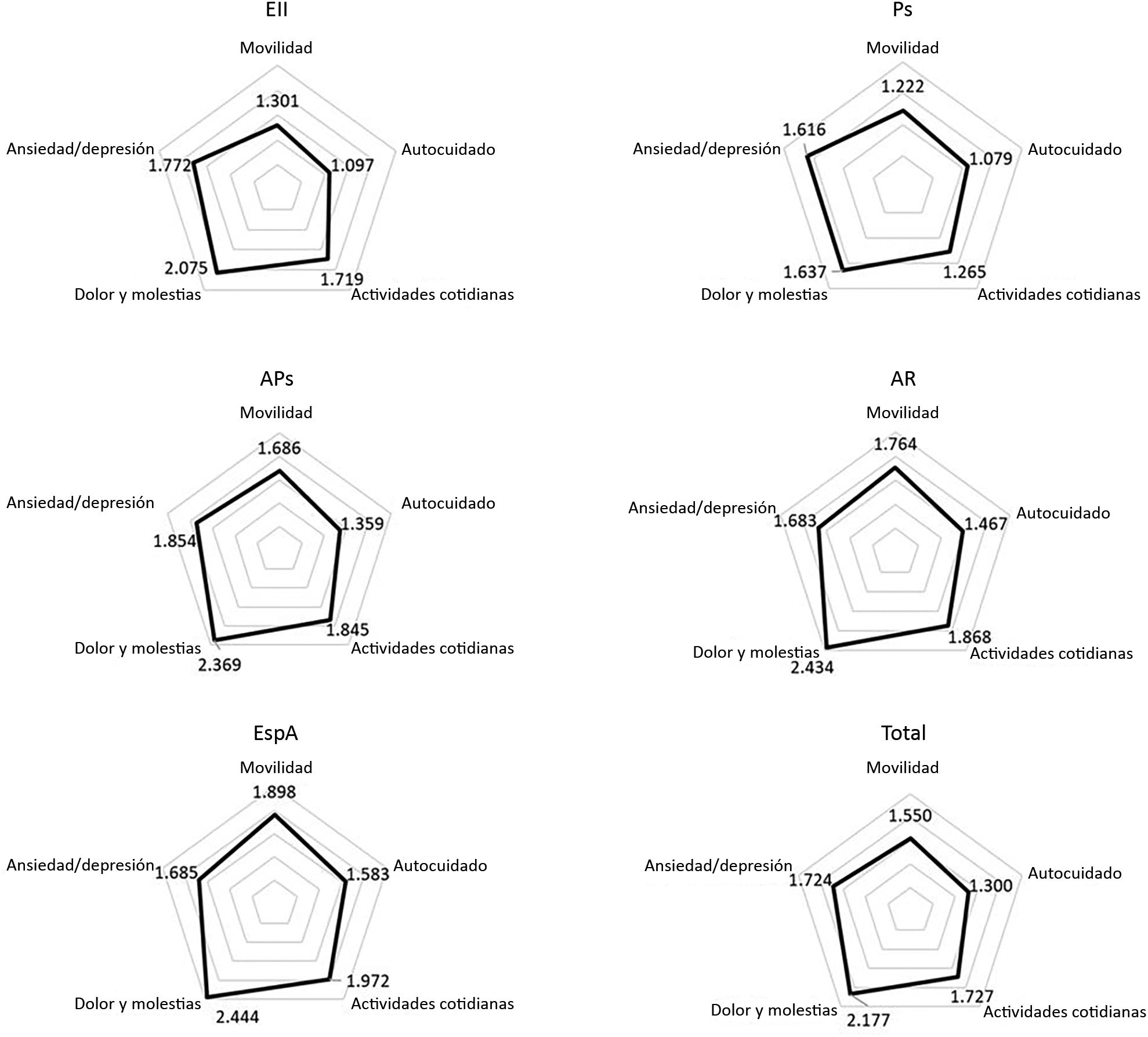
En la figura 2 se muestran los valores de cada dimensión del EQ-5D-5L. Para la muestra total, el dolor y malestar (2.177) tuvo el mayor impacto, seguido de capacidad para las actividades cotidianas (1.727) y la ansiedad/depresión (1.724). Los pacientes con Ps notificaron un mejor estado en cada una de las dimensiones evaluadas.
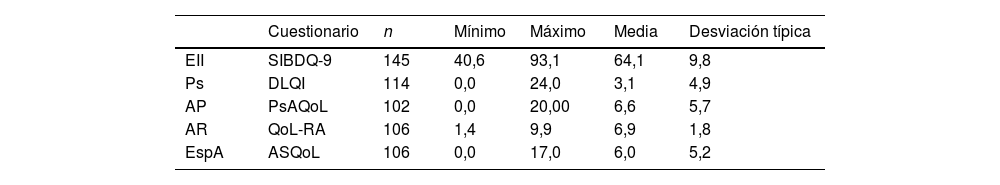
En la tabla 1 se muestran los resultados comunicados por los pacientes en los cuestionarios específicos de cada enfermedad. Los pacientes con AR, EII y Ps alcanzaron el 70% de la puntuación máxima, mientras que los pacientes con AP y EspA no alcanzaron el 50% de la puntuación máxima posible.
Cuestionarios específicos de CVAS
| Cuestionario | n | Mínimo | Máximo | Media | Desviación típica | |
|---|---|---|---|---|---|---|
| EII | SIBDQ-9 | 145 | 40,6 | 93,1 | 64,1 | 9,8 |
| Ps | DLQI | 114 | 0,0 | 24,0 | 3,1 | 4,9 |
| AP | PsAQoL | 102 | 0,0 | 20,00 | 6,6 | 5,7 |
| AR | QoL-RA | 106 | 1,4 | 9,9 | 6,9 | 1,8 |
| EspA | ASQoL | 106 | 0,0 | 17,0 | 6,0 | 5,2 |
AP: artritis psoriásica; AR: artritis reumatoide; EII: enfermedad inflamatoria intestinal; EspA: espondiloartropatía; Ps: psoriasis.
El estudio SACVINFA analizó la CVAS de una amplia cohorte multicéntrica de pacientes con EIMI tratados en los servicios de farmacia de varios hospitales españoles. Se identificaron una serie de factores asociados a una mejor CVAS: sexo masculino, baja actividad de la enfermedad y persistencia en el tratamiento actual. Por el contrario, la edad de los pacientes se asoció negativamente con la CVAS; cuanto mayores eran los pacientes, peor era la CVAS. Hasta donde sabemos, pocos estudios han evaluado la CVAS de pacientes con EIMI. La mayoría de los estudios publicados han evaluado la CVAS de una única enfermedad EIMI, pero el estudio SACVINFA es el primero que evalúa la CVAS de las 5 EIMI con mayor prevalencia en España.
Los resultados del estudio SACVINFA están en línea con los hallazgos publicados sobre la CVAS, tanto en la población general española como en pacientes con enfermedades reumatológicas. En un estudio realizado en adultos no institucionalizados en España (n = 20,587), el sexo femenino, la edad y un mayor número de enfermedades crónicas se asociaban negativamente con la CVAS19. Estos resultados concuerdan con los observados en estudios realizados con pacientes con AR, EspA y enfermedades reumatológicas, en los que las puntuaciones del cuestionario EQ-5D-5L fueron significativamente inferiores en las mujeres que en los hombres20–22. La edad avanzada y la mayor duración de la enfermedad también se asociaron de manera significativa con una puntuación de CVAS más baja21,22. La intensidad de la enfermedad también se asoció con una peor CVAS en los pacientes con AR21 y Ps23. En el estudio SACVINFA, se observó una peor CVAS entre los pacientes con enfermedad moderada/intensa que entre aquellos con enfermedad leve (p < 0,001) o en remisión (p < 0,001) para todas las EIMI excepto para la EII.
Respecto a las dimensiones evaluadas en el cuestionario EQ-5D-5L, la dimensión dolor/malestar fue la que afectó de forma más negativa a la CVAS, seguida de capacidad de realizar actividades cotidianas y ansiedad/depresión. Estos resultados están en consonancia con los publicados en la literatura especializada, ya que las EIMI comparten algunas características sintomáticas comunes, como la fatiga y el dolor, que pueden ser responsables del deterioro funcional y que influyen negativamente en la capacidad para llevar a cabo actividades cotidianas24 y desencadenan trastornos de ansiedad o depresión25, muy frecuentes entre los pacientes con EIMI26. Al comparar las diferentes enfermedades EIMI, cabe destacar que los pacientes que presentaban enfermedades reumáticas inflamatorias (AP, AR y EspA) refirieron un peor estado de salud general en el cuestionario EQ-5D-5L (con puntuaciones de 0,73; 0,72 y 0,71; respectivamente) que los pacientes diagnosticados con EII o Ps (con puntuaciones de 0,81 y 0,87, respectivamente). Las dimensiones más afectadas entre los pacientes con las enfermedades que presentaban un componente reumatológico fueron el dolor/malestar, la capacidad para realizar actividades cotidianas y la movilidad, lo que podría explicarse por la inflamación articular que se produce en estas enfermedades. En otros estudios de pacientes con EIMI se observaron resultados similares, en cuanto a la notificación de un peor estado de salud por parte de los pacientes con un componente reumático e inflamatorio. Ese hecho fue especialmente patente en los dominios relacionados con la movilidad y con limitaciones en desempeño y actividades cotidianas debidas a la función física y al dolor corporal22.
La ansiedad/depresión obtuvo puntuaciones similares en todas las EIMI. Fue la tercera dimensión más afectada en el total de la población, lo que concuerda con otros datos publicados, ya que los pacientes con EIMI tienden a presentar una elevada prevalencia de ansiedad y/o depresión en comparación con la población general27. Además, estudios recientes han demostrado la interacción entre la inflamación y los trastornos del estado de ánimo, especialmente en pacientes con niveles elevados de mediadores inflamatorios como la interleucina-6 (IL-6) y el TNF-α3,28. Asimismo, tanto la duración de la enfermedad como el número de tratamientos que suelen administrarse a lo largo del tiempo podrían repercutir negativamente en el estado de ánimo del paciente.
Los cuestionarios específicos para cada EIMI no son comparables entre sí, pero en la mejor puntuación posible, los pacientes con enfermedades con componente reumatológico notificaron peores resultados en CVAS, a excepción de los pacientes con AR, que alcanzaron una puntuación aproximada de 7/10 en el cuestionario específico para AR.
Por último, cabe mencionar que en el estudio SACVINFA, la adherencia farmacológica no influyó significativamente en la CVAS. Estos resultados también se han observado en otros estudios de pacientes con EIMI (AR y EII), en los que no se observaron diferencias significativas entre los factores psicológicos o la CVAS y la adherencia farmacológica29. Sin embargo, otros estudios de pacientes con EIMI (AP y Ps) observaron una relación positiva entre adherencia y CVAS: aquellos pacientes con buen cumplimiento terapéutico y persistencia con la medicación mostraban mejoras significativas en los parámetros clínicos, la funcionalidad y la calidad de vida30. Asimismo, otro estudio que evaluaba pacientes con AR, AP y EspA, una mayor adherencia al tratamiento correlacionaba con una puntuación más alta en EVA31.
Algunos de los puntos fuertes del presente estudio fueron la participación de una amplia cohorte de pacientes, su realización en un entorno de la vida real, multicéntrico y con un equilibrio razonable entre las enfermedades implicadas. En cuanto a las limitaciones, cabe mencionar que los pacientes no fueron seleccionados aleatorizadamente, lo que habría aportado pruebas más sólidas. Se optó por la inclusión consecutiva de los pacientes para favorecer la recogida de datos debido a los diferentes periodos de recogida de la medicación. Por otro lado, no se consideraron otras comorbilidades con impacto en la calidad de vida, aparte de las enfermedades inflamatorias mediadas por inmunidad. Tampoco se analizó el modelo de atención al paciente, como por ejemplo, la existencia o no de unidades multidisciplinares.
ConclusiónEn los resultados del estudio SACVINFA se muestra que los pacientes con EIMI presentan deterioro de CVAS, especialmente aquellos cuya dolencia incluye un componente reumatológico. En estos pacientes, más edad, ser mujer, enfermedad más intensa y la menor duración del tratamiento se asociaron con una peor CVAS. Sin embargo, la adherencia al tratamiento no afectó a la CVAS. Todos estos hallazgos son importantes y pueden ayudar en la toma de decisiones clínicas y para establecer prioridades durante el manejo de estas enfermedades con el objetivo de mejorar la CVAS de personas afectadas.
Contribución a la literatura científicaEl estudio SACVINFA evaluó la calidad de vida relacionada con la salud de pacientes con las enfermedades inflamatorias inmunomediadas más prevalentes en España. Los resultados del estudio podrían contribuir a generar conocimiento para establecer estrategias que ayuden a optimizar la adherencia, alcanzar los objetivos terapéuticos y prevenir complicaciones.
Responsabilidades éticasLa aprobación ética fue concedida por el Comité ético de investigación clínica del Hospital General Universitario Gregorio Marañón (código: ESC-INM-2019-01).
Consentimiento informadoTodos los participantes dieron personalmente su consentimiento y firmaron por escrito y con fecha el formulario de consentimiento informado.
FinanciaciónEl estudio ha sido financiado por el Instituto Fundación Teófilo Hernando (IFTH-2019-04).
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
.
Declaración de contribución de autoría CRediTAlberto Calvo: Writing – review & editing, Validation, Investigation, Data curation. María Fernández-Pacheco: Writing – review & editing, Methodology, Investigation, Conceptualization. Belén Hernández-Muniesa: Writing – review & editing, Validation, Methodology, Investigation. Rosa Romero-Jiménez: Writing – review & editing, Validation, Methodology, Investigation, Formal analysis, Data curation. Araceli Casado-Gómez: Visualization, Formal analysis, Data curation. Esther Ramírez: Writing – review & editing, Validation, Project administration, Methodology, Investigation, Formal analysis, Data curation, Conceptualization.
Alberto Morellc, Nuria Herreroe, Bárbara Úbedad, Arantza Ais-Larisgoitiaa,b, Elena Lobato-Matillaa,b, Álvaro Muñozf, Miguel Ángel Casadof y Vicente Escudero-Vilaplanaa,b