El ácido valproico (AVP) es un antiepiléptico, cuya utilización se asocia al riesgo de desarrollar encefalopatía hiperamonémica (EHA), una de las reacciones adversas más destacadas de este fármaco1 y favorecida por interacciones medicamentosas. En este sentido, se describe una serie de 3 casos de pacientes que presentaron EHA asociado al uso simultáneo de AVP, fenobarbital (PB) y topiramato (TPM), buscando generar información relevante para la identificación y prevención de situaciones similares.
Descripción de los casosCaso 1Hombre de 42 años, con retraso mental moderado y epilepsia desde los 5 años, manejado con carbamacepina (CBZ), ingresó en la institución por deterioro de conciencia y limitación para la autonomía, cuadro que coincidió con la suspensión de CBZ. El paciente se valoró como hemodinámicamente estable, con Glasgow 10/15 (O2V3M5). Se reinició tratamiento con CBZ sin mejoría y, además presentó crisis convulsiva. Se le administró midazolam (MDZ) y fenitoína, y se trasladó a la unidad de cuidados intensivos (UCI) en estado post-ictal. El video monitoreo electroencefalográfico (VMEEG) identificó un estado epiléptico resistente (EER). En la UCI se suspendió la CBZ, y se continuó el manejo del EER, el paciente necesitó intubación orotraqueal, sedación profunda y medicación escalonada. Se inició AVP (dosis de carga intravenosa [i.v.] de 1.500mg, seguida de 500mg cada 6 h), PB 1.400mg dosis de carga y posteriormente 200mg/día. Debido a que continua con EER, se adicionó TPM 100mg cada 12 h y levetiracetam (LEV), 1.000mg cada 12 h. Durante su evolución, se aumentó la dosis de TPM, gradualmente hasta 200mg cada 12 h, lo que se asoció a una mejoría clínica y electrográfica. Al sexto día de manejo, el VMEEG mostró ondas trifásicas en segmentos del trazado. Además, se encontraron valores plasmáticos de AVP de 66μg/ml, PB 33μg/ml y de amonio de 104μmol/l, al igual que un aumento leve en los valores de transaminasas. La valoración clínica identificó, entre otros, falta de respuesta a estímulos. Por lo anterior, se decidió suspender el AVP e iniciar el desmonte del PB. El paciente presentó mejoría neurológica y del estado de conciencia, al igual que disminución del amonio y de las enzimas hepáticas (tabla 1).
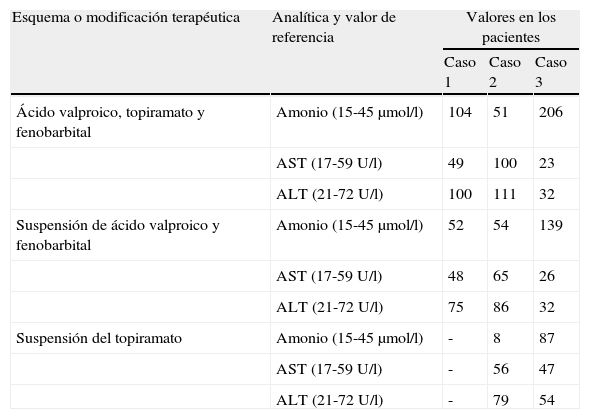
Valores de laboratorio y correlación con la medicación: ácido valproico y topiramato
| Esquema o modificación terapéutica | Analítica y valor de referencia | Valores en los pacientes | ||
| Caso 1 | Caso 2 | Caso 3 | ||
| Ácido valproico, topiramato y fenobarbital | Amonio (15-45μmol/l) | 104 | 51 | 206 |
| AST (17-59 U/l) | 49 | 100 | 23 | |
| ALT (21-72 U/l) | 100 | 111 | 32 | |
| Suspensión de ácido valproico y fenobarbital | Amonio (15-45μmol/l) | 52 | 54 | 139 |
| AST (17-59 U/l) | 48 | 65 | 26 | |
| ALT (21-72 U/l) | 75 | 86 | 32 | |
| Suspensión del topiramato | Amonio (15-45μmol/l) | - | 8 | 87 |
| AST (17-59 U/l) | - | 56 | 47 | |
| ALT (21-72 U/l) | - | 79 | 54 | |
Hombre de 45 años, con epilepsia desde los 21 años, en manejo con CBZ. Ingresó en la institución para realizarle cirugía de epilepsia. En el posquirúrgico, presentó episodio convulsivo tónico-clónico generalizado, por lo que se inició MDZ y fenitoína, el paciente no mejoró de su estado de conciencia, requirió de intubación orotraqueal y fue traslado a la UCI. En este servicio se inició VMEEG y se continuó con el manejo de estado epiléptico con sedación profunda y medicación escalonada, incluyendo AVP. En su evolución, por persistir con EER, se inició PB 1.200mg bolo y luego 200mg/día y TPM 50mg cada 12 h. Posteriormente, se aumentó, en forma gradual, la dosis de TPM a 200mg cada 12 h. En el día 8 se identificó encefalopatía en VMEEG con ondas trifásicas y actividad delta y theta generalizada; además, se encontraron unos valores de amonio en sangre de 51μmol/l, valores plasmáticos de AVP de 38μg/ml y de PB 22 de μg/ml. Por ello, se decidió suspender el PB y el AVP, y aumentar la dosis de TPM a 300mg/12 h. A pesar de este manejo, en el VMEEG persistieron las ondas trifásicas, y el amonio se mantuvo elevado, por lo cual se suspendió el TPM. El paciente empezó a despertar de forma gradual y a presentar normalización de las analíticas de control y de los ritmos cerebrales en el VMEEG (tabla 1).
Caso 3Mujer de 32 años, con epilepsia desde los 3 años, en manejo con CBZ, LEV y gabapentina, ingresó al servicio de urgencias por presentar convulsiones. Se inició manejo MDZ y bolo de AVP de 1.500mg. La paciente continuó con crisis convulsivas, por lo que se decidió trasladar a la UCI y realizar intubación orotraqueal. El VMEEG reportó EER, por lo que se continuó el AVP y se inició PB, bolo de 1g, seguido de 200mg/día, al igual que TPM 50mg cada 12 h. En su evolución, el VMEEG reportó actividad delta generalizada; además, se encontraron valores elevados de amonio (206μmol/l). Por ello, se decidió suspender el AVP y aumentar la dosis de TPM a 100mg cada 8 h. Posteriormente, debido a que los valores amonio continuaban elevados, se suspendió el PB y el TPM. La paciente mostró mejoría neurológica, sin nuevos episodios convulsivos, con evolución electrográfica favorable y recuperación de sus ritmos cerebrales fisiológicos y normalización gradual en niveles de amonio (tabla 1).
Los 3 casos de EHA posiblemente asociados al uso combinado de AVP, PB y TPM fueron comunicados al sistema de farmacovigilancia del país, y la valoración de su causalidad, acorde con el algoritmo de la Organización Mundial de la Salud (OMS)2, fue probable.
DiscusiónEn pacientes con EER, es común la asociación de fármacos antiepilépticos, entre ellos AVP, TPM y PB. Sin embargo, dicha combinación puede inducir hiperamonemia y aumentar el riesgo de una EHA, debido a que estos fármacos disminuyen el metabolismo y la excreción normal de amonio3. En este sentido, en la literatura científica se encuentran descripciones de casos de EHA asociados al uso combinado de AVP y TPM, al igual que de AVP, TPM y PB, posiblemente por una interacción medicamentosa sinérgica4–6. El AVP inhibe la enzima carbamil fosfato sintetasa tipo I, interfiriendo el ciclo de la urea mitocondrial. Por su parte, el TPM aumenta la pérdida renal de bicarbonato y, con ello, afecta a la producción de carbamil-fosfato, clave en el proceso de conversión de amonio a urea. Además el TPM, al igual que el PB, inhibe la síntesis de glutamina sintasa cerebral, enzima que metaboliza el glutamato y amonio a glutamina. Por ello, los pacientes con deficiencias en el ciclo de la urea son los más susceptibles a una hiperamonemia3,7.
La EHA inducida por AVP es una reacción adversa probablemente subdiagnosticado, potencialmente mortal y de incidencia no claramente establecida. Por ello, es fundamental prevenir, identificar e intervenir dicho problema de seguridad. En este contexto, en pacientes en manejo con AVP que desarrollen letargia, vómitos y/o cambios en el estado mental, se deben controlar los valores de amonio en sangre, lo cual debe ser más estricto en pacientes que además estén utilizando TPM y/o PB. Además, en caso de hiperamonemia, se debe suspender el VPA, el PB o el TPM. El monitoreo de signos y síntomas debe ser más estricto durante los primeros 6 meses de manejo, debido a que durante este periodo se presentan la mayoría de reacciones adversas8.