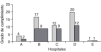INTRODUCCION
Los pacientesoncológicos que desarrollan granulocitopenia como resultadode una quimioterapia mielosupresiva tienen un alto riesgo depadecer infecciones. En la mayoría de ellos lainfección se debe a una persistente colonización delárea afectada por el agente etiológico.
Debido a laneutropenia de base y a otros factores de riesgo (daño demucosas, alteración de la motilidad ciliar,obstrucción neoplásica de tracto respiratorio, etc.)los microorganismos con bajo índice de patogeneicidad puedencausar infecciones posteriores a la colonización, llegandoincluso a provocar una sepsis fatal si no se instaurarápidamente un tratamiento adecuado (1, 2).
En pacientesoncológicos con neutropenia la terapia empíricaconsiste en administrar un tratamiento antibacteriano ante elprimer signo de infección (fiebre) y antes de laidentificación del patógeno causante de lamisma.
El enfoqueestándar de la terapéutica empírica delproceso infeccioso en este tipo de pacientes ha consistidoclásicamente en la utilización de unacombinación de antibióticos, habitualmente unbetalactámico con un aminoglucósido.Las razones que justifican esta combinación son:
-- El mayorespectro antibacteriano que ofrece la combinación de dosfármacos dotados de un espectro de actividad diferente ycomplementario.
-- El efectosinérgico de dos fármacos frente a un determinadomicroorganismo, con la consecuente intensificación de laactividad bactericida.
-- Lalimitación de la aparición de microorganismosresistentes durante el tratamiento (3).
Sin embargo, enlos últimos años la aparición de nuevosantibióticos con un espectro de actividad más amplio,como las cefalosporinas de tercera y cuartageneración o los antibióticoscarbapenémicos, ofrecen la posibilidad de monoterapia.Estudios recientes han demostrado que la monoterapia conceftazidima, cefepime, meropenem o imipenem-cilastatina, es unaalternativa a la terapia combinada como tratamiento empíricopara pacientes oncológicos granulocitopénicos conepisodios febriles (4-7).
No obstante, laterapia combinada puede considerarse aún el tratamiento deelección en pacientes de alto riesgo con bacteriemiapor gramnegativos, especialmente en aquellos con granulocitopeniaprofunda y persistente y/o bacteriemia por Pseudomonasaeruginosa (7, 8).
En el pasado lasterapias antibacterianas empíricas para el tratamiento de laneutropenia febril eran diseñadas para lograr una coberturaóptima en infecciones por gramnegativos, habitualmente lasbacterias predominantes y las que se asociaban con una mayormortalidad. Actualmente numerosos centros hospitalarios han podidoobservar un cambio importante en la etiología de lasinfecciones bacterianas que afectan a estos pacientes, con unincremento en la frecuencia de las bacterias grampositivas, sobretodo estafilococos coagulasa negativos y estreptococos *-hemolíticos yviridans.
Así, enlos siete estudios terapéuticos llevados a cabo por elInternational Antimicrobial Therapy Cooperative Group-EuropeanOrganization for Research and Treatment of Cancer (IATCG-EORTC) laproporción de bacteriemias causadas por cocos grampositivosaumentó desde un 29% del primer ensayo hasta un 69% en elséptimo estudio (7).
La mayoractividad antimicrobiana de las cefalosporinas de tercerageneración, como cefazidima, contra las bacteriasgramnegativas se obtuvo a costa de reducir la actividad contra lasbacterias grampositivas. Como consecuencia, en los pacientes conuna infección primaria por grampositivos la tasa derespuesta tanto a la monoterapia con ceftazidima como a lacombinación de ceftazidima más amikacina ha sidoinsatisfactoria. Además, los pacientes oncológicostratados con ceftazidima presentaron un mayor riesgo de desarrollaruna superinfección por grampositivos (7, 9, 10)
Esto hasuscitado en los últimos cinco años una considerablecontroversia sobre la necesidad de una terapia empíricaespecífica frente a grampositivos en el inicio deltratamiento de episodios febriles en pacientesonco-hematológicos granulocitopénicos.
Recientemente seha utilizado de forma empírica vancomicina o teicoplaninapara mejorar la cobertura frente a bacteriasgrampositivas.
Lamayoría de los estudios realizados por IATCG-EORTC, aunqueno todos, mostraron que la terapia empírica conantibióticos glicopéptidos no era necesaria.En ninguno de ellos la vancomicina o la teicoplanina redujeron lamortalidad total o la causada por infecciones debidas agrampositivos. Además, el uso de vancomicina seasoció con un aumento de la toxicidad (7).
Tambiénhay que considerar que la utilización indiscriminada deglicopéptidos puede dar lugar a la apariciónde resistencias entre estafilococos y enterococos, lo quetendría mayores implicaciones clínicas.
Por tanto, eluso de vancomicina debería limitarse a aquellos centroshospitalarios en los que exista una elevada prevalencia deestafilococos meticilín resistentes (MlRSA) y especialmenteen portadores de catéteres intravenosos permanentes (enestos casos sería aconsejable incluir unglicopéptido como parte del tratamientoantibiótico empírico de inicio: triplecombinación) (8, 11-15).
Dada ladiversidad de regímenes antibióticos propuestos parael tratamiento de la neutropenia febril y la controversia suscitadaen torno a la inclusión o no de glicopéptidoscomo parte de la terapia empírica de inicio, así comoen otros aspectos del tratamiento como la conveniencia de utilizarfactores estimulantes de colonias (16) durante la terapia,nos propusimos diseñar un estudio que nos permitieraconocer:
-- El perfil deutilización de antibióticos y antifúngicosempleados en el tratamiento de la neutropenia febril en el pacienteoncohematológico en nuestro medio.
-- Evaluar losdiferentes protocolos instaurados en nuestros hospitales y,asimismo, establecer el grado de adecuación a losmismos.
MÉTODO
Tipo deestudio
Estudioobservacional, prospectivo, multicéntrico, de tipotransversal.
Serealizó la recogida de datos durante el período detiempo comprendido entre 18 de mayo-19 de junio de 1998 (ambosinclusive).
Pacientesincluidos en el estudio
Laselección de las historias clínicas se realizóatendiendo a los siguientes criterios:
-- Pacientesoncológicos o hematológicos que iniciaron tratamientoantibiótico frente a neutropenia febril en el períodode tiempo considerado. Se incluyeron igualmente aquellos que yaestuvieran en tratamiento cuando empezó elestudio.
-- Se evaluarontodos los casos de neutropenia febril tratados en los servicios deoncología, hematología y UCI.
-- Se haconsiderado que existe neutropenia febril cuando el recuento deneutrófilos es inferior a 500/mm3 y latemperatura corporal es superior a 38,5° C o se producen treselevaciones de temperatura superiores a 38° C durante unperíodo de veinticuatro horas. Segúncriterios de la American Society of Clinical Oncology (ASCO). (12,13)
Recogida dedatos
Las historiasclínicas seleccionadas fueron revisadas con objeto decumplimentar una hoja de recogida de datos previamente consensuadapor todos los hospitales participantes.
Dicha hojaconsta de cuatro apartados:
1. Datos delpaciente. Número de historia clínica, nombre,sexo, edad, diagnóstico del proceso oncológico yservicio en el que ingresa el paciente.
2. Datos deevolución clínica del paciente:
--Situación clínica al inicio de tratamientoantibiótico.
--Situación clínica a las setenta y dos horas de iniciode tratamiento.
--Situación clínica a los siete días detratamiento.
Registrándose en cada uno de ellos recuento deneutrófilos y temperatura corporal.
Al inicio deltratamiento se recogió igualmente la presencia o no de foco,pruebas microbiológicas realizadas al enfermo(hemocultivo/urocultivo), riesgo de nefrotoxicidad y/o alergia abetalactámicos, así como tratamiento (en caso de queexista) con factores estimulantes de colonias y duración delmismo.
3.Tratamiento antibiótico y antifúngico. Seregistró el tratamiento utilizado especifícando encada caso el antibiótico, dosis diaria prescrita yduración del tratamiento.
4.Observaciones.
Valoración de los resultados
Los datosobtenidos se procesaron en una base de datos (Access versión2.0).
Debido alcarácter descriptivo del trabajo se ha optado por expresarlos resultados en función del total de episodios deneutropenia febril registrados (porcentaje). Asimismo paradescribir los datos clínicos y demográficos de lamuestra se ha preferido utilizar como índicesestadísticos la mediana, amplitud intercuartil y valormáximo y mínimo por considerarlos máscorrectos dada la distribución asimétrica que siguenalgunas de estas variables.
Hospitalesparticipantes
-- HospitalCarlos Haya. Málaga.
-- HospitalCiudad de Jaén. Jaén.
-- HospitalGeneral Básico Santa Ana. Motril (Granada).
-- HospitalTorrecárdenas. Almería.
-- HospitalUniversitario San Cecilio. Granada.
-- HospitalUniversitario Virgen de la Victoria. Málaga.
-- HospitalVirgen de las Nieves. Granada.
RESULTADOS YDISCUSION
Evaluación de episodios con neutropeniafebril
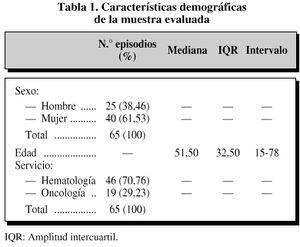
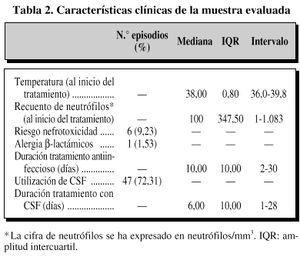
El númerototal de episodios a evaluar durante el período consideradofue de 65. De los cuales, 25 (38,46%) correspondieron a pacientesvarones y 40 (61,53%) a mujeres, con una mediana de edad de 51,5años. Las características demográficas yclínicas de la muestra quedan recogidas en las tablas 1 y 2, respectivamente.
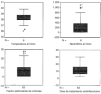
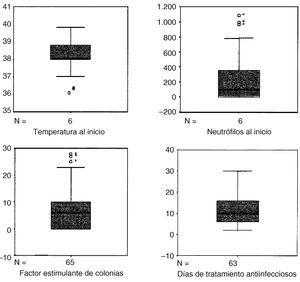
Ladistribución de los valores temperatura, recuento deneutrófilos, duración de tratamiento antiinfeccioso yduración de tratamiento con factores estimulantes decolonias (CSF) se representa en la figura1. Para cada variable la línea central representa lamediana, la altura de las cajas los percentiles 25 y 75 y laslíneas horizontales los valores máximo ymínimo, excepto los valores «outliers»(0).
Figura 1.--«Box-plot» de los datos globalesde temperatura, recuento de neutrófilos, duración detratamiento antiinfeccioso y duración de tratamiento conCSF.
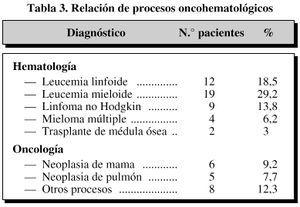
Del total decasos evaluados, 46 (70,76%) corresponden a episodios deneutropenia febril en enfermos hematológicos y 19 (29,23%) apatologías oncológicas. En la tabla 3 se muestra la relación de procesosonco-hematológicos presentes en la muestraestudiada.
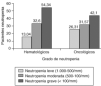
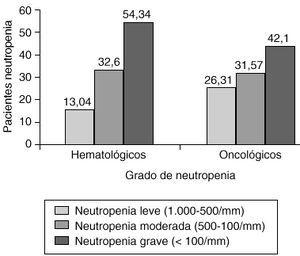
En el momento deinstaurar la terapia empírica antibiótica el mayornúmero de neutropenias severas (54,34%) se observó enpatologías hematológicas (Fig.2). En el grupo de pacientes oncológicos, aunque enmenor proporción (42,34%), también fueron másfrecuentes los casos de neutropenia severa respecto a los decarácter moderado y leve.
Figura 2.--Grado de neutropenia en pacientesoncohematológicos.
Documentar lainfección en estos enfermos no siempre es posible.Así, según el Centro de Cáncer M. D. Andersonde la Universidad de Texas es posible hacerlo en un 47% de lospacientes con fiebre y neutropenia, mientras que en el 53% restantese considera fiebre de origen desconocido.
La frecuencia delas infecciones documentadas microbiológicamente difiere deun centro a otro, influyendo factores tales como el usoprofiláctico de antibióticos en enfermos de altoriesgo (1, 2).
Las infeccionesmás frecuentes en este tipo de pacientes, segúnestudios realizados por la EORTC, se producen en la boca yorofaringe (25%), tracto respiratorio (25%), piel, tejido submucosoy catéteres intravasculares (15%), región perianal(10%), tracto urinario (5-10%), nariz y fosas nasales (5%) y tractogastrointestinal (5%).
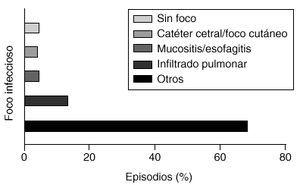
Sin embargo, enel desarrollo de nuestro estudio se observa que la infecciónasociada a catéter es el origen más frecuentementedescrito en este tipo de pacientes, con nueve casos (13,84%),seguida de infecciones secundarias a mucositis/esofagitis concuatro (6,1%) e infiltrado pulmonar con tres (4,2%). El 6,1%restante se debió a otras causas (infecciones urinarias,herpéticas, etc.). En un número importante de casos,45 (69,2%), no se ha localizado el origen de la infección(Fig. 3).
Figura 3.--Focos de infección en pacientesoncológicos con neutropenia.
En lo referentea aislamientos solamente se dispuso de documentación delorigen en un 48,7% de los casos en los que se realizóhemourocultivo.
Tratamientoempírico de la fiebre en el pacienteneutropénico
Tratamientoempírico de inicio
El tratamientoantibiótico de los pacientes neutropénicos debedeterminarse en cada centro hospitalario de acuerdo tanto a lasconsideraciones epidemiológicas de dicha institucióncomo a los patrones de resistencia y el coste.
En lamayoría de los centros se podría tratar a lospacientes considerados de bajo riesgo con monoterapia, mientras queen los enfermos de alto riesgo (< 100/mm3) serecomienda un tratamiento de combinación (17).
Sin embargo,ninguna combinación antibiótica se ha mostradoclaramente superior a otra.
Las respuestasobtenidas en el control inicial de la infección sonsemejantes (60-80%) para las diversas combinacionesantibióticas, pero a pesar de estos buenos resultados y laprobada eficacia del tratamiento combinado hay autores quecuestionan su utilidad a favor de la monoterapia (17).
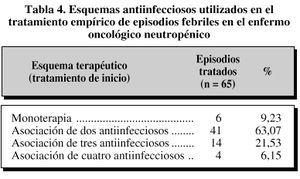
Lavaloración de los distintos esquemas antibióticos ennuestro estudio reveló que en un 9,23% de los episodiostratados se utilizó un sólo antibiótico,siendo el más frecuente en monoterapia cefepime (2g/8 horas i.v.), mientras que en el 90,7% restante se empleóuna terapia combinada (un 63,07% de tratamientos asociaron dosantibióticos).
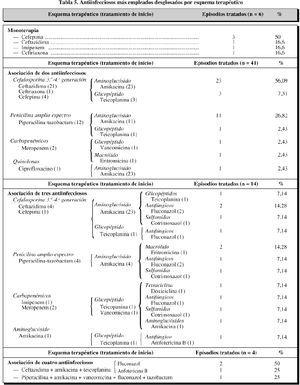
La doblecombinación antibiótica más empleada hasido una cefalosporina más unaminoglucósido (48,78%), siendo ceftazidima lacefalosporina que más frecuentemente se ha asociado. Lasegunda combinación más usada ha sido unapenicilina de amplio espectro (piperacilina-tazobactam)más un aminoglucósido (26,82%). En el otro24,4% se asociaron betalactámicos conglicopéptidos o quinolonas másaminoglucósidos.
En las tablas 4 y 5 se recogen los antiinfecciososmás utilizados, tanto en monoterapia como encombinación, como terapia de inicio (primeras setenta y doshoras de tratamiento) en los episodios febriles.
De las terapiasempiricas combinadas que se aplicaron, el 81,35% de ellasasoció un aminoglucósido como segundoantibiótico, prefiriéndose la amikacina en todos loscasos.
En 11 de losepisodios con neutropenia febril la tapia combinada incluyódesde el inicio un antifúngico, utilizándoseel fluconazol en nueve de ellos y amfotericina B en los dosrestantes. En todos los casos el antifúngico seadministró como agente profiláctico.
El ECOG (EasternCooperative Oncology Group) recomienda la profilaxisantifúngica en pacientes sometidos a TAMO (trasplanteautólogo de médula ósea), en los que aconsejael uso de fluconazol (400 mg/día) o amfotericina B a bajasdosis (0,1-0,25 mg/kg/día) (18).
En nuestroestudio se trató de pacientes diagnosticados de leucemiamielocítica aguda (nueve casos), mieloma múltiple(uno) o sometidos a TAMO (uno); es decir, pacientes considerados dealto riesgo (neutropenia profunda: < 100/mm3 yprolongada: tres semanas), en cuyo caso ciertos autores y a lavista de los resultados obtenidos en ensayos clínicosllevados a cabo en este tipo de pacientes (19) aconsejan igualmentela administración de fluconazol por vía oral (400mg/d) en estos enfermos, aunque serán necesarios másestudios de tipo multicéntrico y aleatorizado paraestablecer la eficacia real, así como las indicaciones delfluconazol en profilaxis.
En cuanto a laincorporación de glicopéptidos (vancomicina yteicoplanina) como parte del tratamiento empírico de inicio,en nuestro estudio fue incluido un glicopéptido en elrégimen antibiótico inicial en 16 de los episodiosevaluados (27,1%), siendo la teicoplanina el más empleado(81,25%). De estos 16 episodios, sólo en ocho estaríajustificada la inclusión del glicopéptido como tripleterapia (cinco por infección de catéter central y enlos tres restantes por sospecha de infección porestafilococo meticilín resistente).
Ajuste deltratamiento antiinfeccioso inicial
Laevaluación de los resultados de la terapia setenta y doshoras después del comienzo es esencial durante elseguimiento del tratamiento antibiótico. La necesidad decambio en el régímen antibiótico viene dadatanto por la persistencia de la fiebre como por la situaciónclínica del enfermo, de modo que siempre que ésta semantenga dentro de un estado satisfactorio, a pesar de lapersistencia de la fiebre, el régimen empíricoinicial no debería modificarse. La fiebre «perse» no es motivo para variar un tratamiento, de hecho puedeser resultado de la quimioterapia, del propio tratamientoantibiótico o de la malignidad subyacente (2).
En contrasteserá precisa una modificación de la terapia cuando laclínica del paciente esté claramente deterioradamientras continúa con el tratamientoempírico.
En nuestroestudio, y tras evaluar persistencia de fiebre y recuento deneutrófilos a las setenta y dos horas del inicio deltratamiento antibiótico, se observó cambio en laterapia inicial en l9 de los 65 episodios estudiados (29,2%). Encuatro de ellos la fiebre había remitido aunque laneutropenia se mantuvo, a pesar de ello en los cuatro seañadió un glicopéptido (vancomicina oteicoplanina) al tratamiento de inicio (sólo en uno de ellosse recogió documentación microbiológica). Enotro de los casos se recuperó la neutropenia y la fiebre,dándose de alta al enfermo, al cual se le modificópreviamente el tratamiento (claritromicina y ciprofloxacino porvía oral).
En el resto deepisodios el enfermo continuaba febril y con cifras deneutrófilos inferiores a 1.000/mm3, por lo quese anadió a la terapia de inicio vancomicina o teicoplanina(ocho casos) o bien fue incorporado un antifúngico (cuatrocasos).
En los dosrestantes la terapia inicial fue sustituida a los tres díaspor otra combinación antibiótica (en una de ellas sejustificó microbiológicamente estamodificación) (tabla6).
Todos losepisodios con neutropenia febril que requirieron unamodificación en el tratamiento habían sido tratadosinicialmente con una terapia combinada (no hubo modificaciones, sinembargo, en los tratados con monoterapia).
Por otra parte,en 10 episodios (15,4%) se observó fiebre persistente orecurrencia seis o siete días después del comienzo dela terapia, por lo que se modificó el tratamiento de inicio(betalactámico másaminoglucósido), añadiéndoseamfotericina B en dos casos (uno de ellos por candidiasisesofágica) y un glicopéptido en otros cinco.En el resto y tras documentación microbiológica sesustituyó el tratamiento empírico inicial por elespecífico.
Utilización de factores estimulantes decolonias
En algunos casoslas infecciones en el paciente neutropénico no responden ala terapia antiinfecciosa, persistiendo en la mayoría laneutropenia profunda y la fiebre a pesar del ajusteantibiótico y la adición deantifúngicos.
Laadministración de G-CSF (filgrastim) y GM-CSF (sargamostrim)pueden reducir la incidencia y duración de episodios deneutropenia febril después de la quimioterapia endeterminados casos. Aunque el uso rutinario de factoresestimulantes de colonias como terapia adyuvante en pacientesneutropénicos con fiebre de origen desconocido noestá recomendado, en determinadas situaciones en las que seprevé un empeoramiento en las condiciones clínicasdel paciente, tales como neumonía, episodios dehipotensión, celulitis severa, infecciones fúngicassistémicas y disfunción multiorgánicasecundaria a la sepsis, el uso de estos agentes síestá indicado.
Segúnrecomendaciones de la ASCO y de la Infectious Diseases Society ofAmerica la terapia con CSF debería considerarsetambién en pacientes de alto riesgo con neutropenia severamantenida e infección documentada que no responde altratamiento antibiótico (20, 21). En caso de utilizarse eltratamiento debe retirarse una vez que el recuento deneutrófilos sea > 500-1.000/mm3 (16).
En nuestroestudio se emplearon CSF en 47 episodios (72,3%) (tabla 2). De ellos, 25 corresponden a pacientesconsiderados de alto riesgo, los cuales presentaron un recuento deneutrófilos < 100/mm3.Según las recomendaciones establecidas por los organismosanteriormente citados (21) tan sólo en un 53,2% de los casosen los que se administraronfactores estimulantes decolonias estaría justificado su uso.
En seis de losepisodios la terapia con CSF se implantó previamente altratamiento antibiótico; en la mayoría (25 casos) seinició a la vez que el tratamiento, mientras que en el restola administración de dichos factores tuvo lugar a lo largodel mismo.
El promedio fuede 6,8 dosis administradas por paciente.
Valoración del cumplimiento deprotocolos
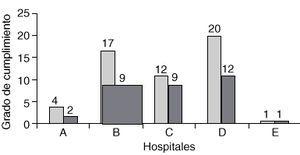
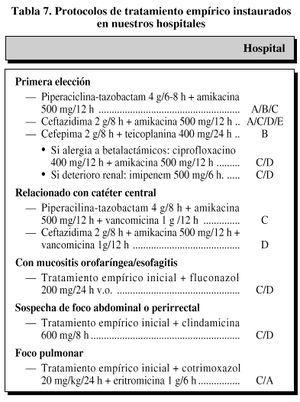
Se ha evaluadoel grado de adecuación de cada hospital a sus propiosprotocolos. En la figura 4 se muestrancinco de los siete centros que han participado en el estudio y queposeen elaborados protocolos de tratamiento (tabla 7).
Figura 4.--Grado de cumplimiento de protocolos porhospital.
Así, A,B, C, D y E representan a cada uno de estos hospitales, figurandoen cada caso el número total de episodios tratados, junto alnúmero de casos en los que el tratamiento se ajustarealmente al protocolo instaurado por dicho centro.
De losresultados expuestos en 1a figura 4 seobserva que C (75%) y D (60%) son los centros hospitalarios conmayor cumplimiento. En el caso de B y A la adecuación alprotocolo fue del 50,6 y 50%, respectivamente. El caso de E no seconsidera representativo por estudiar un solo caso(100%).
De los doshospitales que carecen de protocolo, uno de ellos presentóun porcentaje de cumplimiento alto (40%) para el esquemapiperacilina-tazobactam más amikacina implantado por otroscentros. Asimismo en B y D se observó el cumplimiento (5,8 y5%, respectivamente) de un protocolo diferente al del propiohospital.
Entre losmotivos de incumplimiento más frecuentes se encontraron laadministración, no justificada, de teicoplanina oamfotericina B como terapia de inicio, fluconazol a las cuarenta yocho horas, el empleo de ceftazidima o ceftriaxona en monoterapia obien la asociación de antibióticos que no se ajustana ninguno de los protocolos instaurados tales como laasociación de meropenem o imipenem junto a amikacina yteicoplanina o bien cefepima más amikacina.
A la vista deestos resultados podemos concluir lo siguiente:
-- El estudiorealizado supone una aproximación para conocer en elámbito hospitalario la situación y el perfil deutilización de antiinfecciosos en el tratamiento de laneutropenia febril del enfermo oncohematológico.
-- Eltratamiento empírico más utilizado en nuestro medioha sido la doble combinación de una cefalosporinamás un aminoglucósido (63,07%), siendoceftazidima y amikacina, respectivamente, los que con másfrecuencia se asociaron.
-- Lamonoterapia está generando un interés creciente comoalternativa aconsejable a la terapia combinada, especialmente comotratamiento de pacientes considerados de bajo riesgo. En nuestroestudio, sin embargo, se han tratado con monoterapia neutropeniasmoderadas-severas, presentando los pacientes una buenaevolución
-- Aunque el usorutinario de factores estimulantes de colonias como terapiaadyuvante en la neutropenia febril no está recomendado, suadministración en nuestros centros sanitarios ha sidoelevada (72,3%), si bien en un 53% de los casos su uso se justificapor tratarse de pacientes de alto riesgo con neutropenia mantenida,en cuyo caso sí está indicada suadministración.
-- Lamayoría de nuestros centros hospitalarios poseen protocolosinstaurados que recogen el tratamiento antiinfeccioso de laneutropenia febril. El grado de adhesión a los protocolospor parte de cada centro varía entre un 50 y un75%.
AGRADECIMIENTOS
A laboratoriosAMGEN por su apoyo al Grupo de Trabajo en FarmaciaOncológica de la Zona Andalucía Oriental al quepertenecen los hospitales participantes.