evaluar el impacto en la mejora de la adecuación de la prescripción tras una intervención farmacéutica basada en la revisión y optimización posológica de las prescripciones de sulfametoxazol-trimetoprima.
Métodosse realizó un estudio de intervención de tipo antes-después en un hospital de tercer nivel. El primer periodo (intervención) fue prospectivo y abarcó desde septiembre de 2021 hasta enero de 2022. El segundo periodo (posintervención) fue retrospectivo y comprendió desde marzo hasta diciembre de 2022.
En caso de discrepancia entre la indicación y la posología pautada y recomendada, se notificó al facultativo y se registró el grado de aceptación. En el periodo posintervención, se analizó de forma retrospectiva la adecuación posológica, comprobando si se había intervenido desde el servicio de farmacia. Se realizó análisis estadístico mediante la prueba de chi-cuadrado.
Resultadosen el periodo intervención se analizaron 69 prescripciones y se detectaron 18 inadecuadas (26%), 12 relacionadas con infección por Stenotrophomonas maltophilia. En el periodo posintervención se revisaron 129 prescripciones y 12 fueron consideradas inadecuadas (9%). En el análisis estadístico de los resultados obtenidos (18/69 y 12/129) se observaron diferencias estadísticamente significativas (p = 0,0082).
Conclusionesla intervención farmacéutica en la revisión y optimización posológica mejora el uso de sulfametoxazol-trimetoprima. Los resultados obtenidos aportan evidencia sobre la importancia de la revisión farmacéutica de dichas prescripciones.
Evaluate the impact on improving the appropriateness of prescribing following a pharmaceutical intervention based on the review and optimisation of sulfamethoxazole-trimethoprim prescriptions.
MethodsA before-after intervention study was conducted in a tertiary hospital. The first period, or intervention period, was prospective and ran from September 2021 to January 2022. The second or post-intervention period was retrospective and covered the period March-December 2022.
In case of discrepancy between indication and prescribed and recommended dosage, the physician was notified and the degree of acceptance was recorded. In the post-intervention period, we retrospectively analysed the adequacy of the dosage, checking whether any intervention had been carried out by the Pharmacy Department. Statistical analysis was performed using the chi-square test.
ResultsDuring the intervention period, 69 prescriptions were analysed, and 18 were found to be inappropriate (26%), 12 related to Stenotrophomonas maltophilia infection. In the post-intervention period, 129 prescriptions were reviewed, and 12 were considered inadequate (9%). Statistical analysis of the results obtained in both periods (18/69 and 12/129) showed statistically significant differences (p = 0.0082).
ConclusionsPharmaceutical intervention in the review and optimisation of prescriptions improves the use of sulfamethoxazole-trimethoprim. The results obtained provide evidence of the importance of pharmaceutical review of such prescriptions.
Tras la pandemia de la COVID-19 se observó, en el caso concreto de nuestro hospital, un aumento de aislamientos de Stenotrophomonas maltophilia (S. maltophilia). Entre los factores de riesgo de aparición de este patógeno oportunista se encuentran la inmunodepresión, la estancia prolongada en el hospital, sobre todo en unidades especiales, uso de antibióticos de amplio espectro y utilización de dispositivos intravasculares o ventilación mecánica1,2.
Durante el periodo pandémico se detectaron, de forma ocasional, desde el servicio de farmacia, dosis infraterapéuticas (menores a 9 mg/kg/día de trimetoprima) del tratamiento considerado de elección de dicho microorganismo: sulfametoxazol-trimetoprima o cotrimoxazol (SMX-TMP)3–6.
Dado que, además, se trata de un antibiótico en el que se observan errores asociados a la prescripción por la variabilidad de la posología en función de la indicación y la posibilidad de confusión de dosis entre los 2 principios activos que lo contienen7,8, se planteó un estudio prospectivo de revisión de los pacientes con el tratamiento activo en el hospital.
El objetivo de este trabajo fue evaluar el impacto en la mejora de la adecuación de la prescripción tras una intervención farmacéutica basada en la revisión y la optimización posológica de las prescripciones de SMX-TMP.
Material y métodosSe realizó un estudio de intervención de tipo antes-después en un hospital de tercer nivel. El primer periodo, o periodo de intervención, fue prospectivo y abarcó desde septiembre 2021 hasta enero de 2022. El segundo periodo, o periodo posintervención, fue retrospectivo y comprendió desde marzo hasta diciembre de 2022.
Se incluyeron en ambos periodos todos los pacientes mayores de 18 años que habían recibido tratamiento con SMX-TMP en las fechas mencionadas.
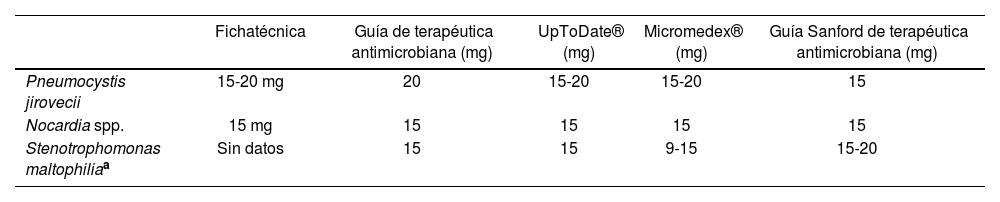
Para establecer los criterios de adecuación posológica, se realizó una búsqueda de las dosis recomendadas de SMX-TMP en las distintas guías de tratamiento3,4, y bases de datos de información de medicamentos5,6, además de la ficha técnica del medicamento9. En el caso concreto del tratamiento de infección por S. maltophilia se consideró adecuada la dosis de, al menos, trimetoprim 9 mg/kg/día6, aunque la mayoría de las fuentes consultadas recomendaban 15 mg/kg/día (tabla 1).
Pautas recomendadas para algunos microorganismos con necesidad de dosis altas, expresadas en forma de trimetoprima/kg/día (consultado 30 agosto 2021)
| Fichatécnica | Guía de terapéutica antimicrobiana (mg) | UpToDate® (mg) | Micromedex® (mg) | Guía Sanford de terapéutica antimicrobiana (mg) | |
|---|---|---|---|---|---|
| Pneumocystis jirovecii | 15-20 mg | 20 | 15-20 | 15-20 | 15 |
| Nocardia spp. | 15 mg | 15 | 15 | 15 | 15 |
| Stenotrophomonas maltophiliaa | Sin datos | 15 | 15 | 9-15 | 15-20 |
Durante el año 2024 las dosis sugeridas han cambiado (8-12 mg/kg/día6,10, 8-15 mg/kg/día5 o 10-15 mg/kg/día11), tras la actualización de la guía IDSA (Infectious Diseases Society of America) 2023 de tratamiento de bacterias gramnegativas resistentes, en la que se recomienda, además, tratamiento combinado12. En la última revisión de dicha guía de 2024, la recomendación de la dosis vuelve a aumentar13 (10-15 mg/kg/día).
Los pacientes se identificaron a través del aplicativo corporativo de prescripción y los datos de los mismos se obtuvieron por la revisión de la historia clínica electrónica de cada paciente.
Se recogieron variables del paciente (edad, sexo y peso), servicio prescriptor, indicación de tratamiento y microorganismo responsable de la infección en caso de confirmación microbiológica.
En el periodo de intervención, en caso de discrepancia entre la indicación y la posología pautada y la recomendada, se notificó al facultativo responsable la recomendación por vía telefónica, además de al equipo PROA (Programa de optimización del uso de antimicrobianos) del centro. Por último, se registró el grado de aceptación de dichas intervenciones.
Posteriormente, en el periodo considerado posintervención se revisaron todos los pacientes tratados con SMX-TMP y se analizó de forma retrospectiva la adecuación posológica, comprobando si en el programa de prescripción electrónica se había registrado alguna intervención farmacéutica. Los datos obtenidos se agruparon en una hoja de Excel.
Se realizó un análisis de estadística descriptiva. Para los datos categóricos se estudiaron la frecuencia y porcentaje de aparición de cada variable, y para los datos cuantitativos se estudió la mediana con su correspondiente rango intercuartil, respectivamente.
Para comparar las poblaciones y los resultados obtenidos en cada periodo se realizó análisis estadístico mediante la prueba de chi-cuadrado utilizando el programa SPSS® V.24. La significación estadística se estableció con un valor de p ≤ 0,05.
ResultadosEn la primera fase del estudio de adecuación posológica se analizaron 69 prescripciones de 65 pacientes, 55% hombres, mediana de edad 66 años (55-79). Las unidades de ingreso fueron: enfermedades infecciosas (15), reanimación (11), respiratorio (10), cardiología (4), cirugía general (4), digestivo (3), hematología (3), medicina interna (3), urología (3), otorrinolaringología (3) y varios (10). Las indicaciones de los tratamientos fueron: 23 tratamientos profilácticos, 5 tratamientos empíricos y 41 dirigidos. Según microorganismo: 14 S. maltophilia, 6 Pneumocystis jirovecii (P. jirovecii), 6 Staphylococcus aureus resistente a meticilina (SARM), 6 Escherichia coli, 3 Klebsiella pneumoniae (K. pneumoniae), 2 Acinetobacter baumannii, uno Toxoplasma gondii y 3 otros.
Se detectaron 18 prescripciones inadecuadas (26%). Doce fueron dosis infraterapeúticas en relación con el diagnóstico microbiológico (10 correspondían a pacientes con infección por S. maltophilia, uno por K. pneumoniae, uno por SARM), uno en relación a un tratamiento empírico, 2 ajustes por función renal en tratamientos dirigidos frente a S. maltophilia y 3 errores de conciliación del tratamiento domiciliario profiláctico. Se aceptaron 17 intervenciones (94%).
En el segundo periodo de análisis retrospectivo se revisaron 129 prescripciones de 127 pacientes, 61% hombres, mediana de edad 66 años (54-77). Las unidades de ingreso fueron: reanimación (28), enfermedades infecciosas (17), respiratorio (16), medicina interna (10), urgencias (9), nefrología (8), cardiología (8), hematología (6), otorrinolaringología (6), cirugía vascular (5), oncología médica (3), urología (3) y varios (10). Las indicaciones de los tratamientos fueron: 43 tratamientos profilácticos, 12 tratamientos empíricos, 3 supresivos y 71 dirigidos. De los tratamientos dirigidos, según el microorganismo: 14 S. maltophilia, 12 E. coli, 8 Klebsiella oxytoca, 6 Enterobacter cloacae, 5 P. jirovecii, 4 A. baumannii, 4 SARM, 3 K. pneumoniae, 3 Nocardia spp., 2 Staphylococcus aureus sensible a meticilina (SASM), 2 T. gondii y 8 otros.
De las 129 prescripciones analizadas de manera retrospectiva, 12 fueron consideradas inadecuadas (9%). Se registraron intervenciones farmacéuticas en 7 prescripciones (5%), y 6 de ellas (86%) fueron aceptadas.
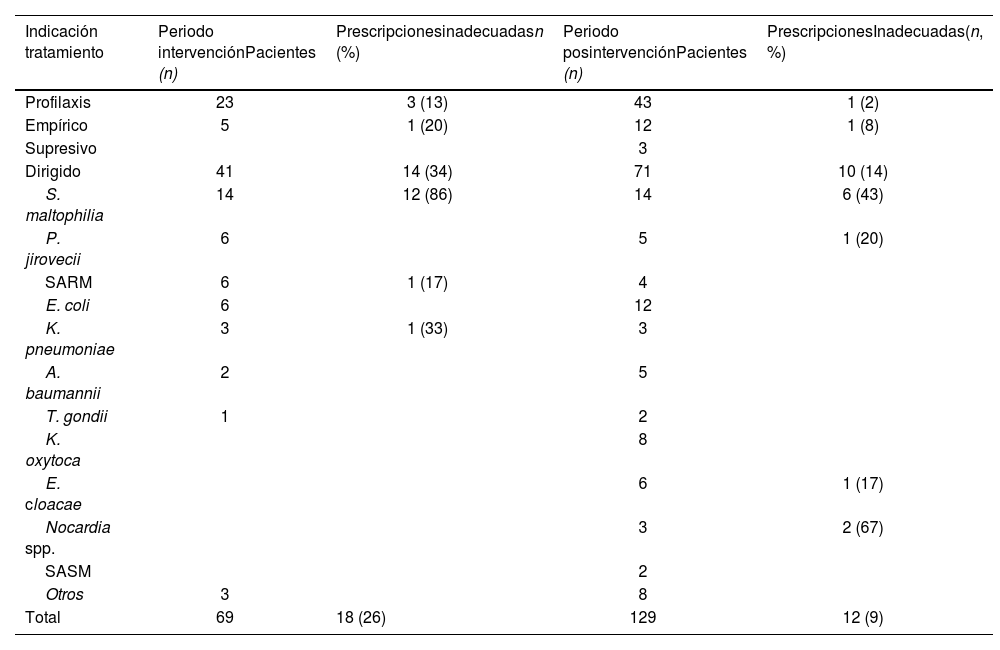
De las prescripciones consideradas inadecuadas, 10 fueron por dosis infraterapéuticas (5 relacionadas con S. maltophilia, 2 con Nocardia spp., una con P. jirovecii, una con E. cloacae, y una con tratamiento empírico), uno por uso de dosis mayores de las recomendadas en profilaxis y un ajuste por función renal en tratamiento dirigido frente a S. maltophilia. Los resultados obtenidos se han resumido en la tabla 2.
Indicación de tratamiento y prescripciones inadecuadas detectadas en ambos periodos
| Indicación tratamiento | Periodo intervenciónPacientes (n) | Prescripcionesinadecuadasn (%) | Periodo posintervenciónPacientes (n) | PrescripcionesInadecuadas(n, %) |
|---|---|---|---|---|
| Profilaxis | 23 | 3 (13) | 43 | 1 (2) |
| Empírico | 5 | 1 (20) | 12 | 1 (8) |
| Supresivo | 3 | |||
| Dirigido | 41 | 14 (34) | 71 | 10 (14) |
| S. maltophilia | 14 | 12 (86) | 14 | 6 (43) |
| P. jirovecii | 6 | 5 | 1 (20) | |
| SARM | 6 | 1 (17) | 4 | |
| E. coli | 6 | 12 | ||
| K. pneumoniae | 3 | 1 (33) | 3 | |
| A. baumannii | 2 | 5 | ||
| T. gondii | 1 | 2 | ||
| K. oxytoca | 8 | |||
| E. cloacae | 6 | 1 (17) | ||
| Nocardia spp. | 3 | 2 (67) | ||
| SASM | 2 | |||
| Otros | 3 | 8 | ||
| Total | 69 | 18 (26) | 129 | 12 (9) |
A. baumannii: Acinetobacter baumannii; E. Cloacae: Enterobacter cloacae; E. coli: Escherichia coli; K. oxytoca: Klebsiella oxytoca; K. pneumoniae: Klebsiella pneumoniae; P. jirovecii: Pneumocystis jirovecii; S. maltophilia: Stenotrophomonas maltophilia; SARM: Staphylococcus aureus resistente a meticilina; SASM: Staphylococcus aureus sensible a meticilina; T. gondii: Toxoplasma gondii.
En el análisis estadístico (prueba de chi-cuadrado) de los resultados obtenidos en ambos periodos (18/69 y 12/129) se observaron diferencias estadísticamente significativas (p = 0,0082).
Mediante el mismo test estadístico se determinó la similitud entre las poblaciones respecto a edad, sexo e indicación de tratamiento, ya que no se encontraron diferencias estadísticamente significativas. En cuanto a los microorganismos, se analizaron solo aquellos con necesidad de dosis altas, no encontrándose tampoco diferencias (p = 0,0504).
DiscusiónDurante la primera fase del estudio de adecuación de dosis se confirmó por el servicio de farmacia que había un porcentaje significativo de prescripciones de SMX-TMP que no se ajustaban a las dosis habituales recomendadas, especialmente en el caso de la infección por S. maltophilia. Este elevado porcentaje también se ha constatado en otro estudio de evaluación de adecuación posológica donde el porcentaje de dosificación inadecuada para S. maltophilia era del 74,3%7. En nuestro caso, se detectaron 2 posibles causas de infradosificación en dichos tratamientos. Por un lado, la información añadida en los antibiogramas de S. maltophilia, en la que figuraba la siguiente dosis recomendada por EUCAST: dosis alta: 0,24 g trimetoprima + 1,2 g sulfametoxazol/12 h oral o IV14, lo que era insuficiente para pacientes con peso mayor a 53 kg. Por otro lado, en la guía de consulta habitual3, en la monografía de cotrimoxazol, figuraba en el apartado de posología como dosis habitual 160/800 mg/8-12 h, y solamente aparecía una pequeña reseña en los comentarios para los microorganismos en los que son necesarias dosis más elevadas y que podía pasar desapercibida. Dicha información aparece en el apartado de posología desde 2023, facilitando la consulta10.
Desde del servicio de farmacia se recomendó el cambio de la información añadida en los antibiogramas. Este cambio, asociado a la labor realizada mediante las intervenciones individualizadas del servicio de farmacia, han podido contribuir a la mejora observada en la adecuación de las dosis pautadas en el periodo posintervención, especialmente en el tratamiento de S. maltophilia. Por otro lado, en el segundo periodo detectamos errores de infradosificación en prescripciones relacionadas con Nocardia spp., para la cual la información de dosis recomendada contenida en el antibiograma tampoco era correcta, por lo que desde el servicio de farmacia también se recomendó el cambio de esta información.
Al igual que se ha observado en otros estudios con antibióticos15, la intervención farmacéutica en la revisión y optimización posológica de las prescripciones, en este caso de SMX-TMP, mejora el uso del antibiótico.
Dado el amplio rango de dosis posible en función de la indicación del tratamiento y la continua actualización de las guías de tratamiento, creemos necesaria la revisión de la posología de SMX-TMP para evitar el alto porcentaje de prescripciones inadecuadas, especialmente en el caso de microorganismos con necesidad de dosis elevadas.
Los resultados obtenidos aportan evidencia sobre la importancia de la revisión farmacéutica de dichas prescripciones, lo que podría promover su implementación en otros centros hospitalarios y considerar su inclusión como objetivo dentro de los PROA.
FinanciaciónLos autores declaran que no recibieron financiación para la realización de este trabajo.
Conflicto de interesesLos autores declaran no tener conflictos de intereses.
Presentación en congresosLa primera parte del estudio (fase inicial), fue presentada en formato póster en el congreso número 67 de la Sociedad Española de Farmacia Hospitalaria (Barcelona, 24-26 de noviembre de 2022).
Declaración de autoríaMaialen Inclán-Conde y José Antonio Domínguez-Menéndez han colaborado en la concepción y diseño del trabajo, la recogida de datos, análisis e interpretación de datos, escritura, revisión crítica y aprobación de la versión final. Clara Vila-Gallego, Maite Vara-Urruchua han colaborado en el diseño, recogida de datos, análisis, revisión crítica y aprobación de la versión final. Ana Victoria Aguirrezabal-Arredondo, Oscar Luis Ferreiro-Beneitez, Matxalen Vidal-García, Pamela Ruiz-Rodríguez han colaborado en el análisis e interpretación de los datos, revisión crítica y aprobación de la versión final para su publicación.
Declaración de contribución de autoría CRediTMaialen Inclán-Conde: Writing – review & editing, Writing – original draft, Visualization, Validation, Supervision, Software, Resources, Project administration, Methodology, Investigation, Formal analysis, Data curation, Conceptualization. Clara Vila-Gallego: Writing – review & editing, Visualization, Validation, Supervision, Methodology, Investigation, Formal analysis, Data curation, Conceptualization. Maite Vara-Urruchua: Writing – review & editing, Visualization, Validation, Methodology, Formal analysis, Data curation, Conceptualization. Ana Victoria Aguirrezabal-Arredondo: Writing – review & editing, Writing – original draft, Visualization, Validation, Supervision, Formal analysis. Oscar Luis Ferreiro-Beneitez: Writing – review & editing, Writing – original draft, Visualization, Validation, Supervision, Formal analysis. Matxalen Vidal-García: Writing – review & editing, Writing – original draft, Visualization, Validation, Supervision, Formal analysis. Pamela Ruiz-Rodríguez: Writing – review & editing, Writing – original draft, Visualization, Validation, Supervision, Formal analysis. José Antonio Domínguez-Menéndez: Writing – review & editing, Writing – original draft, Visualization, Validation, Supervision, Resources, Project administration, Methodology, Investigation, Formal analysis, Data curation, Conceptualization.