los objetivos son conocer la opinión de neurólogos y farmacéuticos hospitalarios sobre aquellos aspectos aún en el debate respecto al papel de los anticuerpos monoclonales anti-CGRP en el tratamiento preventivo de la migraña. Identificar aquellas controversias aún existentes. Proponer recomendaciones consensuadas de mejora asistencial. Y promover el acceso de los clínicos y los pacientes a estos nuevos tratamientos en la prevención de la migraña con fármacos biológicos, a fin de mejorar la atención y seguimiento del paciente.
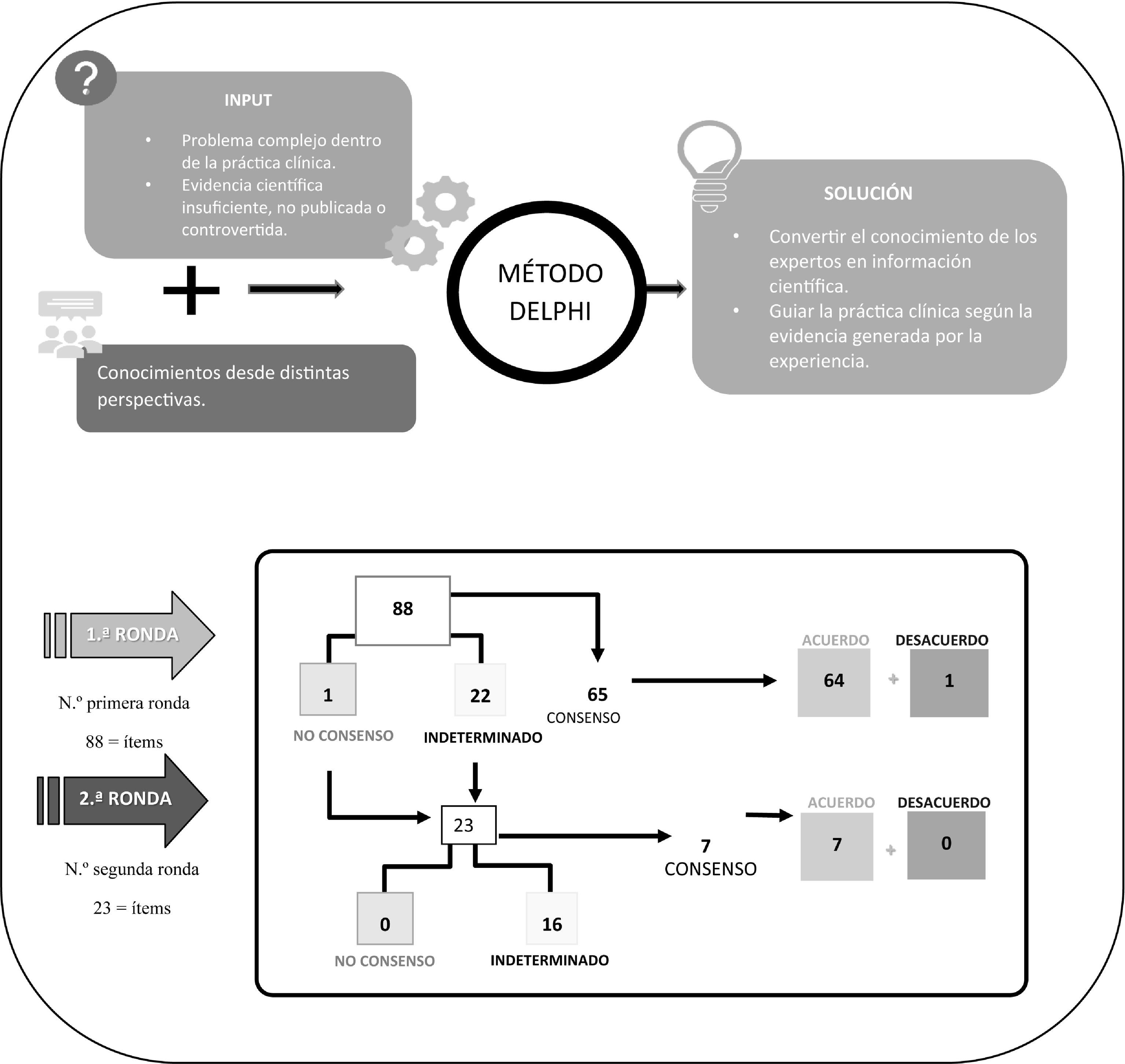
Métodosse identificaron y valoraron recomendaciones para la utilización de fármacos biológicos en la prevención de la migraña a través de la metodología de consenso Delphi, proponiendo 88 aseveraciones agrupadas en 3 temas: un módulo de clínica que trata sobre el manejo de los tratamientos biológicos en la migraña, un módulo de pacientes que trata sobre las estrategias de educación al paciente y mejora de la adhesión y un módulo de coordinación que incluye las aseveraciones relacionadas con las estrategias para mejorar el trabajo conjunto entre los 2 colectivos. Se empleó la escala ordinal de Likert de 9 puntos para puntuar dichas recomendaciones y, posteriormente, los datos se analizaron estadísticamente a través de diferentes métricas.
Resultadostras las 2 rondas de consulta, se alcanzó consenso en el acuerdo en 71 aseveraciones (80,7%) y consenso en el desacuerdo en una de ellas (1,1%), quedando como indeterminadas 16 aseveraciones (18,2%) de las 88 debatidas.
Conclusionesel alto grado de consenso indica que la opinión de neurólogos y farmacéuticos hospitalarios sobre el papel de los anticuerpos monoclonales anti-CGRP en el tratamiento de la migraña es muy similar y permite identificar aquellas controversias aún existentes, para mejorar la atención y seguimiento del paciente con migraña.
The objectives are to know the opinion of neurologists and hospital pharmacists on those aspects still under debate regarding the role of anti-CGRP monoclonal antibodies in the preventive treatment of migraine. To identify those controversies that still exist. To propose agreed recommendations for improvement of care. And to promote access of clinicians and patients to these new treatments in the prevention of migraine with biological drugs, in order to improve patient care and follow-up.
MethodologyRecommendations for the use of biological drugs in the prevention of migraine were identified and evaluated through the Delphi consensus methodology, proposing 88 statements grouped into three themes: a clinical module that deals with the management of biological treatments in migraine; a patient module that discusses patient education and adherence improvement strategies; and a coordination module that includes statements related to strategies to improve joint work between the two groups. The 9-point Likert ordinal scale was used to score these recommendations and, subsequently, the data was statistically analyzed through different metrics.
ResultsAfter both rounds of voting, consensus was reached in agreement on 71 of the 88 statements (80.7%), leaving one statement (1.1%) with consensus in disagreement and 16 remaining as indeterminate (18.2%).
ConclusionsThe high degree of consensus indicates that the opinion of neurologists and hospital pharmacists on the role of anti-CGRP monoclonal antibodies in the treatment of migraine is very similar and allows identifying those controversies that still exist, to improve the care and follow-up of patients with migraine.
La insuficiente eficacia y tolerabilidad de los tratamientos preventivos orales actuales de la migraña ha impulsado la búsqueda de nuevas estrategias terapéuticas, permitiendo el desarrollo de anticuerpos monoclonales (AMC) dirigidos específicamente frente al péptido relacionado con el gen de la calcitonina (CGRP; calcitonin gene related peptide), relevante en la fisiopatología de la migraña o frente a su receptor (AMC anti-CGRP)1.
Estos AMC anti-CGRP han demostrado su seguridad y eficacia en ensayos clínicos y estudios de la vida real. No atraviesan la barrera hematoencefálica evitando la aparición de acontecimientos adversos en el sistema nervioso central, no existe riesgo de interacciones farmacológicas respecto a los tratamientos preventivos tradicionales al no metabolizarse en el hígado, inician su respuesta tras pocas semanas de iniciarse el tratamiento y cuentan con una excelente tolerabilidad. Además, han demostrado ser eficaces en la migraña episódica y crónica, tanto en parámetros objetivos como subjetivos2.
Además, en raras ocasiones se han notificado reacciones anafilácticas, aunque están contraindicados en pacientes con hipersensibilidad al principio activo y se desconoce su seguridad a largo plazo en pacientes con antecedentes o riesgo cardiovascular, así como en mayores de 65 años. Y, como medida de precaución, es preferible evitar su uso durante el embarazo3,4.
Los AMC anti-CGRP que han mostrado eficacia tanto en la migraña crónica como en la episódica son: eptinezumab (aún no comercializado en España), galcanezumab, fremanezumab y erenumab5–8. Y, en España, están financiados para el tratamiento preventivo de pacientes con migraña episódica de alta frecuencia (8–14 días de migraña/mes) y en aquellos con migraña crónica tras el fracaso de 3 tratamientos preventivos (incluyendo toxina botulínica en pacientes con migraña crónica) utilizados en las dosis adecuadas y durante un mínimo de 3 meses.
El consenso del equipo pluridisciplinar en el tratamiento de los pacientes con migraña permitirá avanzar en el manejo de estos fármacos y conseguir los mejores resultados en la salud.
Por ello, los objetivos de este documento de consenso fueron: conocer la opinión de neurólogos y farmacéuticos hospitalarios consensuando aspectos aún en debate sobre el papel de los AMC anti-CGRP en el tratamiento de la migraña, identificar aquellas controversias aún existentes, proponer recomendaciones consensuadas de mejora asistencial y promover el acceso de los clínicos y los pacientes a estos nuevos tratamientos en la prevención de la migraña con fármacos biológicos, a fin de mejorar la atención y seguimiento del paciente.
MétodoInicialmente se constituyó un comité científico (CC) formado por 4 farmacéuticos hospitalarios y 4 neurólogos expertos en migraña, que revisó la bibliografía más reciente sobre su tratamiento y propuso 88 aseveraciones agrupadas en 3 módulos: aspectos clínicos en el manejo de los tratamientos biológicos, estrategias de educación al paciente y mejora de la adherencia, y coordinación para mejorar el flujo de trabajo.
Posteriormente el CC seleccionó a un panel inicial de 62 neurólogos y farmacéuticos hospitalarios con reconocida experiencia en el control y seguimiento de pacientes con migraña que, debido a la disponibilidad profesional de 3 de los panelistas, quedó reducido a 59 en la segunda ronda.
El equipo técnico-científico de la Unidad de Investigación de Luzán 5 Health Consulting participó en el soporte técnico y metodológico del proyecto.
El método elegido para debatir las aseveraciones propuestas fue la elaboración de un consenso con metodología Delphi, una técnica de comunicación estructurada que, mediante la guía y supervisión de los coordinadores y sin necesidad de presencialidad, permite a un grupo de expertos numeroso, obtener una solución a partir del planteamiento de un problema complejo dentro de la práctica clínica o de escasa evidencia9–11.
Siguiendo dicho método, el cuestionario se envió a los panelistas para que respondieran mostrando su grado de acuerdo con las aseveraciones, proporcionando para ello una escala ordinal única tipo Likert de 9 puntos estructurada en 3 grupos según nivel de acuerdo-desacuerdo, siendo de 1 a 3 interpretado como no consenso, de 4 a 6 interpretado como indeterminado y de 7 a 9 interpretado como expresión de apoyo. Aquellas aseveraciones sin el suficiente consenso pasaron a una segunda ronda. El tiempo total empleado para obtener los resultados fue de 4 meses y toda la comunicación se realizó a través de correo electrónico y de la plataforma Delphi.
Por último, el CC se reunió para debatir y analizar los resultados, definiendo cada aseveración como: sí consenso cuando 2/3 o más (≥66,66%) puntúan dentro de los rangos de 1 a 3 o de 7 a 9; no consenso cuando las puntuaciones de 1/3 o más (≥33,33%) se sitúan en el rango de 1 a 3 y otro tercio en el rango de 7 a 9; e indeterminado cuando la mediana de la puntuación se sitúa entre el rango de 4 a 612.
ResultadosComo se muestra en la figura 1 tras la celebración de 2 rondas de consulta, se alcanzó consenso en el acuerdo en 71 aseveraciones (80,7%) y consenso en el desacuerdo en una aseveración (1,1%), quedando como indeterminadas 16 aseveraciones (18,2%) de las 88 totales, cuyas puntuaciones y grado de acuerdo se muestran en las tablas 1, 2 y 3.
Módulo de clínica
| Mediana(IIQ) | %acuerdo | %desacuerdo | |
|---|---|---|---|
| 9 (1) | 95,2 | 1,6 |
| 8 (2) | 79,0 | 8,1 |
| 7 (5) | 51,7 | 31,7 |
| 8 (3) | 67,8 | 9,7 |
| 8 (2) | 85,5 | 4,8 |
| 8 (1) | 91,9 | 1,6 |
| 8 (5) | 67,7 | 24,2 |
| 9 (2) | 80,6 | 6,5 |
| 8 (2) | 83,9 | 1,6 |
| 7 (2) | 67,7 | 11,3 |
| 8 (2) | 91,9 | 1,6 |
| 8 (4) | 72,6 | 12,9 |
| 8 (2) | 79,0 | 0,0 |
| 7 (2) | 58,3 | 13,3 |
| 7 (2) | 73,3 | 1,7 |
| 5 (2) | 20,0 | 26,7 |
| 3 (3) | 11,7 | 61,7 |
| 7 (2) | 60,0 | 18,3 |
| 7 (2) | 60,0 | 8,3 |
| 6 (3) | 38,3 | 16,7 |
| 9 (1) | 88,7 | 3,2 |
| 7 (2) | 72,6 | 9,7 |
| 7 (2) | 74,2 | 8,1 |
| 8 (1) | 87,1 | 1,6 |
| 8 (1) | 75,8 | 4,8 |
| 7 (0) | 81,7 | 6,7 |
| 7 (0) | 80,0 | 3,3 |
| 7 (1) | 77,4 | 3,2 |
| 7 (2) | 74,2 | 12,9 |
| 8 (3) | 72,6 | 9,7 |
| 8 (3) | 74,2 | 8,1 |
| 8 (3) | 69,4 | 12,9 |
| 6 (3) | 36,7 | 20,0 |
| 9 (1) | 93,6 | 3,2 |
| 7 (2) | 71,7 | 3,3 |
| 5 (4) | 30,0 | 26,7 |
| 5 (2) | 15,0 | 28,3 |
| 2 (3) | 11,7 | 65,0 |
| 7 (3) | 58,3 | 10,0 |
AMC: anticuerpos monoclonales.
MIDAS: Migraine Disability Assessment Scale.
Módulo de pacientes
| Mediana(IIQ) | %acuerdo | %desacuerdo | |
|---|---|---|---|
| 9 (0) | 100,0 | 0,0 |
| 9 (0) | 98,4 | 0,0 |
| 9 (1) | 85,5 | 4,8 |
| 9 (1) | 85,5 | 4,8 |
| 9 (1) | 90,3 | 6,5 |
| 9 (1) | 98,4 | 1,6 |
| 9 (1) | 95,2 | 0,0 |
| 9 (0) | 95,2 | 0,0 |
| 9 (1) | 98,4 | 0,0 |
| 9 (0) | 98,4 | 0,0 |
| 9 (0) | 96,8 | 0,0 |
| 9 (0) | 98,4 | 0,0 |
| 9 (2) | 95,2 | 1,6 |
| 9 (0) | 100,0 | 0,0 |
| 9 (0) | 100,0 | 0,0 |
| 9 (0) | 98,4 | 1,6 |
| 9 (0) | 98,4 | 0,0 |
| 9 (1) | 98,4 | 0,0 |
| 9 (0) | 98,4 | 0,0 |
| 7 (2) | 71,7 | 1,7 |
| 9 (1) | 95,2 | 0,0 |
| 9 (1) | 98,4 | 0,0 |
| 9 (1) | 95,2 | 0,0 |
| 8 (2) | 88,7 | 1,6 |
| 9 (1) | 98,4 | 0,0 |
AMC: anticuerpos monoclonales.
MIDAS: Migraine Disability Assessment Scale.
Módulo de coordinación
| Mediana(IIQ) | %acuerdo | %desacuerdo | |
|---|---|---|---|
| 9 (1) | 93,5 | 0,0 |
| 9 (0) | 95,2 | 0,0 |
| 9 (2) | 80,6 | 3,2 |
| 9 (1) | 93,6 | 0,0 |
| 9 (1) | 91,9 | 1,6 |
| 8 (3) | 70,0 | 8,3 |
| 5 (2) | 21,7 | 23,3 |
| 5 (3) | 41,7 | 23,3 |
| 4 (3) | 5,0 | 46,7 |
| 8 (2) | 90,3 | 1,6 |
| 9 (1) | 91,9 | 0,0 |
| 8 (2) | 75,8 | 3,2 |
| 9 (1) | 93,5 | 0,0 |
| 9 (1) | 91,9 | 1,6 |
| 9 (1) | 87,1 | 3,2 |
| 8 (3) | 72,6 | 1,6 |
| 8 (2) | 87,1 | 1,6 |
| 9 (4) | 71,7 | 16,7 |
| 4 (5) | 26,7 | 48,3 |
| 9 (1) | 95,2 | 0,0 |
| 7 (3) | 67,7 | 14,5 |
| 9 (1) | 93,5 | 0,0 |
| 8 (2) | 75,8 | 9,7 |
| 2 (3) | 9,7 | 72,6 |
AMC: anticuerpos monoclonales.
Este módulo agrupó 39 aseveraciones de las que 27 fueron consensuadas en el acuerdo y 12 quedaron como indeterminadas (tabla 1).
En relación con el inicio del tratamiento y la valoración del paciente, se alcanzó un consenso superior al 85% respecto a que los criterios para seleccionar los pacientes a los que se financia el tratamiento con AMC eran correctos, que la valoración previa debería incluir una escala de impacto o discapacidad y que previamente al inicio del tratamiento, el paciente debía aportar un calendario que reflejase el número de días de cefalea y migraña, así como el uso de medicación sintomática o la necesidad de acudir a urgencias.
Para el rango comprendido entre 66 y 85%, se alcanzó el consenso al valorar como criterio de fracaso terapéutico la falta de tolerabilidad a tratamientos preventivos orales, y como criterio de falta de respuesta el uso de 2 ciclos de toxina botulínica, con uso de dosis de 195 U en al menos uno de ellos. También el considerar la no necesidad de suspender inicialmente un tratamiento preventivo oral o la toxina botulínica en los pacientes que presentan una respuesta parcial antes de iniciar un AMC, y la importancia de que cada centro disponga de todos los AMC para que pueda adquirir experiencia de uso con todos ellos.
Sin embargo, quedaron como indeterminadas el considerar como fracaso la contraindicación al tratamiento, la necesidad de monitorizar los niveles séricos de AMC y los niveles de anticuerpos antifármaco ante la falta de eficacia, y el uso de AMC con precaución en los pacientes con diagnóstico confirmado con inicio de la migraña a partir de los 55 años.
En relación con la duración y respuesta al tratamiento, se obtuvo consenso superior al 85% en que el uso concomitante de AMC con otros biológicos debería considerarse de forma individualizada, y para el rango comprendido entre 66 y 85% el considerar que el parámetro más importante para valorar la efectividad era la disminución del número de días con migraña y el considerar «respondedor» a un paciente, cuando esa disminución del número de días sin migraña superaba el 50% en episódica y el 30% en crónica. También sobre la capacidad de un paciente para responder a un AMC independientemente de no haberlo hecho antes a otro y a aconsejar el uso de un AMC diferente, cuando no ha habido respuesta con el primero. Respecto a si era seguro, se valoraron como indeterminadas el cambio inmediato de AMC sin realizar un periodo de lavado o si se debería esperar un periodo de 5 vidas medias como periodo de lavado para el inicio de un AMC en un paciente que estaba recibiendo otro ante un fallo de tratamiento. También se valoraron como indeterminadas si ante un acontecimiento adverso grave era recomendable esperar un periodo de 5 vidas medias como periodo de lavado para el inicio de un AMC en un paciente que estaba recibiendo otro, o esperar un periodo de al menos 3 vidas medias como periodo de lavado para el cambio de AMC.
Con respecto a la continuidad del tratamiento, se alcanzó consenso superior al 85% en cuanto a la necesidad de esperar un periodo de 3 meses para evaluar su efectividad, en considerar necesario un seguimiento tras la retirada por si hubiese que instaurarlo de nuevo y, en ausencia de una tasa de respuesta del 50%, continuar el tratamiento en caso de disminución significativa de la intensidad del dolor.
Para el rango comprendido entre 66 y 85%, hubo consenso sobre la necesidad de continuar el tratamiento en ausencia de una tasa de respuesta del 50% en caso de disminución significativa de la necesidad de tratamiento sintomático, de que existiesen criterios objetivos de mejoría, de un aumento significativo de la respuesta al tratamiento sintomático y de producirse una mejoría significativa de las escalas de impacto o discapacidad.
Además, también se valoró la retirada temporal del fármaco al cabo de un año en aquellos pacientes con una buena tasa de respuesta y el esperar al menos un periodo equivalente a 5 vidas medias sin recibir ningún AMC antes de buscar un embarazo en el caso de mujeres en edad fértil.
Sin embargo, quedaron indeterminadas las aseveraciones relativas a si se debía suspender temporalmente el AMC en los pacientes con COVID-19 debido a la ausencia de estudios y a valorar la retirada del fármaco al cabo de 3 meses en los pacientes con pérdida de respuesta al AMC.
Entre aquellas relacionadas con el tratamiento en situaciones especiales también se alcanzó el consenso en el rango comprendido entre 66 y 85% para la indicación de no utilizar los AMC en las mujeres embarazadas o en los pacientes con ictus o cardiopatía isquémica, así como el utilizarlos con precaución en los pacientes con factores de riesgo cardiovascular o enfermedad de Raynaud y hacerlo de manera individualizada en los pacientes con enfermedades oncohematológicas activas, enfermedades sistémicas graves o en los pacientes inmunodeprimidos.
Se valoraron como indeterminadas tanto el uso de los AMC en mayores de 65 años por un mayor riesgo cardiovascular asociado a la edad, como en los pacientes con diagnóstico confirmado con inicio de la migraña a partir de los 55 años. También en la recomendación de separar al menos de 5 a 7 días la dosis del AMC de cualquiera de las vacunas frente a la COVID-19.
Módulo de pacientesLas 25 aseveraciones de este módulo se recogen en la tabla 2. Se alcanzó un consenso superior al 85%. En el rango entre 66 y 85% se encontraron las recomendaciones de realizar sesiones grupales, formativas y de intercambio de experiencias, problemas o inquietudes.
Con respecto a las estrategias de educación al paciente, con un grado de consenso superior al 98%, se consideró que una correcta educación e implicación del paciente facilitaría un mejor abordaje de su enfermedad y que su educación debería empezar por el conocimiento de la importancia del estilo de vida y las medidas higiénicas, que se deberían utilizar fármacos profilácticos orales adecuados como medida previa a instaurar un AMC y que el uso de un diario de cefaleas por parte del paciente para la toma de medicamentos y aparición de síntomas sería de utilidad. Por otro lado, en relación con la mejora de la adherencia, destacan la utilidad para el éxito del tratamiento de informar al paciente de los resultados esperados, formarle en las instrucciones de administración e informarle de los posibles efectos adversos y/o complicaciones, así como también proporcionar un contacto profesional ágil y especializado.
Además, se obtuvo un elevado grado de consenso respecto a realizar una visita de seguimiento a los 3 meses desde el inicio del tratamiento, realizar una primera valoración de eficacia y seguridad en la primera visita mediante parámetros objetivos (diario, escalas y calidad de vida), y asegurar el modo correcto de administración del tratamiento, así como revisar la aparición de efectos adversos y su manejo correcto en todas las visitas de seguimiento.
Por último, mencionar el consenso alcanzado sobre la necesidad de incluir que la opinión del paciente en el manejo de la enfermedad facilita la adherencia y, por tanto, el éxito terapéutico.
Módulo de coordinaciónEn este tercer módulo, se incluyeron 24 aseveraciones relacionadas con las estrategias para mejorar el trabajo conjunto, de las cuales 19 alcanzaron un consenso en el acuerdo, una en el desacuerdo y 4 quedaron como indeterminadas.
Se alcanzó un consenso en el acuerdo superior al 85% en la necesidad de mejorar la coordinación entre farmacia hospitalaria y neurología desde un punto de vista clínico, pues repercute positivamente en la atención del paciente, y en la necesidad de definir un procedimiento de actuación consensuado y desarrollar actividades formativas conjuntas. Además, se consensuó que el diseño y elaboración de material informativo debería ser conjunto, y que dicha coordinación, debería implicar a todos los profesionales sanitarios comprometidos en la atención al paciente y que este debe conocer la existencia del equipo multidisciplinar.
También se consensuó que un neurólogo experto en cefaleas fuese el responsable del paciente y quien debe solicitar el tratamiento. Además en el caso de los pacientes complejos, se consensuará entre los servicios de neurología y farmacia hospitalaria, cualquier aspecto relacionado con la indicación, validación, dispensación y administración, así como los criterios de respuesta para no limitar la continuación del tratamiento y el registro en vida real del seguimiento del paciente.
Hubo unanimidad de consenso en la aseveración que la selección del tratamiento no es responsabilidad del farmacéutico.
Quedaron como indeterminadas que el seguimiento del paciente es responsabilidad de farmacia hospitalaria, que la educación sanitaria del paciente debería asumirla el servicio de farmacia hospitalaria o de neurología, y que en el programa formativo del servicio de neurología debería incluirse una rotación específica en farmacia hospitalaria.
DiscusiónEl método Delphi es una metodología de consenso de un panel de expertos, que permite tomar decisiones en situaciones de incertidumbre, cuyas opiniones pueden generar ideas o guías, desarrollar directrices, definir indicadores o interacciones clínicamente significativas12–16.
Aunque el consenso de expertos se considere el nivel más bajo en la pirámide de evidencia, su fortaleza radica tanto en los inputs disponibles para los expertos (revisión sistemática, experimentos, experiencia personal, estudios cualitativos) como en los métodos utilizados para alcanzar el consenso16. El alto grado de consenso alcanzado, superior al 80%, junto con iniciativas como la edición del Libro blanco de la migraña en España o la celebración de la jornada multidisciplinar NEXOS Neurología, muestra un entorno general de sinergia entre neurólogos y farmacéuticos hospitalarios y supone un punto de partida, estableciendo una base práctica para su implantación en la práctica real, el registro de resultados en vida real de los AMC o la integración del farmacéutico en las unidades de cefaleas17,18.
Durante la celebración de dicha jornada, se evidenció que los fármacos preventivos orales disponibles ofrecen una respuesta insuficiente mientras que los AMC anti-CGRP ofrecían una alta selectividad y que es necesario facilitar el acceso a los nuevos fármacos y educar en su administración, favoreciendo la creación de un grupo de trabajo entre ambos servicios para un mejor abordaje de los pacientes con migraña.
En el Manual de práctica clínica en cefaleas, de la Sociedad Española de Neurología (SEN), se indica como opción terapéutica para pacientes con migraña refractaria el uso de fármacos con diferentes mecanismos de acción de manera simultánea19, en línea con nuestro estudio. En concreto, que el uso concomitante de AMC con otros fármacos biológicos debe considerarse de manera individualizada, que no era necesario suspender un tratamiento preventivo antes de iniciar el uso de un AMC cuando presenta una respuesta parcial, que se debería utilizar uno distinto cuando no se haya obtenido respuesta con el primero, pues hasta un 30% de pacientes inicialmente no respondedores pueden obtener un beneficio con el cambio de monoclonal y que debería utilizarse al menos 3 meses para valorar su efectividad, evaluada a través de la disminución de días con migraña, sin tener en cuenta su intensidad, como sí hacen algunos estudios20.
Según el estudio de Briceño-Casado et al., (2020)21, comparando la eficacia y la seguridad de 3 AMC anti-CGRP, indican que podrían considerarse alternativas terapéuticas equivalentes, favoreciendo además la sostenibilidad de los sistemas sanitarios a través de la competencia de precios.
Se acordó valorar la retirada temporal tras un año de tratamiento cuando el paciente alcanza una buena respuesta, haciendo seguimiento por si fuera necesario reinstaurarlo, al igual que en aquellos pacientes que no reduzcan los días de migraña de 30 a 50% a las 12 semanas, siguiendo así las recomendaciones de uso racional de los medicamentos22.
El éxito del tratamiento radica en la adherencia, considerándose de utilidad informar al paciente de los resultados esperados, formar al paciente en las instrucciones de administración y en el manejo de la conservación del AMC, informar al paciente de los posibles efectos adversos y/o complicaciones, proporcionar herramientas para la identificación de la falta de adhesión, proporcionar un contacto profesional ágil y especializado, y utilizar un diario de cefaleas, ya que la educación sanitaria mejora la calidad de vida de los pacientes23. En España, los datos de adherencia de 6 a 12 meses a tratamientos profilácticos para la migraña indican tasas en torno al 30%24. Son también fundamentales las visitas de seguimiento, valorando la eficacia mediante parámetros objetivos y su seguridad, asegurando el modo correcto de administración y revisando la aparición de acontecimientos adversos y su correcto manejo, lo que requiere herramientas para documentar la atención farmacéutica, como es Pharmacists´ Care of Migraineurs Scale (PCMS) propuesta por Skomo ML25,26.
El Libro blanco de la migraña en España incluye, como agente implicado, a la farmacia hospitalaria especialmente en relación con la validación de la prescripción y dispensación de los anticuerpos monoclonales anti CGRP17.
El papel de la Comisión de Farmacia y Terapéutica en la selección de AMC que se incluyen en la Guía farmacoterapéutica podría condicionar la disponibilidad de todos los AMC y la elección del tratamiento, habiendo podido influir en el desacuerdo manifiesto sobre la responsabilidad del farmacéutico hospitalario en la elección final del tratamiento.
Aportación a la literatura científicaLos resultados del consenso para el tratamiento de la prevención de la migraña entre las especialidades de neurología y farmacia hospitalaria, indican un entorno general de sinergia entre neurólogos y farmacéuticos hospitalarios.
A nivel de práctica clínica, los resultados confirman como opción terapéutica para pacientes con migraña refractaria, el uso de fármacos con diferentes mecanismos de acción de forma simultánea, como ocurre en el uso de anticuerpos monoclonales (AMC) con otros fármacos biológicos. Además, los resultados del consenso indican que se debe valorar la retirada temporal tras un año de tratamiento cuando el paciente alcanza una buena respuesta, haciendo seguimiento por si fuera necesario reinstaurarlo.
Referente a la relación médico-paciente, los resultados del consenso indican que una correcta educación sanitaria sobre el manejo y conservación del AMC, así como informar al paciente de los posibles efectos adversos y/o complicaciones, y estableciendo las visitas de seguimiento, mejoran la calidad de vida de los pacientes y la adherencia al tratamiento.
Declaración de autoríaLas conclusiones, hallazgos y comentarios que aparecen reflejados en esta obra son propios de los autores y, por tanto, son responsabilidad única y exclusivamente de los mismos. Se podrían mencionar opciones terapéuticas que podrían contener indicaciones, posologías y/o formas de administración de productos no autorizados actualmente en España. Se recuerda que cualquier fármaco mencionado deberá ser utilizado de acuerdo con la ficha técnica vigente en España.
FinanciaciónNinguna.
AgradecimientosLos autores desean agradecer a Luzán 5 Health Consulting S.A. por su apoyo durante la preparación de este manuscrito.
Conflicto de interesesEste proyecto de investigación ha sido financiado por Lilly S.A.
Miguel Ángel Calleja-Hernández ha recibido honorarios por su participación en actividades de docencia para: Lilly, Novartis y Teva; por asesoramiento para Novartis; por conferencias para Lilly y Novartis; y ha recibido ayudas por proyectos de investigación para Lilly, Novartis y Teva. Ángel Luis Guerrero-Peral ha recibido honorarios por asesoramiento y conferencias para (en orden alfabético) Abbvie-Allergan, Exeltis, Lilly, Novartis, Pfizer y Teva; ha recibido ayudas para proyectos de investigación por parte de Abbvie-Allergan; y ha recibido honorarios por participar en ensayos clínicos para Alder, Amgen, Biohaven, Lilly, Lundbeck, Novartis y Teva. Pablo Irimia-Sieira ha recibido honorarios por su participación en actividades de docencia y consultoría de Abbvie-Allergan, Eli-Lilly, Lundbeck, Novartis, Pfizer y Teva. Icíar Martínez-López ha recibido honorarios por actividades de docencia para Amgen, Boehringer, GSK, Janssen-Cilag, Novartis, Roche y Teva. Sonia Santos-Lasaosa ha recibido honorarios por participar en conferencias para Abbvie-Allergan, Chiesi, Exeltis, Lilly, Novartis y Teva; ha recibido honorarios por su participación en actividades de docencia para Almirall; y ha recibido honorarios por asesoramiento para Abbvie-Allergan, Lundbeck y Pfizer. Maite Sarobe-Carricas no tiene ningún conflicto de interés. José María Serra López-Matencio ha recibido honorarios por impartir conferencias para BristolMyersSquibb y Janssen-Cilag. José Miguel Láinez-Andrés ha recibido honorarios por asesoramiento para Abbvie-Allergan, Bayer, Lilly, Lundbeck, Merck, Novartis, Pfizer y Teva; ha recibido honorarios por conferencias para Abbvie-Allergan, Lilly, Lundbeck, Novartis y Teva; y ha recibido ayudas por partivpar en ensayos clínicos para Abbvie-Allergan, Amgen, Electrocore, Lilly, Lundbeck, Novartis, y Teva.