La tuberculosis supone un problema de salud pública a nivel mundial. La forma ganglionar es la forma más frecuente de tuberculosis extrapulmonar. En 2022, se notificaron en España 3.927 casos de tuberculosis, de los cuales el 27,4% correspondieron a formas extrapulmonares1. La tasa de notificación de casos de tuberculosis pulmonar multirresistente (MDR) y extremadamente resistente (XDR) fue de 0,38 por 100.000 habitantes2.
Descripción del casoUn varón de 51 años, natural de Guinea Ecuatorial, presentaba, como antecedentes familiares de interés, un hermano fallecido a los 18 años por hepatitis y una hija fallecida por accidente de tráfico que padecía una enfermedad autoinmune, tratada con corticosteroides. Entre los antecedentes personales destaca un episodio de tuberculosis miliar por Mycobacterium tuberculosis (M. tuberculosis) complex resistente a isoniazida, en junio de 2009, tratado con terapia tuberculostática empírica con 4 fármacos con buena respuesta.
Desde 2018 sufrió deterioro progresivo de la función renal, con inicio de hemodiálisis (HD) en 2019. Se sospechaba entre una glomerulonefritis crónica no biopsiada y un componente de hiperfiltración por obesidad como motivo del deterioro. Coincidiendo con ello, presentó cuadros febriles y elevación persistente de reactantes de fase aguda sin aislamientos microbiológicos, además de una historia de afectación multisistémica: uveítis, artralgias-artritis, hepatitis autoinmune e imagen de angiotomografía computarizada (angioTAC) de aumento de la densidad en el tronco celíaco, aorta abdominal distal, ilíaca común e hipogástrica izquierdas. Se pensó que podía tratarse de vasculitis de grandes vasos, pero la tomografía por emisión de positrones-tomografía axial computarizada (PET-TAC) descartó alteración metabólica vascular. El estudio inmunológico (inmunoglobulinas, complemento, estudio de enfermedad de fondo (EEF), anticuerpos anticitoplasma de neutrófilos (ANCA) y anticuerpos contra la membrana basal glomerular (anti-MBG) fue negativo y el paciente respondió al tratamiento con colchicina y prednisona.
En 2021 presentó un nuevo episodio de fiebre asociado a artralgias/artritis de tobillo y bultoma latero-cervical. Con la sospecha de poliartritis inflamatoria, se reiniciaron los corticoesteroides y se aumentó la dosis de colchicina. Debido a los antecedentes de tuberculosis, se realizaron hemocultivos, prueba de Mantoux, biopsia ganglionar y tomografía computarizada de cuello, tórax y abdomen. La prueba de Mantoux resultó positiva, la adenectomía mostraba datos sugerentes de afectación tuberculosa y confirmándose finalmente el crecimiento de M. tuberculosis resistente a estreptomicina, isoniacida, rifampicina, etambutol, pirazinamida y etionamida.
Tras conocer de estos resultados, se inició tratamiento con amikacina vía intravenosa (dosis inicial de 10 mg/kg/día), linezolid (LZD) 600 mg al día vía oral y levofloxacino 500 mg vía oral posdiálisis. El paciente se dializaba durante 4,5 horas durante 3 días a la semana, en modalidad HD extendida con dializador Solacea. La amikacina se monitorizó farmacocinéticamente, lo que produjo cambios del régimen a 1.000 mg/3 días a la semana y posteriormente a 250 mg los mismos días. A las 2 semanas se cambió LZD por tedizolid (TZD), por anemia y trombocitopenia, así como por presentar un episodio de crisis tónico-clónica generalizada. No se monitorizó la concentración plasmática de LZD, por lo que se desconoce si los efectos adversos estuvieron relacionados con concentraciones supraterapéuticas del fármaco.
A los 2 meses ingresó por neumonía COVID-19. En dicho ingreso se optimizó el tratamiento tuberculostático, añadiendo clofazimina 200 mg al día vía oral y bedaquilina vía oral (400 mg durante las 2 primeras semanas, permaneciendo posteriormente con 200 mg/48 h tras las sesiones de HD) y suspendiendo la amikacina por mareos e inestabilidad vestibular, asociados al fármaco.
En el TAC de control, realizado en enero de 2022, se objetivó mejoría radiológica de las adenopatías necrosadas laterocervicales, por lo que se decidió completar tratamiento tuberculostático con bedaquilina, clofazimina, levofloxacino y TDZ, hasta completar 6 meses.
Desde el inicio del tratamiento farmacológico presentó control progresivo de la situación inflamatoria, con mejoría del estado general, apetito y anemia. Como efectos secundarios, desarrolló neuropatía periférica a nivel de los miembros inferiores como posible toxicidad por TZD. No se observaron efectos adversos relacionados con la bedaquilina.
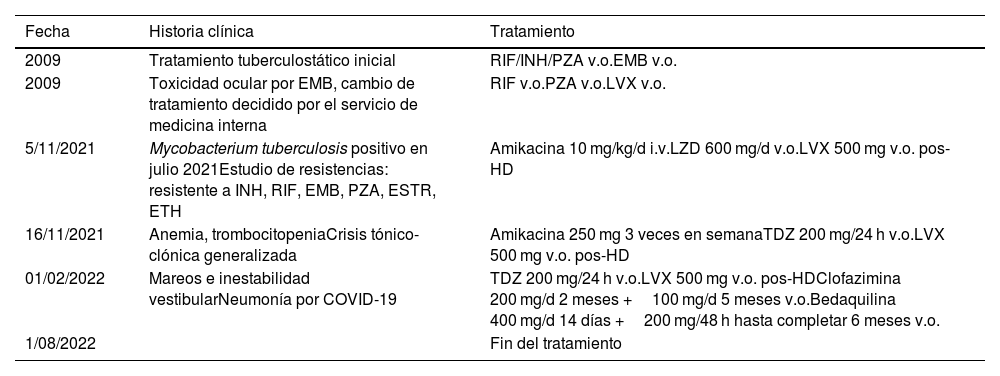
En la tabla 1 se muestra una evolución temporal de los tratamientos recibidos.
Tratamiento recibido desde el momento del diagnóstico
| Fecha | Historia clínica | Tratamiento |
|---|---|---|
| 2009 | Tratamiento tuberculostático inicial | RIF/INH/PZA v.o.EMB v.o. |
| 2009 | Toxicidad ocular por EMB, cambio de tratamiento decidido por el servicio de medicina interna | RIF v.o.PZA v.o.LVX v.o. |
| 5/11/2021 | Mycobacterium tuberculosis positivo en julio 2021Estudio de resistencias: resistente a INH, RIF, EMB, PZA, ESTR, ETH | Amikacina 10 mg/kg/d i.v.LZD 600 mg/d v.o.LVX 500 mg v.o. pos-HD |
| 16/11/2021 | Anemia, trombocitopeniaCrisis tónico-clónica generalizada | Amikacina 250 mg 3 veces en semanaTDZ 200 mg/24 h v.o.LVX 500 mg v.o. pos-HD |
| 01/02/2022 | Mareos e inestabilidad vestibularNeumonía por COVID-19 | TDZ 200 mg/24 h v.o.LVX 500 mg v.o. pos-HDClofazimina 200 mg/d 2 meses +100 mg/d 5 meses v.o.Bedaquilina 400 mg/d 14 días +200 mg/48 h hasta completar 6 meses v.o. |
| 1/08/2022 | Fin del tratamiento |
EMB: etambutol; ESTR: estreptomicina; ETH: etionamida; HD: hemodiálisis; INH: isoniazida; LVX: levofloxacino; LZD: linezolid PZA: pirazinamida; RIF: rifampicina; TDZ: tedizolid; v.i.: vía intravenosa; v.o.: vía oral.
El paciente continuó en seguimiento por parte del servicio de nefrología, acudiendo a las sesiones de HD 3 veces por semana hasta que, finalmente, se produjo el fallecimiento debido a una infección por COVID-19 en junio de 2025.
DiscusiónLa respuesta del huésped frente a M. tuberculosis está mediada por la inmunidad celular, de forma que los grupos poblacionales con compromiso de esta función presentan una mayor susceptibilidad de contraer tuberculosis activa. Dentro de este grupo se encuentran los pacientes en diálisis, ya que se suman factores predisponentes como la edad avanzada, tratamiento inmunosupresor y uremia3. El riesgo incrementado con respecto a la población general es de 6,9 a 52,5 veces.
Es habitual que en este grupo de pacientes la enfermedad se manifieste de una forma inespecífica, lo que puede retrasar el diagnóstico. En cuanto a la presentación, algunos autores afirman que existe una mayor incidencia de tuberculosis miliar en pacientes en HD con respecto a la población general4.
Además del difícil diagnóstico, el aumento de las cepas resistentes a fármacos dificulta el tratamiento. En función de la resistencia a los medicamentos tuberculostáticos, las cepas se clasifican en 3 grupos: MDR-TB, pre-XDR-TB y XDR-TB. Una cepa es MDR-TB cuando es resistente a 2 o más fármacos de primera línea, y pre-XDR-TB cuando es resistente a fármacos de primera línea y fluoroquinolonas o inyectables de segunda línea (capreomicina, estreptomicina u otros aminoglucósidos)5.
El tratamiento de un paciente con tuberculosis MDR debe ser individualizado y estar guiado por los resultados de sensibilidad a los fármacos antituberculosos6. En este caso, se inició un régimen con LZD, levofloxacino y amikacina, asociados a bedaquilina. De los fármacos incluidos, levofloxacino y amikacina requieren ajuste posológico en pacientes que reciben terapia de sustitución renal, mientras que el linezolid no. Bedaquilina no formó parte de la combinación inicial por dificultades en la tramitación de la adquisición como medicamento extranjero. Por la aparición de efectos adversos asociados al tratamiento, este fue optimizado a bedaquilina, TDZ y clofazimina, asociado a levofloxacino durante 6 meses.
LZD es un fármaco efectivo en el tratamiento de la tuberculosis MDR. Sin embargo, la elevada proporción de efectos adversos, principalmente la neuropatía periférica y mielotoxicidad, obligan en ocasiones a reducir la dosis diaria de 600 mg a 300 mg. A menudo esto no resulta suficiente y es necesario suspender el tratamiento7. En nuestro caso, fue sustituido por TDZ, otra oxazolidinona, tras una crisis tónico-clónica que se relacionó con el tratamiento con LZD. TDZ no tiene indicación para el tratamiento de la tuberculosis, pero ha demostrado actividad in vitro frente a cepas de M. tuberculosis8, y se ha reportado algún caso in vivo de pacientes con TB tratados con éxito con TDZ en lugar de LZD9.
Por otro lado, bedaquilina es un fármaco relativamente nuevo de administración oral que actúa inhibiendo la ATP (adenosina 5′-trifosfato) sintasa micobacteriana. Presenta una elevada unión a proteínas plasmáticas (>99%), por lo que es improbable que se elimine en cantidades significativas durante la HD. Además, su excreción urinaria es inferior al 0,001%, por lo que parece innecesario ajustar la dosis en población con técnicas de depuración renal. Sin embargo, los pacientes con insuficiencia renal podrían tener alterada la absorción, distribución o metabolismo secundario del principio activo, por lo que se recomienda un especial control5.
La clofazimina es un fármaco antileproso que, combinado con los anteriores, forma parte de los nuevos regímenes de tratamiento de las formas de MDR-TB. Se administra por vía oral a una dosis de 100 o 200 mg en formas graves. Un estudio en el que 8 pacientes recibieron la dosis de 200 mg antes de la diálisis mostró que la reducción de las concentraciones de fármaco tras la diálisis era insignificante10.
Las principales limitaciones de este caso fueron el retraso del inicio del tratamiento con bedaquilina por problemas burocráticos y la ausencia de niveles plasmáticos de los fármacos empleados.
Para la redacción de este caso clínico, se ha realizado una búsqueda bibliográfica en PubMed, tras la cual no se ha identificado ningún caso de tuberculosis ganglionar MDR en un paciente en HD tratado con la combinación de bedaquilina, TDZ, clofazimina y levofloxacino durante 6 meses, por lo que se trataría del primer caso publicado. Esta combinación resultó eficaz y bien tolerada. Por lo tanto, este régimen podría ser aplicable en pacientes en HD con tuberculosis MDR y un perfil de susceptibilidad a fármacos análogo al que presentaba este paciente.
Consentimiento informadoLos autores declaran que para la publicación de este caso se obtuvo el consentimiento informado del paciente.
Declaración de autoría y originalidadLos autores del trabajo que remiten el envío a la revista Farmacia Hospitalaria declaran que todos han participado de forma sustancial en la elaboración, corrección y aprobación de la versión final del presente manuscrito.
FinanciaciónLos autores declaran que no se recibió ningún tipo de financiación.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
Declaración de contribución de autoría de CRediTPaula Novo González: Writing – review & editing, Writing – original draft. Irene Galindo Marín: Validation, Data curation, Conceptualization. Elena García Benayas: Validation, Supervision, Methodology, Formal analysis, Conceptualization. Carmen Mon Mon: Methodology, Investigation, Formal analysis. Rafael Torres Perea: Validation, Investigation. Sara Hernández Egido: Validation, Investigation, Data curation.