Determinar los factores asociados al fracaso virológico en pacientes con el virus de la inmunodeficiencia humana con tratamiento antirretroviral atendidos en una institución de salud colombiana.
MétodoEstudio transversal, observacional, retrospectivo y analítico en pacientes con el virus de la inmunodeficiencia humana con tratamiento antirretroviral entre 2007-2020. Se recogieron variables sociodemográficas, farmacológicas y clínicas, incluyendo la carga viral, el grado de adherencia y la tasa de reclamación de medicamentos. Para el análisis estadístico se obtuvieron las odds ratio crudas y ajustadas y los intervalos de confianza.
ResultadosDe una población de 5.406 pacientes, la proporción de fracaso virológico fue de 16,7% y en el modelo ajustado se encontró asociación entre el fracaso virológico con el tiempo en el tratamiento mayor a un año, la tasa de posesión de la reclamación inferior al 80%, la no reclamación oportuna por omisión o suspensión, la adherencia inferior al 85%, el recuento de CD4 inferior a 500, niveles de colesterol total mayores de 201 mg/dl, lipoproteína de alta densidad menor de 39 mg/dl y presencia de micosis.
ConclusionesEn nuestra cohorte de pacientes con el virus de la inmunodeficiencia humana, un menor tiempo en tratamiento, un recuento de CD4 menor de 200, una baja tasa de reclamación de los medicamentos, así como la no reclamación oportuna por omisión y suspensión y un menor grado de adherencia son factores que se relacionan con el fracaso virológico.
To determine the factors associated with virologic failure in HIV patients on antiretroviral treatment treated in a Colombian health institution.
MethodThis was a cross-sectional observational retrospective analytical study of HIV patients receiving antiretroviral treatment between 2007-2020. Sociodemographic, pharmacological and clinical variables were collected, including viral load, adherence, and the medication possession ratio. For statistical analysis, crude and adjusted odds ratios and confidence intervals were obtained.
ResultsIn a population of 5,406 patients, the proportion of virologic failure was 16.7%. Moreover, in the adjusted model, an association was found between virologic failure and time on treatment greater than one year, medication possession ratio under 80%, failure to claim medications from the pharmacy due to dose omission or discontinuation, adherence under 85%, CD4 count under 500, total cholesterol levels above 201 mg/dL, high density lipoproteins under 39 mg/dL and presence of mycosis.
ConclusionsIn our cohort of HIV patients, short treatment periods, CD4 counts under 200, a low medication possession ratio, failure to timely claim medications from the pharmacy due to omission or discontinuation, and a lower degree of adherence were factors related to virologic failure.
A largo plazo, el tratamiento antirretroviral (TAR) mejora la supervivencia de los pacientes con VIH. Sin embargo, una proporción significativa de pacientes presentan fracaso virológico tras 6 meses de inicio del TAR, lo que aumenta la morbimortalidad, especialmente en regímenes farmacológicos posteriores a un fallo virológico1,2.
Algunos estudios han asociado el fracaso virológico con factores sociodemográficos como la edad superior a 45 años y la baja escolaridad, factores farmacológicos como la mala adherencia, el tiempo de tratamiento, antecedentes de omisión o suspensión del tratamiento, presencia de reacciones adversas a medicamentos, antecedentes de retraso en la autorización del medicamento, desafiliación al sistema de salud, cambios de tratamiento y factores clínicos como el bajo recuento de CD4, los niveles altos de colesterol total y la presencia de infecciones oportunistas3-6.
La relevancia de algunos de estos factores que explican el fracaso virológico requiere una revisión para ajustarse al contexto local, con el ánimo de diseñar estrategias de intervención desde la gestión institucional del riesgo en salud que mejoren los resultados del tratamiento del paciente con virus de la inmunodeficiencia humana (VIH). El objetivo de esta investigación fue determinar los factores asociados al fracaso virológico en pacientes VIH con tratamiento antirretroviral en una institución de salud de Colombia entre los años 2007 y 2020.
MétodosEstudio transversal, observacional, retrospectivo y analítico, donde se exploraron los factores asociados al fracaso virológico en pacientes VIH con TAR. La población de estudio fue conformada por pacientes con diagnóstico de VIH y naïve en el uso de TAR, atendidos en una institución de salud de Colombia entre 2007 y 2020, que contaran con información de carga viral 6 meses después del inicio del TAR. Se excluyeron los pacientes que no tuvieran disponible la información completa de las variables clínicas, farmacológicas y sociodemográficas evaluadas (pérdida de información superior al 20%) y pacientes con menos de 6 meses de tratamiento para evitar tener falsos positivos (tiempo suficiente para garantizar disminución de la carga viral).
El desenlace evaluado fue fracaso virológico (más de 50 copias del virus/ml en sangre), el cual se midió teniendo en cuenta la última carga viral del paciente durante el periodo evaluado. Además, se identificaron los factores sociodemográficos (edad, sexo, estrato socioeconómico, estado civil, residencia, ocupación, afiliación en salud, escolaridad, acompañante), farmacológicos (grupo farmacológico, tiempo en tratamiento, adherencia al tratamiento, tasa de reclamación de medicamentos en farmacia, cambio de esquema TAR durante el tratamiento) y clínicos (recuento de CD4, infecciones oportunistas y riesgo cardiovascular).
Se definió que los pacientes presentaban riesgo cardiovascular cuando se identificaron niveles de colesterol total o lipoproteínas de alta densidad (HDL) por fuera de metas (≥ 201 mg/dl o ≤ 39 mg/dl, respectivamente). Las infecciones oportunistas se identificaron a partir del historial de exámenes de laboratorio y la historia clínica del paciente.
Para la medición del grado de adherencia se tuvo en cuenta la información recolectada por el farmacéutico durante la consulta de seguimiento farmacoterapéutico mediante el Simplified Medication Adherence Questionnaire (SMAQ)7. La tasa de reclamación de medicamentos en farmacia o tasa de posesión de la medicación se evaluó teniendo en cuenta los registros de dispensaciones mensuales del servicio farmacéutico y se calculó el porcentaje basado en el número de dispensaciones que debería tener el paciente acorde con el tiempo que llevaba en tratamiento.
Las variables clínicas y farmacológicas se tomaron al momento de identificar el desenlace evaluado o en la última medición que se identificó de cada paciente.
Se estructuró una base de datos en Microsoft Excel© con la información recopilada del software de historia clínica y seguimiento farmacoterapéutico y los datos de dispensación de medicamentos de la institución. Además, se recopiló información de pruebas de laboratorio suministrada por el asegurador. En el estudio se controló el sesgo de selección, incluyendo el 100% de los registros disponibles y los sesgos de información mediante aplicación de criterios de exclusión. Además, los potenciales confusores fueron controlados mediante la aplicación de modelos ajustados (análisis multivariado).
El análisis de los datos se realizó mediante análisis univariantes, biva-riantes y multivariantes, usando R Studio (software de libre uso). Primero, se calcularon medidas de frecuencia para las variables cualitativas y para las variables cuantitativas, se probó normalidad y se calcularon medidas de resumen; estos resultados se presentaron en cuadros, texto y gráficas. En el análisis bivariado, se realizó prueba chi cuadrado y regresión logística binaria simple para calcular las odds ratio crudas (ORc) y sus intervalos de confianza al 95% y, finalmente, se realizó una regresión logística binaria múltiple con fines explicativos para calcular OR ajustadas (ORa), con las variables en las que encontró diferencias estadísticamente significativas.
Según el artículo 11 de la resolución 008430 de 1993 del Ministerio de Salud de Colombia, esta investigación se consideró como “sin riesgos”. Se trabajó con información existente en la base de datos de la institución de salud +helPharma, no se realizó ninguna intervención que pusiera en riesgo la salud de los pacientes. Fueron suprimidos datos de identificación, garantizando de esta manera la confidencialidad y privacidad de la información. Se contó con el aval científico de la entidad aseguradora.
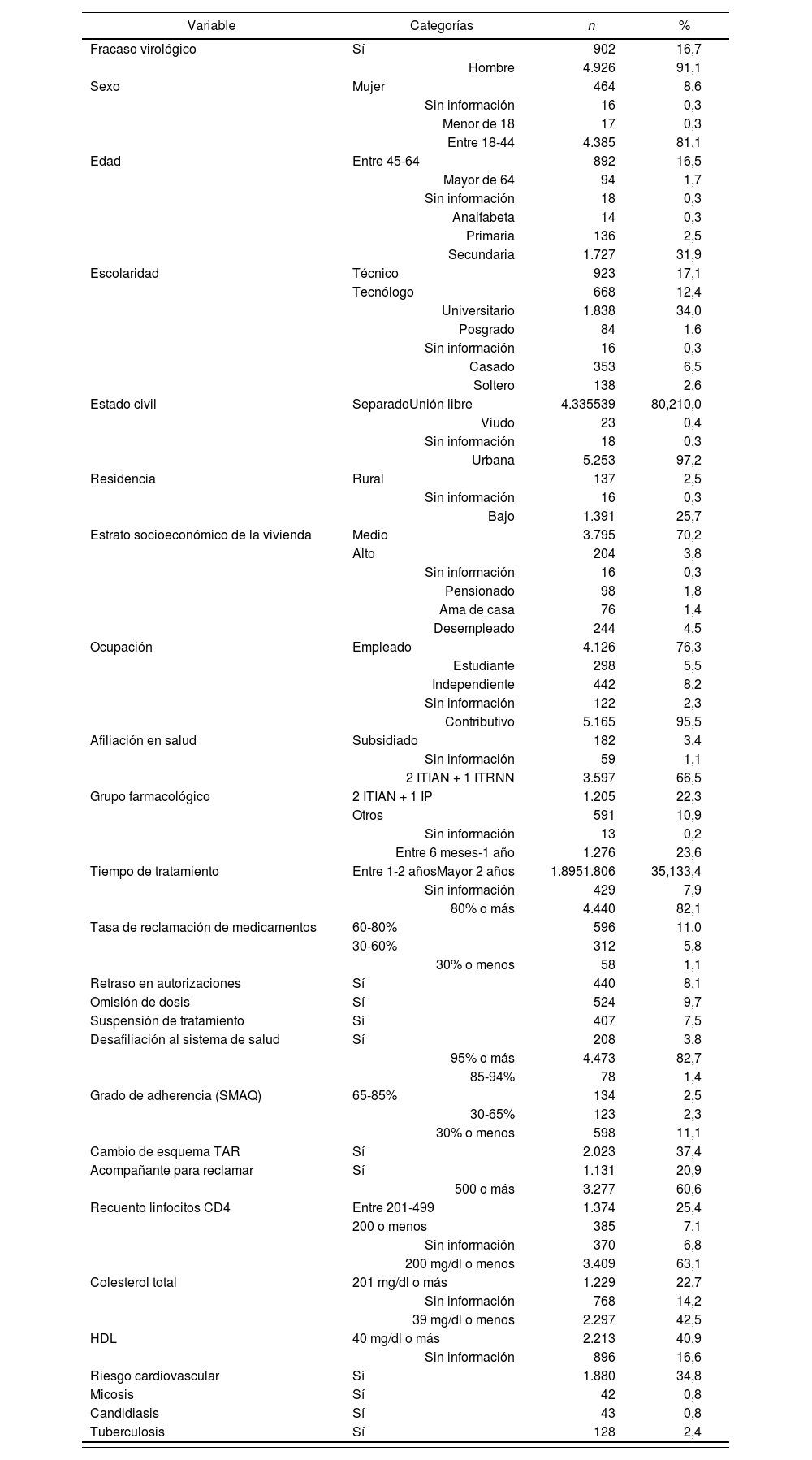
ResultadosSe evaluaron 5.838 registros de pacientes con VIH en TAR, de los cuales se excluyeron 432 pacientes y quedaron un total de 5.406 de pacientes. La proporción de fracaso virológico fue del 16,7%. El 91,1% de los pacientes eran hombres, el 81,1% tenía entre 18 y 44 años, el 34,0% eran universitarios, el 83,2% se encontraban sin pareja, el 97,2% residían en zona urbana, el 95,9% residían en viviendas de estratos socioeconómicos bajo y medio, el 76,3% eran empleados y el 95,5% pertenecían al régimen de afiliación al sistema de salud contributivo.
Con respecto a las características farmacológicas, se halló que el 66,5% tenían un esquema terapéutico con dos inhibidores de la transcriptasa inversa análogos a nucleósido (ITIAN) más un inhibidor de la transcriptasa inversa no nucleósido (ITRNN), el 33,4% presentaban más de 2 años en tratamiento, el 82,1% presentó una reclamación de medicamentos superior al 80% y se presentaron reclamaciones inoportunas de los medicamentos debido a retrasos en las autorizaciones (8,1%), omisión de dosis (9,7%), suspensión de tratamiento (7,5%) y desafiliación al sistema de salud (3,8%). Relacionado con la adherencia, se encontró que el 82,7% era adherente al tratamiento (≥ 95%) y el 11,0% se clasificó como no adherente o tuvo una adherencia inferior al 30%. Además, 4 de cada 10 pacientes presentaron cambio de esquema TAR durante su tratamiento y 2 de cada 10 pacientes van acompañados a su cita médica.
En cuanto a las variables clínicas, se observó que el 60,6% tenían un recuento de linfocitos CD4 ≥ 500, tal y como se indica en la tabla 1.
Características sociodemográficas y clínicas de los pacientes con tratamiento antirretroviral
| Variable | Categorías | n | % |
|---|---|---|---|
| Fracaso virológico | Sí | 902 | 16,7 |
| Hombre | 4.926 | 91,1 | |
| Sexo | Mujer | 464 | 8,6 |
| Sin información | 16 | 0,3 | |
| Menor de 18 | 17 | 0,3 | |
| Entre 18-44 | 4.385 | 81,1 | |
| Edad | Entre 45-64 | 892 | 16,5 |
| Mayor de 64 | 94 | 1,7 | |
| Sin información | 18 | 0,3 | |
| Analfabeta | 14 | 0,3 | |
| Primaria | 136 | 2,5 | |
| Secundaria | 1.727 | 31,9 | |
| Escolaridad | Técnico | 923 | 17,1 |
| Tecnólogo | 668 | 12,4 | |
| Universitario | 1.838 | 34,0 | |
| Posgrado | 84 | 1,6 | |
| Sin información | 16 | 0,3 | |
| Casado | 353 | 6,5 | |
| Soltero | 138 | 2,6 | |
| Estado civil | SeparadoUnión libre | 4.335539 | 80,210,0 |
| Viudo | 23 | 0,4 | |
| Sin información | 18 | 0,3 | |
| Urbana | 5.253 | 97,2 | |
| Residencia | Rural | 137 | 2,5 |
| Sin información | 16 | 0,3 | |
| Bajo | 1.391 | 25,7 | |
| Estrato socioeconómico de la vivienda | Medio | 3.795 | 70,2 |
| Alto | 204 | 3,8 | |
| Sin información | 16 | 0,3 | |
| Pensionado | 98 | 1,8 | |
| Ama de casa | 76 | 1,4 | |
| Desempleado | 244 | 4,5 | |
| Ocupación | Empleado | 4.126 | 76,3 |
| Estudiante | 298 | 5,5 | |
| Independiente | 442 | 8,2 | |
| Sin información | 122 | 2,3 | |
| Contributivo | 5.165 | 95,5 | |
| Afiliación en salud | Subsidiado | 182 | 3,4 |
| Sin información | 59 | 1,1 | |
| 2 ITIAN + 1 ITRNN | 3.597 | 66,5 | |
| Grupo farmacológico | 2 ITIAN + 1 IP | 1.205 | 22,3 |
| Otros | 591 | 10,9 | |
| Sin información | 13 | 0,2 | |
| Entre 6 meses-1 año | 1.276 | 23,6 | |
| Tiempo de tratamiento | Entre 1-2 añosMayor 2 años | 1.8951.806 | 35,133,4 |
| Sin información | 429 | 7,9 | |
| 80% o más | 4.440 | 82,1 | |
| Tasa de reclamación de medicamentos | 60-80% | 596 | 11,0 |
| 30-60% | 312 | 5,8 | |
| 30% o menos | 58 | 1,1 | |
| Retraso en autorizaciones | Sí | 440 | 8,1 |
| Omisión de dosis | Sí | 524 | 9,7 |
| Suspensión de tratamiento | Sí | 407 | 7,5 |
| Desafiliación al sistema de salud | Sí | 208 | 3,8 |
| 95% o más | 4.473 | 82,7 | |
| 85-94% | 78 | 1,4 | |
| Grado de adherencia (SMAQ) | 65-85% | 134 | 2,5 |
| 30-65% | 123 | 2,3 | |
| 30% o menos | 598 | 11,1 | |
| Cambio de esquema TAR | Sí | 2.023 | 37,4 |
| Acompañante para reclamar | Sí | 1.131 | 20,9 |
| 500 o más | 3.277 | 60,6 | |
| Recuento linfocitos CD4 | Entre 201-499 | 1.374 | 25,4 |
| 200 o menos | 385 | 7,1 | |
| Sin información | 370 | 6,8 | |
| 200 mg/dl o menos | 3.409 | 63,1 | |
| Colesterol total | 201 mg/dl o más | 1.229 | 22,7 |
| Sin información | 768 | 14,2 | |
| 39 mg/dl o menos | 2.297 | 42,5 | |
| HDL | 40 mg/dl o más | 2.213 | 40,9 |
| Sin información | 896 | 16,6 | |
| Riesgo cardiovascular | Sí | 1.880 | 34,8 |
| Micosis | Sí | 42 | 0,8 |
| Candidiasis | Sí | 43 | 0,8 |
| Tuberculosis | Sí | 128 | 2,4 |
HDL: lipoproteínas de alta densidad; IP: inhibidores de la proteasa; ITIAN: inhibidores de la transcriptasa reversa análogos a nucleósidos; ITRNN: inhibidores de la transcriptasa reversa no nucleósidos; SMAQ: Simplified Medication Adherence Questionnaire; TAR: tratamiento antirretroviral.
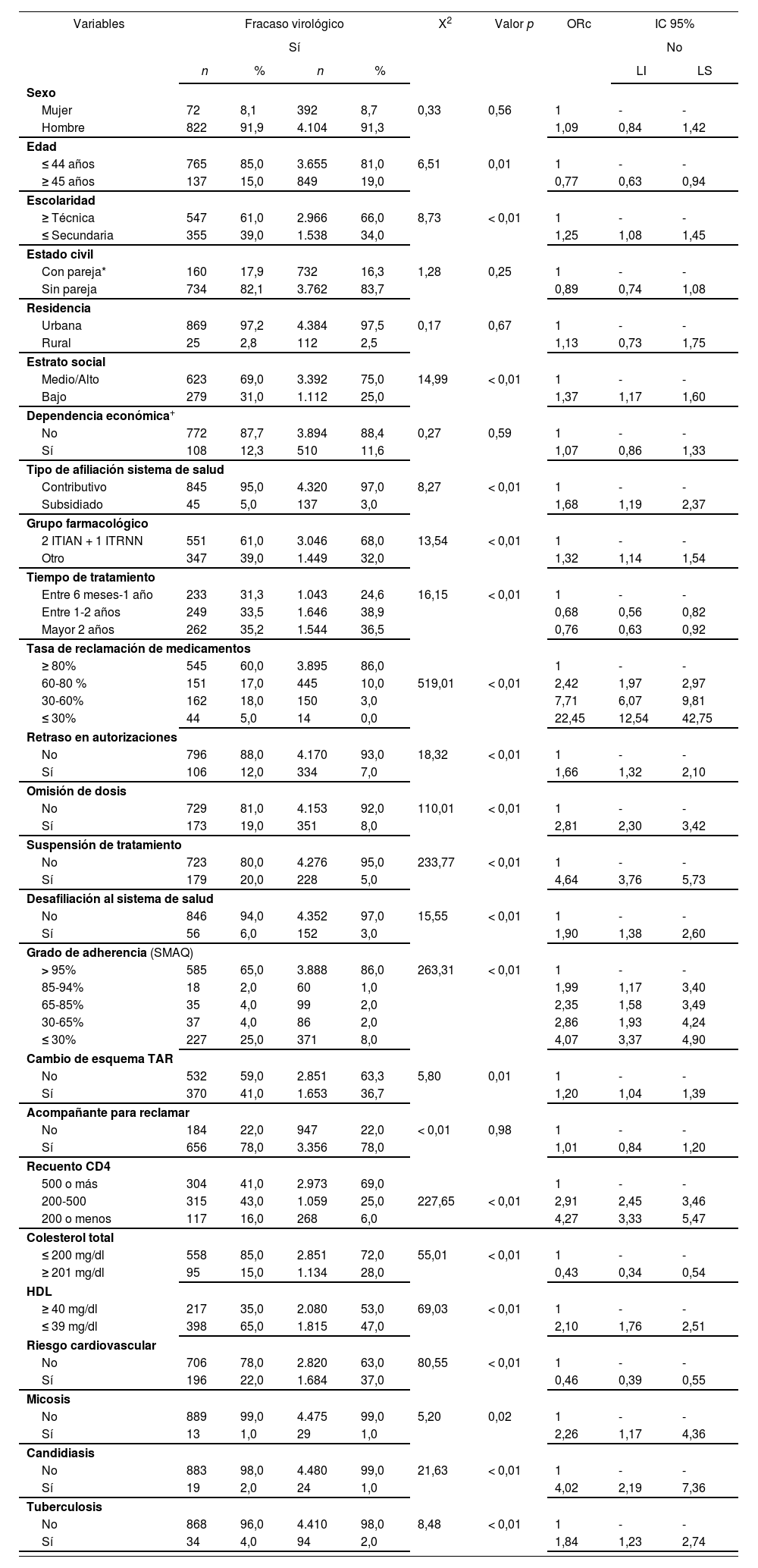
Al explorar la asociación cruda entre los factores demográficos, farmacológicos y clínicos con el fracaso, se halló que tener una escolaridad menor o igual a secundaria, estrato social bajo, afiliación al régimen subsidiado en salud, grupo farmacológico diferente a dos ITIAN + un ITRNN, tasa de reclamación ≤ 80%, no reclamación oportuna (retraso autorizaciones, omisión dosis, suspensión del tratamiento, desafiliación), adherencia ≤ 85%, cambio de esquema TAR, recuento de CD4 < 500, HDL ≤ 39 mg/dl y presencia de micosis, candidiasis y tuberculosis, explican de manera significativa el desenlace. Por su parte, tener ≥ 45 años, estar sin pareja, estar por más de un año en tratamiento, presentar niveles de colesterol ≥ 201 mg/dl y tener riesgo cardiovascular se comportan como factores protectores (Tabla 2).
Factores asociados al fracaso virológico en pacientes VIH con tratamiento antirretroviral
| Variables | Fracaso virológico | X2 | Valor p | ORc | IC 95% | ||||
|---|---|---|---|---|---|---|---|---|---|
| Sí | No | ||||||||
| n | % | n | % | LI | LS | ||||
| Sexo | |||||||||
| Mujer | 72 | 8,1 | 392 | 8,7 | 0,33 | 0,56 | 1 | - | - |
| Hombre | 822 | 91,9 | 4.104 | 91,3 | 1,09 | 0,84 | 1,42 | ||
| Edad | |||||||||
| ≤ 44 años | 765 | 85,0 | 3.655 | 81,0 | 6,51 | 0,01 | 1 | - | - |
| ≥ 45 años | 137 | 15,0 | 849 | 19,0 | 0,77 | 0,63 | 0,94 | ||
| Escolaridad | |||||||||
| ≥ Técnica | 547 | 61,0 | 2.966 | 66,0 | 8,73 | < 0,01 | 1 | - | - |
| ≤ Secundaria | 355 | 39,0 | 1.538 | 34,0 | 1,25 | 1,08 | 1,45 | ||
| Estado civil | |||||||||
| Con pareja* | 160 | 17,9 | 732 | 16,3 | 1,28 | 0,25 | 1 | - | - |
| Sin pareja | 734 | 82,1 | 3.762 | 83,7 | 0,89 | 0,74 | 1,08 | ||
| Residencia | |||||||||
| Urbana | 869 | 97,2 | 4.384 | 97,5 | 0,17 | 0,67 | 1 | - | - |
| Rural | 25 | 2,8 | 112 | 2,5 | 1,13 | 0,73 | 1,75 | ||
| Estrato social | |||||||||
| Medio/Alto | 623 | 69,0 | 3.392 | 75,0 | 14,99 | < 0,01 | 1 | - | - |
| Bajo | 279 | 31,0 | 1.112 | 25,0 | 1,37 | 1,17 | 1,60 | ||
| Dependencia económica+ | |||||||||
| No | 772 | 87,7 | 3.894 | 88,4 | 0,27 | 0,59 | 1 | - | - |
| Sí | 108 | 12,3 | 510 | 11,6 | 1,07 | 0,86 | 1,33 | ||
| Tipo de afiliación sistema de salud | |||||||||
| Contributivo | 845 | 95,0 | 4.320 | 97,0 | 8,27 | < 0,01 | 1 | - | - |
| Subsidiado | 45 | 5,0 | 137 | 3,0 | 1,68 | 1,19 | 2,37 | ||
| Grupo farmacológico | |||||||||
| 2 ITIAN + 1 ITRNN | 551 | 61,0 | 3.046 | 68,0 | 13,54 | < 0,01 | 1 | - | - |
| Otro | 347 | 39,0 | 1.449 | 32,0 | 1,32 | 1,14 | 1,54 | ||
| Tiempo de tratamiento | |||||||||
| Entre 6 meses-1 año | 233 | 31,3 | 1.043 | 24,6 | 16,15 | < 0,01 | 1 | - | - |
| Entre 1-2 años | 249 | 33,5 | 1.646 | 38,9 | 0,68 | 0,56 | 0,82 | ||
| Mayor 2 años | 262 | 35,2 | 1.544 | 36,5 | 0,76 | 0,63 | 0,92 | ||
| Tasa de reclamación de medicamentos | |||||||||
| ≥ 80% | 545 | 60,0 | 3.895 | 86,0 | 1 | - | - | ||
| 60-80 % | 151 | 17,0 | 445 | 10,0 | 519,01 | < 0,01 | 2,42 | 1,97 | 2,97 |
| 30-60% | 162 | 18,0 | 150 | 3,0 | 7,71 | 6,07 | 9,81 | ||
| ≤ 30% | 44 | 5,0 | 14 | 0,0 | 22,45 | 12,54 | 42,75 | ||
| Retraso en autorizaciones | |||||||||
| No | 796 | 88,0 | 4.170 | 93,0 | 18,32 | < 0,01 | 1 | - | - |
| Sí | 106 | 12,0 | 334 | 7,0 | 1,66 | 1,32 | 2,10 | ||
| Omisión de dosis | |||||||||
| No | 729 | 81,0 | 4.153 | 92,0 | 110,01 | < 0,01 | 1 | - | - |
| Sí | 173 | 19,0 | 351 | 8,0 | 2,81 | 2,30 | 3,42 | ||
| Suspensión de tratamiento | |||||||||
| No | 723 | 80,0 | 4.276 | 95,0 | 233,77 | < 0,01 | 1 | - | - |
| Sí | 179 | 20,0 | 228 | 5,0 | 4,64 | 3,76 | 5,73 | ||
| Desafiliación al sistema de salud | |||||||||
| No | 846 | 94,0 | 4.352 | 97,0 | 15,55 | < 0,01 | 1 | - | - |
| Sí | 56 | 6,0 | 152 | 3,0 | 1,90 | 1,38 | 2,60 | ||
| Grado de adherencia (SMAQ) | |||||||||
| > 95% | 585 | 65,0 | 3.888 | 86,0 | 263,31 | < 0,01 | 1 | - | - |
| 85-94% | 18 | 2,0 | 60 | 1,0 | 1,99 | 1,17 | 3,40 | ||
| 65-85% | 35 | 4,0 | 99 | 2,0 | 2,35 | 1,58 | 3,49 | ||
| 30-65% | 37 | 4,0 | 86 | 2,0 | 2,86 | 1,93 | 4,24 | ||
| ≤ 30% | 227 | 25,0 | 371 | 8,0 | 4,07 | 3,37 | 4,90 | ||
| Cambio de esquema TAR | |||||||||
| No | 532 | 59,0 | 2.851 | 63,3 | 5,80 | 0,01 | 1 | - | - |
| Sí | 370 | 41,0 | 1.653 | 36,7 | 1,20 | 1,04 | 1,39 | ||
| Acompañante para reclamar | |||||||||
| No | 184 | 22,0 | 947 | 22,0 | < 0,01 | 0,98 | 1 | - | - |
| Sí | 656 | 78,0 | 3.356 | 78,0 | 1,01 | 0,84 | 1,20 | ||
| Recuento CD4 | |||||||||
| 500 o más | 304 | 41,0 | 2.973 | 69,0 | 1 | - | - | ||
| 200-500 | 315 | 43,0 | 1.059 | 25,0 | 227,65 | < 0,01 | 2,91 | 2,45 | 3,46 |
| 200 o menos | 117 | 16,0 | 268 | 6,0 | 4,27 | 3,33 | 5,47 | ||
| Colesterol total | |||||||||
| ≤ 200 mg/dl | 558 | 85,0 | 2.851 | 72,0 | 55,01 | < 0,01 | 1 | - | - |
| ≥ 201 mg/dl | 95 | 15,0 | 1.134 | 28,0 | 0,43 | 0,34 | 0,54 | ||
| HDL | |||||||||
| ≥ 40 mg/dl | 217 | 35,0 | 2.080 | 53,0 | 69,03 | < 0,01 | 1 | - | - |
| ≤ 39 mg/dl | 398 | 65,0 | 1.815 | 47,0 | 2,10 | 1,76 | 2,51 | ||
| Riesgo cardiovascular | |||||||||
| No | 706 | 78,0 | 2.820 | 63,0 | 80,55 | < 0,01 | 1 | - | - |
| Sí | 196 | 22,0 | 1.684 | 37,0 | 0,46 | 0,39 | 0,55 | ||
| Micosis | |||||||||
| No | 889 | 99,0 | 4.475 | 99,0 | 5,20 | 0,02 | 1 | - | - |
| Sí | 13 | 1,0 | 29 | 1,0 | 2,26 | 1,17 | 4,36 | ||
| Candidiasis | |||||||||
| No | 883 | 98,0 | 4.480 | 99,0 | 21,63 | < 0,01 | 1 | - | - |
| Sí | 19 | 2,0 | 24 | 1,0 | 4,02 | 2,19 | 7,36 | ||
| Tuberculosis | |||||||||
| No | 868 | 96,0 | 4.410 | 98,0 | 8,48 | < 0,01 | 1 | - | - |
| Sí | 34 | 4,0 | 94 | 2,0 | 1,84 | 1,23 | 2,74 | ||
X2: chi cuadrado; IC: intervalo de confianza, ITIAN: inhibidores de la transcriptasa reversa análogos a nucleósidos; ITRNN: inhibidores de la transcriptasa reversa no nucleósidos; LI: límite inferior, LS: límite superior; ORc: odds ratio cruda; SMAQ: Simplified Medication Adherence Questionnaire; TAR: tratamiento antirretroviral.
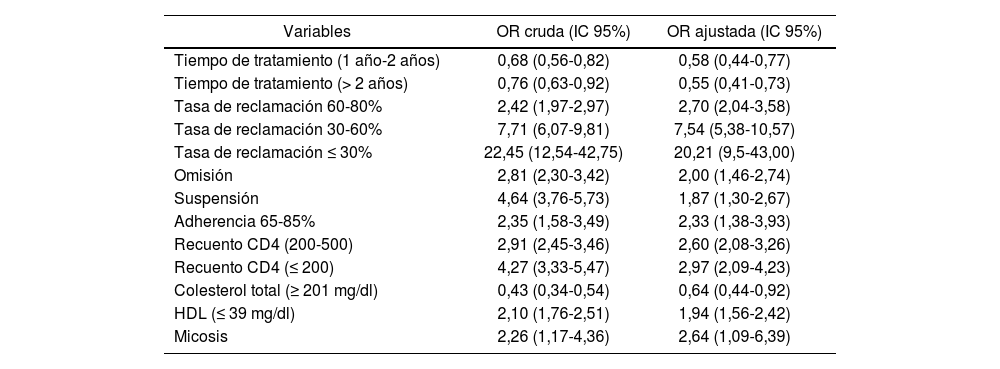
En el modelo ajustado se observó que los factores que explicaban el fracaso virológico fueron el tiempo en el tratamiento mayor a un año, la tasa de reclamación de medicamentos en farmacia inferior al 80%, la no reclamación oportuna por omisión o suspensión, la adherencia inferior al 85%, el recuento de CD4 < 500, niveles de colesterol total ≥ 201 mg/dL, HDL ≤ 39 mg/dl y presencia de micosis (Tabla 3).
Factores que explican el fracaso virológico en pacientes VIH con tratamiento antirretroviral
| Variables | OR cruda (IC 95%) | OR ajustada (IC 95%) |
|---|---|---|
| Tiempo de tratamiento (1 año-2 años) | 0,68 (0,56-0,82) | 0,58 (0,44-0,77) |
| Tiempo de tratamiento (> 2 años) | 0,76 (0,63-0,92) | 0,55 (0,41-0,73) |
| Tasa de reclamación 60-80% | 2,42 (1,97-2,97) | 2,70 (2,04-3,58) |
| Tasa de reclamación 30-60% | 7,71 (6,07-9,81) | 7,54 (5,38-10,57) |
| Tasa de reclamación ≤ 30% | 22,45 (12,54-42,75) | 20,21 (9,5-43,00) |
| Omisión | 2,81 (2,30-3,42) | 2,00 (1,46-2,74) |
| Suspensión | 4,64 (3,76-5,73) | 1,87 (1,30-2,67) |
| Adherencia 65-85% | 2,35 (1,58-3,49) | 2,33 (1,38-3,93) |
| Recuento CD4 (200-500) | 2,91 (2,45-3,46) | 2,60 (2,08-3,26) |
| Recuento CD4 (≤ 200) | 4,27 (3,33-5,47) | 2,97 (2,09-4,23) |
| Colesterol total (≥ 201 mg/dl) | 0,43 (0,34-0,54) | 0,64 (0,44-0,92) |
| HDL (≤ 39 mg/dl) | 2,10 (1,76-2,51) | 1,94 (1,56-2,42) |
| Micosis | 2,26 (1,17-4,36) | 2,64 (1,09-6,39) |
HDL: lipoproteínas de alta densidad; IC: intervalo de confianza; OR: odds ratio.
La tasa de fracaso virológico del estudio fue del 16,7%, la cual es superior a los hallazgos de investigaciones realizadas en Italia (8,4%)8, Filipinas (10,3%)9 y Europa (9,8%)10; esta diferencia puede ser explicada por las particularidades de la composición y la dinámica intrínseca entre las poblaciones. Sin embargo, también se declara que estos resultados fueron inferiores a lo publicado en Suiza (35%)11 y China (35%)12.
Se ha demostrado que a medida que se reduce el grado de adherencia aumenta la probabilidad de presentar fracaso virológico, resultados similares a estudios realizados en otras regiones como Camerún, Etiopía y Uganda5,13,14, hecho que demuestra que es mejor resolver el problema de adherencia y sus causas antes de cambiar el esquema TAR, dado que una baja adherencia al tratamiento es asociada a una baja concentración de los antirretrovirales en suero e implica el riesgo de no alcanzar las concentraciones plasmáticas adecuadas para detener la producción viral.
Con respecto a la asociación inversa entre el recuento de linfocitos CD4 y la carga viral, los resultados del estudio son similares a la evidencia científica notificada en diferentes estudios, como el de De Luca et al.15, quienes recuperaron datos de 26 cohortes de adultos en ocho países que comenzaron maraviroc en 2005-2016, y el de Gunda et al.3 en Tanzania durante 2017 y 2018, donde el estado inmunológico de los pacientes disminuyó mientras que la replicación viral aumentó.
El tiempo de tratamiento juega un papel importante en la asociación con el fracaso virológico, donde se ha observado que a mayor tiempo en el tratamiento se reduce la probabilidad de fracaso virológico, resultados similares a este estudio y como lo demuestran otros estudios16-18. Igualmente, algunos estudios demuestran que la aparición de eventos adversos de medicamentos, los cambios de esquemas terapéuticos, la interrupción frecuente del TAR, los antecedentes de omisión y antecedentes de suspensión de tratamiento en pacientes con VIH se asoció con fallo virológico6,19-21, dado que puede presentar una acumulación de varias mutaciones que confieren resistencia del VIH a los antirretrovirales22.
Si bien el uso a largo plazo de la TAR reduce la morbilidad y mortalidad de los pacientes, Míguez et al.23 documentan los efectos inversos sobre la salud cardiovascular de los pacientes a causa del tratamiento TAR, ya que estos se han relacionado con efectos adversos asociados al aumento de los niveles de colesterol. Estos resultados fueron similares en nuestro estudio con los pacientes que presentan niveles de colesterol total ≥ 201 mg/dl, y de manera similar a lo reportado por Padmapriyadarsini et al.24, se observó la relación entre HDL (≤ 39 mg/dl) y el fracaso viral. En este sentido, es coherente afirmar que los pacientes que presentan niveles altos de colesterol son pacientes adherentes a la terapia TAR y, por ende, tienen menos probabilidad de presentar fracaso terapéutico. Por ello, es importante reforzar el asesoramiento sobre el estilo de vida en cuanto a dieta y ejercicio en los pacientes con TAR y evaluar la posibilidad de inicio de tratamiento hipolipemiante.
Con frecuencia se ha demostrado que la edad es un factor que explica o predice el fallo virológico de los pacientes VIH. Acorde con esto, en este estudio identificamos en el modelo ajustado que los pacientes mayores de 45 años redujeron en un 10% la probabilidad de presentar fracaso virológico, lo cual puede estar relacionado con la madurez y estabilidad emocional25-27.
Es claro que los pacientes con inmunidad comprometida son más vulnerables a diferentes infecciones oportunistas que sostienen el círculo vicioso de inmunidad y replicación viral28. Este estudio demostró que la presencia de micosis y candidiasis aumentaron la probabilidad de fracaso virológico.
Otros factores asociados con fracaso virológico son los antecedentes de retraso en la autorización del medicamento y desafiliación en salud. Algunos estudios similares desarrollados en el contexto colombiano, como el de Machado et al.29, identificaron que un 20,9% de los pacientes estudiados no tomaban el medicamento debido a que se encontraban desafiliados al sistema de salud por pérdida del empleo. En este sentido, aunque la adherencia se ha demostrado como un factor fundamental para garantizar el éxito terapéutico, existen factores sociales y del sistema de salud que pueden influir en esta y generar una alta probabilidad de fracaso terapéutico29,30, por ello es necesario buscar estrategias que permitan garantizar que todos los pacientes reciban su tratamiento de manera continua y oportuna31.
La principal fortaleza del estudio fue la selección completa de los pacientes, pues se trabajó con el censo total de los registros de la cohorte de pacientes VIH 2007 a 2020, excluyendo los pacientes que lleven menos de 6 meses con el tratamiento, situación que controla en mayor medida los sesgos de selección en el estudio. Sin embargo, se deben leer con especial cuidado los resultados, pues el diseño transversal del estudio limita la inferencia causal, por ello, estos resultados son aplicables solo a la población en la cual se realizó el estudio. Además, el hecho de tener información secundaria limita la inclusión de otros confusores importantes para comprender los factores no etiológicos del fracaso viral. Finalmente, comprender los factores asociados con el fracaso virológico permite identificar las barreras al tratamiento de los pacientes VIH para favorecer la gestión del riesgo en salud desde lo individual y comunitario.
Se concluye que el uso inadecuado del medicamento, principalmente la falta de adherencia y la reclamación oportuna de los medicamentos, el grado de inmunosupresión, los pacientes en fase de inicio del tratamiento o tener un perfil lipídico alterado aun con tratamiento farmacológico, son factores que se relacionan con la aparición de fracaso virológico en pacientes con VIH. Identificar estos factores permite la planificación de estrategias encaminadas en la importancia del uso adecuado del TAR, la adherencia y la reclamación oportuna del TAR, principalmente en pacientes que inician su tratamiento. Además, es preciso establecer un seguimiento estrecho de aquellos pacientes con mayor riesgo de presentar fracaso terapéutico, teniendo en cuenta los factores clínicos, farmacológicos y sociales que pueden afectar a la adherencia.
FinanciaciónSin financiación.
Conflicto de interésSin conflictos de interés.
Aportación a la literatura científicaEs una investigación que aporta conocimiento sobre los factores sociodemográficos, clínicos y farmacológicos asociados con el fracaso virológico en pacientes con virus de la inmunodeficiencia humana/sida. En esta investigación se trabajó con una importante muestra de pacientes, todos con tratamiento antirretroviral activo, situación que sin duda permitirá concluir la relevancia que tienen los factores identificados.
Los resultados de esta investigación permiten la planificación de estrategias centradas en la importancia del uso adecuado del tratamiento antirretroviral, la adherencia y la tasa de reclamación de medicamentos en farmacia, principalmente en pacientes que inician su tratamiento, y establecer estrategias para un seguimiento estrecho a aquellos pacientes con mayor posibilidad de presentar fracaso terapéutico.
Early Access date (08/19/2022).