revisar y analizar la literatura disponible sobre la administración de noradrenalina (NA) por vía periférica con el fin de aportar recomendaciones que garanticen el correcto uso y la seguridad del paciente.
Métodorevisión sistemática en las bases de datos PubMed, ISI Web of Science, SCOPUS y Science Direct, utilizándose los siguientes términos de búsqueda: («Noradrenaline» [Mesh]) AND («Norepinephrine» [Mesh]) AND («Vasopressors» [Mesh]) AND («Peripheral infussions» [Mesh]) OR («Extravasations» [Mesh]). Se identificaron 1.040 artículos. Se excluyeron estudios en animales y estudios escritos en idiomas diferentes al inglés. Finalmente se incluyeron 83 artículos.
Resultadosla administración de NA se puede realizar por vía periférica. Se debe tener en cuenta el riesgo que existe de extravasación, siendo la fentolamina la primera línea farmacológica de tratamiento. También se ha relacionado con la aparición de tromboflebitis, celulitis, necrosis tisular, isquemia de miembros y gangrena, aunque su incidencia parece ser baja. El uso de NA periférica en niños parece llevarse a cabo sin complicaciones evidentes. Se sugiere el empleo de unas concentraciones estándares para reducir el riesgo de errores. Se recomienda emplear solución salina 0,9% como diluyente predeterminado para la NA periférica.
Conclusioneslas infusiones periféricas de noradrenalina podrían ser una opción segura y beneficiosa en la reanimación temprana siempre y cuando se sigan una serie de directrices que reduzcan la probabilidad de las complicaciones asociadas a esta vía.
To review and analyze the available literature on peripheral administration of noradrenaline (NA) with the aim of providing recommendations to ensure correct use and patient safety.
MethodsSystematic review on the databases PubMed, ISI Web of Science, SCOPUS and Science Direct, using the following search terms: (“Noradrenaline” [Mesh]) AND (“Norepinephrine” [Mesh]) AND (“Vasopressors” [Mesh]) AND (“Peripheral infusions” [Mesh]) OR (“Extravasations” [Mesh]). A total of 1,040 articles were identified. Animal studies and studies written in languages other than English were excluded. Finally, 83 articles were included.
ResultsNA can be administered peripherally. The risk of extravasation should be taken into account, with phentolamine being the first pharmacological line of treatment. It has also been related to the appearance of thrombophlebitis, cellulitis, tissue necrosis, limb ischemia and gangrene, although its incidence seems to be low. The use of peripheral NA in children seems to be carried out without obvious complications. The use of standard concentrations is suggested to reduce the risk of errors. It is recommended to use 0.9% saline as the default diluent for peripheral NA.
ConclusionsPeripheral infusions of NA could be a safe and beneficial option in early resuscitation provided that a number of guidelines are followed that reduce the likelihood of complications associated with this route.
La noradrenalina (NA) es una catecolamina (agonista α1 y β1 adrenoreceptor) utilizada para restaurar la presión arterial en diversas situaciones de shock debido a sus propiedades vasoconstrictoras, considerándose al día de hoy el vasopresor de primera línea1–3. En nuestro país coexisten comercializadas la NA bitartrato, correspondiente a concentraciones de 0,5 mg/ml y 1 mg/ml de NA base (1 mg/ml y 2 mg/ml de NA bitartrato, respectivamente). La dosis administrada no está condicionada por estas diferencias ya que se dosifica por el peso del paciente; sin embargo, el volumen sí puede variar de forma sustancial en función de las distintas diluciones4.
Tradicionalmente, los vasopresores se han infundido por vía central; sin embargo, en los últimos años, algunos como la fenilefrina y la dopamina se han administrado por vía periférica, a diferencia de la NA5. Un análisis post hoc del estudio Australasian Resuscitation In Sepsis Evaluation (ARISE) del año 2020, demostró que los pacientes con shock séptico a los que se les administró NA a través de un acceso vascular periférico iniciaron el tratamiento vasoactivo aproximadamente 2,5 horas antes y sin aumentar el riesgo de complicaciones6. Una revisión sistemática reciente de la literatura centrada en vasopresores por vía periférica refleja que la NA es el agente administrado con mayor frecuencia (702 episodios), seguido por fenilefrina (546), dopamina (108), metaraminol (74) y vasopresina-adrenalina (<5 episodios)7. Existe una preocupación por este uso de NA por vía periférica y puede atribuirse a que in vivo posee una potencia vasoconstrictora de un 76% superior a la fenilefrina8.
Habitualmente las concentraciones clásicas empleadas en los servicios de medicina crítica son de 200 μg/ml y en ocasiones 400 μg/ml de NA bitartrato. Clásicamente se ha recomendado su administración a través de un catéter venoso central por el riesgo que poseen los medicamentos vasoactivos de producir daño local y necrosis tisular en el caso de producirse una extravasación4.
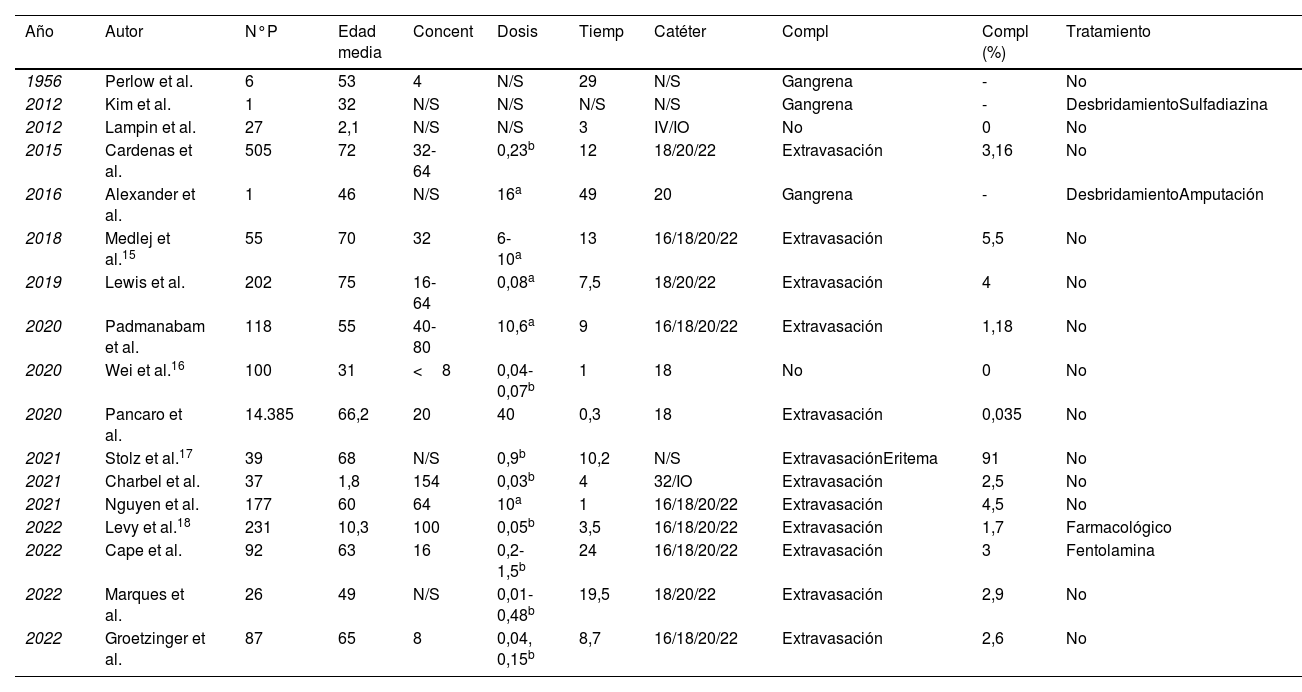
Existen estudios observacionales y guías clínicas que propugnan con una creciente popularidad el empleo de vasopresores como la NA por vía periférica durante cortos periodos de tiempo, aunque con poca evidencia médica9. No hay estudios que comparen directamente la extravasación y el daño tisular entre ambas vías de administración, lo que dificulta la verdadera evaluación de la administración de noradrenalina por vía periférica10. La tabla 1 muestra una revisión de los diversos artículos publicados con infusiones de NA periférica en población adulta y pediátrica. Se postula que este tipo de administración disminuye el tiempo requerido para tratar y controlar la inestabilidad hemodinámica, y esto a su vez, se ha asociado con una disminución de la morbimortalidad11–14.
Artículos publicados de administración de noradrenalina por vía periférica en población adulta y pediátrica
| Año | Autor | N°P | Edad media | Concent | Dosis | Tiemp | Catéter | Compl | Compl (%) | Tratamiento |
|---|---|---|---|---|---|---|---|---|---|---|
| 1956 | Perlow et al. | 6 | 53 | 4 | N/S | 29 | N/S | Gangrena | - | No |
| 2012 | Kim et al. | 1 | 32 | N/S | N/S | N/S | N/S | Gangrena | - | DesbridamientoSulfadiazina |
| 2012 | Lampin et al. | 27 | 2,1 | N/S | N/S | 3 | IV/IO | No | 0 | No |
| 2015 | Cardenas et al. | 505 | 72 | 32-64 | 0,23b | 12 | 18/20/22 | Extravasación | 3,16 | No |
| 2016 | Alexander et al. | 1 | 46 | N/S | 16a | 49 | 20 | Gangrena | - | DesbridamientoAmputación |
| 2018 | Medlej et al.15 | 55 | 70 | 32 | 6-10a | 13 | 16/18/20/22 | Extravasación | 5,5 | No |
| 2019 | Lewis et al. | 202 | 75 | 16-64 | 0,08a | 7,5 | 18/20/22 | Extravasación | 4 | No |
| 2020 | Padmanabam et al. | 118 | 55 | 40-80 | 10,6a | 9 | 16/18/20/22 | Extravasación | 1,18 | No |
| 2020 | Wei et al.16 | 100 | 31 | <8 | 0,04-0,07b | 1 | 18 | No | 0 | No |
| 2020 | Pancaro et al. | 14.385 | 66,2 | 20 | 40 | 0,3 | 18 | Extravasación | 0,035 | No |
| 2021 | Stolz et al.17 | 39 | 68 | N/S | 0,9b | 10,2 | N/S | ExtravasaciónEritema | 91 | No |
| 2021 | Charbel et al. | 37 | 1,8 | 154 | 0,03b | 4 | 32/IO | Extravasación | 2,5 | No |
| 2021 | Nguyen et al. | 177 | 60 | 64 | 10a | 1 | 16/18/20/22 | Extravasación | 4,5 | No |
| 2022 | Levy et al.18 | 231 | 10,3 | 100 | 0,05b | 3,5 | 16/18/20/22 | Extravasación | 1,7 | Farmacológico |
| 2022 | Cape et al. | 92 | 63 | 16 | 0,2-1,5b | 24 | 16/18/20/22 | Extravasación | 3 | Fentolamina |
| 2022 | Marques et al. | 26 | 49 | N/S | 0,01-0,48b | 19,5 | 18/20/22 | Extravasación | 2,9 | No |
| 2022 | Groetzinger et al. | 87 | 65 | 8 | 0,04, 0,15b | 8,7 | 16/18/20/22 | Extravasación | 2,6 | No |
Catéter: calibre del catéter; Compl: tipo de complicaciones; Compl (%): Tanto por ciento de complicaciones; Concent: concentración de noradrenalina en μg/ml; IV: intravenoso; IO: intraóseo; N°P: número de pacientes; N/S: no sabe; Tiemp: tiempo en horas.
Por las razones expuestas anteriormente y al ser considerada una medicación de alto riesgo, es preciso abordar estrategias de seguridad desde las unidades implicadas en su uso habitual y que participan en su proceso asistencial, como el servicio de farmacia hospitalaria. De forma generalizada, faltan protocolos estandarizados en relación a la vía de administración periférica de estos fármacos. Se cree que existen una serie de directrices que deben cumplirse siempre, por lo que es vital la existencia de protocolos consensuados realizados por equipos multidisciplinares que incluyan a médicos, farmacéuticos y enfermeros para evitar la aparición de efectos adversos. También es importante la implementación de programas de calidad que, por ejemplo, eviten una administración conjunta de medicamentos vasopresores con otras medicaciones para evitar los bolos inadvertidos.
El objetivo de esta revisión es analizar y sintetizar la evidencia aportada por la literatura médica disponible sobre la administración de NA por vía periférica tanto en los adultos como en los niños, con el fin de consensuar unas prácticas de actuación que aseguren su correcto empleo y la seguridad del paciente.
MetodologíaSe llevó a cabo una revisión sistemática sobre la administración de noradrenalina por vía periférica en las bases de datos PubMed, ISI Web of Science, SCOPUS y Science Direct. La búsqueda se realizó en octubre de 2023 estableciendo un horizonte temporal de 10 años (2013-2023). Se diseñó una estrategia de búsqueda que utilizó los siguientes términos Mesh: («Noradrenaline» [Mesh]) AND («Norepinephrine» [Mesh]) AND («Vasopressors» [Mesh]) AND («Peripheral infussions» [Mesh]) OR («Extravasations» [Mesh]).
Se incluyeron todas las publicaciones con fecha de publicación de los últimos 10 años sin distinguir en tipo de artículo ni filtros adicionales.
Se excluyeron estudios en animales, estudios escritos en idiomas diferentes al inglés o español y aquellos publicados en revistas no indexadas.
Para elaborar una estrategia de búsqueda bibliográfica coherente, se formuló la siguiente pregunta de investigación siguiendo la metodología PICO: «¿cómo administrar noradrenalina por vía periférica en pacientes con necesidad de reanimación temprana para asegurar su seguridad y eficacia?» Se encuentra desglosada en la tabla 2.
Pregunta de investigación según formato PICO
| Componentes | Descripción |
|---|---|
| Paciente o problema | Pacientes en necesidad de reanimación temprana que reciben noradrenalina por vía periférica |
| Intervención | Uso de noradrenalina periférica siguiendo protocolos estandarizados y con monitorización adecuada |
| Comparación | Administración central de noradrenalina u otros vasopresores |
| Outcomes (Resultados) | Reducción de complicaciones asociadas a la administración periférica de noradrenalina, seguridad del paciente y efectividad en el manejo de la inestabilidad hemodinámica |
| Pregunta resultante | ¿Cómo administrar noradrenalina por vía periférica en pacientes con necesidad de reanimación temprana para asegurar su seguridad y eficacia? |
PICO: Población/Problema, Intervención, comparación, resultados.
Tres revisores evaluaron de forma independiente todos los títulos y resúmenes basados en los criterios de elegibilidad definidos. Si el resumen cumplía con los criterios de inclusión, se leía y analizaba el texto completo. Las diferencias en las opiniones de los revisores se resolvieron mediante discusión y consenso o consulta con un tercer revisor. Con el propósito de asegurar la calidad del análisis, se consideraron exclusivamente estudios publicados en revistas indexadas y aquellos que detallaran los datos esenciales definidos por Dartois et al.19. Estos comprenden las características esenciales de los pacientes, las dosis y la vía de administración, el número de observaciones, la selección del modelo, el modelo estructural, la variabilidad interindividual, los modelos de error, el método de estimación y el software utilizado.
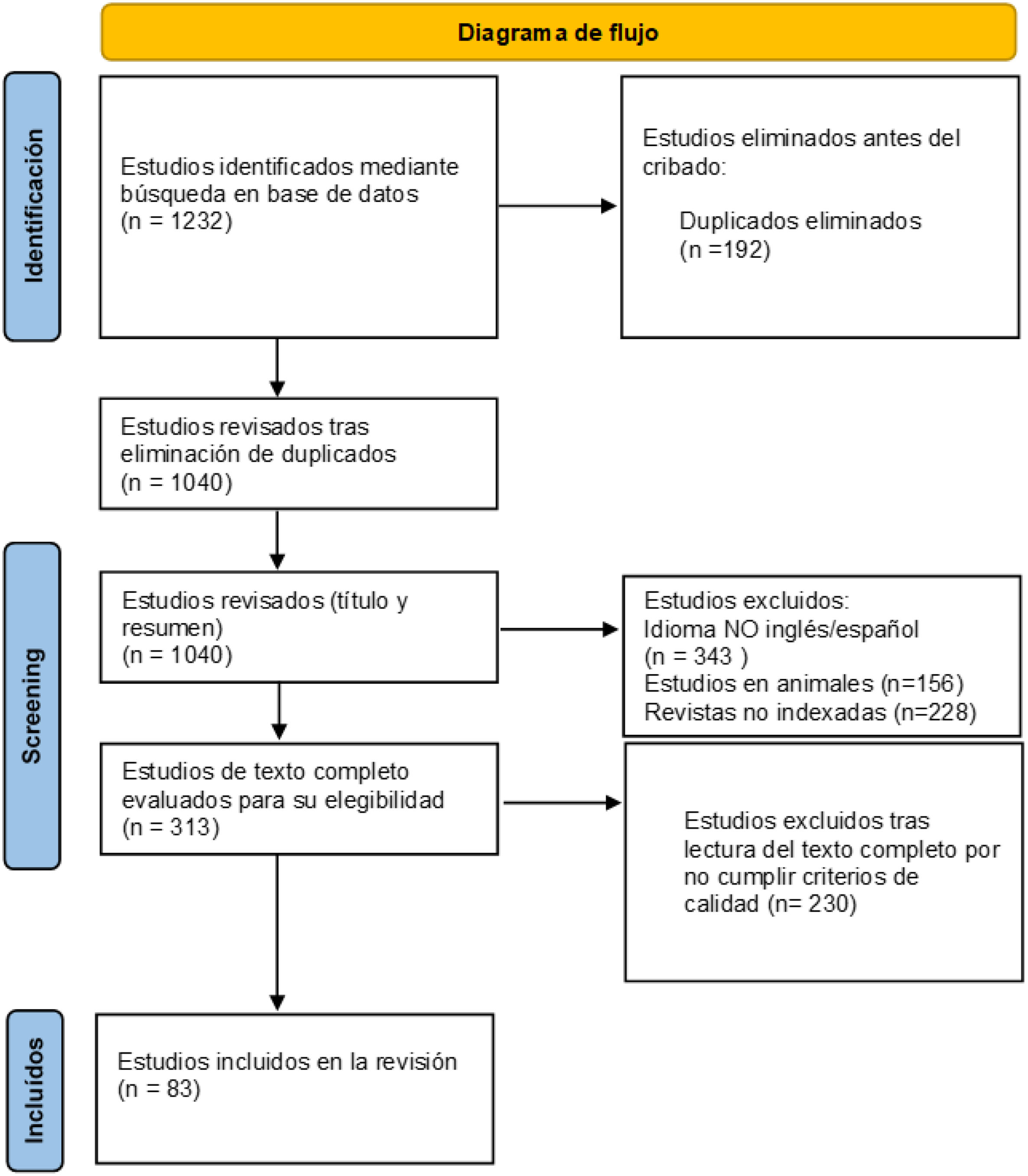
Esta revisión sistemática fue desarrollada según los criterios PRISMA encaminados a optimizar la calidad de las revisiones sistemáticas.
ResultadosLa búsqueda electrónica permitió identificar 1.040 artículos no repetidos en las distintas bases de datos.
Tras el análisis por los revisores, se escogieron 83 artículos para su análisis, 20 de los cuales correspondían a protocolos médicos realizados por diferentes instituciones sanitarias de todo el mundo.
La figura 1 muestra el diagrama de flujo PRISMA de la búsqueda bibliográfica y selección de artículos.
Las principales cuestiones a responder son:
¿Se puede administrar noradrenalina por vía periférica? Sí, pero la norma general es mediante un acceso venoso central para una administración segura, debido al riesgo de extravasación (fuga inadvertida del medicamento a tejidos circundantes)5.
En los últimos años está emergiendo en la práctica médica una administración periférica de diversos agentes vasopresores, principalmente durante la práctica anestésica en el periodo perioperatorio, situaciones de inserción compleja o contraindicaciones de canalización de vía central, durante el tiempo de instauración de dichos accesos centrales, países en vías de desarrollo y/o preferencia del paciente (tabla 1).
¿Es seguro el empleo de noradrenalina periférica en medicina perioperatoria? En nuestro país las publicaciones sobre el uso de NA periférica son anecdóticas, al contrario que en el norte de Europa, principalmente Holanda20. Un estudio retrospectivo de los años 2012-2016 de los hospitales de Ámsterdam y Utrech, que incluye 14.385 pacientes quirúrgicos que precisaron NA por vía periférica durante una anestesia general, estiman un riesgo de extravasación de 1-8 casos cada 10.000 pacientes y todos los casos fueron leves y no precisaron tratamiento médico y/o quirúrgico5. Además, el trabajo reciente de Fu et al.21 describe que la NA por vía periférica con infusiones a 0,08 μg/kg/minuto a muy bajas concentraciones (8 μg/ml) es altamente efectiva en el control de la hipotensión arterial tras la anestesia subaracnoidea en cesáreas, sin correlacionarse con efectos adversos graves.
La escuela holandesa aboga por la seguridad tras más de una década empleándola en el periodo perioperatorio por múltiples razones, entre las que podemos destacar la «hipervigilancia» del paciente en el ámbito quirúrgico, la dilución de NA y baja tasa de infusión.
¿Empleo de noradrenalina periférica en niños? Es menos frecuente su uso que en adultos, por lo que la literatura es muy limitada, pero estudios reportan su uso sin complicaciones evidentes. Se describe también su uso intraóseo22,23.
Charbel et al.23 en una serie de 37 pacientes pediátricos muestra las diferencias con respecto a la administración en pacientes adultos, como su uso con gran proporción en vías distales, empleo de perfusiones con mayor concentración (entre 40-245 μg/ml), una tasa de infusión alta de hasta 0,4 μg/kg/minuto (velocidad de 0,9-2 ml/hora), pero al igual que en los adultos, con una duración de infusión corta (tiempo máximo de 270 minutos) mostrando un solo caso de extravasación leve sin necesidad de tratamiento.
¿Es importante una estandarización de las dosis, concentraciones y duración de la infusión de medicamentos vasoactivos? Sí. Existen pocos datos respecto a esta cuestión, pero parece recomendable el empleo de unas concentraciones estándares en todas las áreas clínicas para reducir el riesgo de errores derivados de la existencia de diferentes concentraciones. Las concentraciones siempre deben ser más bajas para su empleo por vía periférica que cuando se emplean por un catéter central y nunca son intercambiables (tabla 1). La NA periférica habitualmente se administra a una concentración que oscila, según la literatura, entre 16-32 μg/ml debido a la preocupación por la extravasación y la necrosis de tejidos24. La proporción de complicaciones asociadas a la administración de NA por vía periférica se correlaciona con la dosis (12% vs. 2%) si las dosis utilizadas son menores a 0,13 μg/kg/minuto y unas concentraciones inferiores a 22,3 μg/ml25. La escuela holandesa, con una amplia experiencia en el ámbito de la anestesiología, emplea de forma estándar una dilución de 20 μg/ml con una tasa de infusión de 0,01 y 0,1 μg/kg/minuto con un volumen administrado aproximadamente de 2-15 ml/hora5.
La razón de la necesidad de estas bajas concentraciones es por el aumento de la vasoconstricción local desarrollada al infundir el fármaco junto con la hipoperfusión tisular asociada, que con el tiempo pudiera conllevar a una lesión tisular local4.
La infusión siempre debe realizarse mediante bombas electrónicas que facilitan una detección precoz de obstrucción del flujo por sus alarmas de alta sensibilidad2.
La duración de la infusión se correlaciona con el riesgo de extravasación y debe ser determinado por los protocolos locales y estudiado caso a caso (tabla 1), ya que no existen estudios de alta calidad sobre dicha cuestión. La reciente revisión de Loubani y Green indica que el tiempo de administración del fármaco osciló entre una y 528 horas, con una media de 24 horas4. Cárdenas et al.26 exponen en un estudio observacional la reducción de complicaciones con el uso de la ecografía en la canalización venosa, el empleo de catéteres de 20 o 18 G en fosa antecubital y una duración de la infusión inferior a las 72 horas. Cape et al.27 muestran que los casos de extravasación son de aparición muy temprana (2,43 horas) destacando la necesidad de una vigilancia estrecha, principalmente en aquellos casos con vías periféricas de pequeño grosor y unas altas tasas de infusión.
¿Emplearemos cualquier diluyente? No. Varios hospitales recomiendan emplear solución salina 0,9% como diluyente predeterminado para la NA periférica tras la aparición de casos de hiponatremia severa y convulsiones secundarias a la administración de NA periférica a 4 μg/ml en dextrosa al 5%24. La política de dichos hospitales incluye desaconsejar concentraciones tan bajas como la referida por asociarse a un aporte excesivo de cristaloides.
¿Importancia del tamaño y localización del catéter periférico? Existen considerables diferencias entre los trabajos publicados respecto a la importancia del tamaño del catéter28,29. En la revisión de casos expuesta en la tabla 1, el tamaño de los catéteres no influye en la aparición de efectos adversos. Sin embargo, existe un amplio consenso en la importancia de la colocación de las vías de grueso calibre (>4 mm) en fosa antecubital y por encima de la fosa poplítea11. Groetzinger et al.30 reportan una incidencia similar de extravasaciones respecto a otros autores a pesar de que hasta un 44% de las canalizaciones se realizaron bajo control ecográfico.
¿Existe un riesgo bajo de efectos adversos con la administración periférica? Sí. Los riesgos descritos con la administración de NA periférica son: extravasación, tromboflebitis, celulitis, necrosis tisular, isquemia de miembros y gangrena31,32. Hay que tener en cuenta que no todos los vasopresores tienen el mismo efecto a nivel periférico, la NA, por ejemplo, es la que más isquemia produce a nivel distal, esto no pasa con la adrenalina o la fenilefrina subcutánea.
La evidencia médica disponible respecto a la incidencia de dichos efectos adversos indica que es relativamente baja (2-5%) y parece asociarse a una administración durante un tiempo prolongado y una vía periférica distal10. La mayoría de efectos adversos se producen tras más de 6 horas de infusión de vasopresores por vía periférica, aunque se ha reportado un caso de lesión tisular a los 5 minutos de inicio de la administración de fenilefrina por vía periférica33. Se describen casos de necrosis cutánea con dosis extremadamente bajas de NA (4 μg/ml)34. Durante intervenciones quirúrgicas la aparición de complicaciones es más baja que en el paciente crítico (0,035% vs. 4%), probablemente por ausencia de daño endotelial y un mejor árbol venoso periférico10,21.
En distintas series consultadas se describe que en la mayoría de los casos las complicaciones han sido leves, principalmente eritema local y tromboflebitis sin necesidad de intervenciones mayores35. Durante la cirugía, los casos de extravasación son extremadamente raros no reportándose ningún caso asociado a NA, pero si se han correlacionado con la administración periférica de dopamina (6 casos), calcio (5 casos), fenilefrina (2 casos), adrenalina (un caso) y dobutamina (un caso)2.
Por otra parte, una revisión sistemática reciente con más de 1.300 pacientes postula que el riesgo con esta práctica clínica es extremadamente bajo7.
Es importante una monitorización estrecha de esta complicación.
¿Factores de riesgo de extravasación? Su empleo por vía periférica puede originar efectos adversos relacionados a una posible extravasación. Se relaciona una posible extravasación a una serie de factores expuestos en la tabla 3. Entre los factores modificables se incluyen la localización de la vía, el tiempo de infusión, la concentración y la dosis de NA periférica; por lo que se debería incidir en ellos como futuras líneas de investigación. La media de tiempo de extravasación de los diferentes estudios suele ser entre 21 y 35 horas10,11,36.
Factores de riesgo de extravasación
| Categoría y factores de riesgo |
|---|
| Relacionados con el pacienteEnfermedad vascularEnfermedad tejido conectivoDiabetes mellitusHipertensión arterialLinfedemaTromboflebitisAlteración nivel concienciaDeliriumEdades extremasNeuropatías periféricasPaciente crítico |
| Relacionados con la infusiónDuraciónConcentraciónTasa de infusiónLocalización vía periférica |
| Relacionados con la instituciónProtocolo de inserción vías periféricasMonitorización de medicación alto riesgoMedición de grados de extravasaciónProtocolo de tratamiento extravasación |
¿Podemos instaurar medidas y protocolos para disminuir las posibles complicaciones? Sí. Parece imperativo el desarrollo de protocolos locales para la vigilancia de la administración de vasopresores por vía periférica. Un metaanálisis para la evaluación de la incidencia de complicaciones derivadas de la infusión de vasopresores por vía periférica indica que la existencia de controles con pautas de seguridad se asoció con una incidencia significativamente menor de eventos adversos35. Por otra parte, un reciente estudio indica que la existencia de un protocolo de NA periférica se asocia con una disminución en la necesidad de inserción de catéteres venosos centrales de hasta un 30%. Una medida fundamental es la formación del personal en el reconocimiento precoz de los signos y síntomas de una posible extravasación. El acceso venoso debe ser de un tamaño mínimo 20G y este debe ser lo más proximal posible, evitando los lugares de flexión en pacientes despiertos. Se debe comprobar tras su canalización con la aspiración de sangre y administración directa en el bolo de 5-10 ml de suero25.
Los protocolos locales han de detallar las áreas clínicas del empleo de NA por vía periférica como velocidad máxima, duración de la administración de agentes vasopresores e intervalos de tiempo de revisión requeridos para controlar la administración mediante infusión intravenosa periférica (protocolo adjunto). Las recomendaciones expuestas en el protocolo de NA periférica del Departamento de Urgencias del Virginia Commonwealth University Health System se exponen en la tabla 437. En dicho protocolo ha de incluirse la concentración de NA en las preparaciones, la necesidad de tomar la tensión arterial solo en el brazo contralateral a la administración de NA o en los miembros inferiores, así como la posibilidad de comprobación del tamaño de la vena y catéter mediante ecografía. Por otra parte, no parece aconsejable el empleo de varias medicaciones vasopresoras de forma conjunta, aunque diversos trabajos clínicos muestran su empleo (NA-adrenalina y NA vasopresina) sin reportar un aumento de complicaciones38,39.
Protocolo Virginia Commonwealth University Health System
| Máxima dosis de NA 20 mcg/minutoCanalización vía central lo antes posible para disminuir riesgo de extravasaciónVía periférica en la fosa antecubital o la vena yugular externaCatéter 20 o 18GComprobar test positivo a aspiración de sangre y administrar un bolo de 5-10 ml de suero salinoMonitorización horaria de la vía periférica por enfermeríaVigilar signos/síntomas extravasaciónPalidez cutáneaAcrocianosisEdemaÚlceras cutáneasMáxima duración de la infusión de 4 horasNo aplicable en casos de parada cardiacaSi se sospecha extravasación: detener la infusión y valorar reiniciar por otra vía (en diferente extremidad)Tratamiento según protocolo (tabla 5)Otras líneas: nitroglicerina tópica 2% o terbutalina subcutánea |
¿Existe tratamiento para la extravasación de noradrenalina? Sí, se expone un protocolo para el manejo de la extravasación en la tabla 5.
Tratamiento de extravasación por medicamentos avosactivos
| Detener la infusión del fármaco vasopresorAspiración de 4-5 ml por vía periférica si es posibleAplicar gasas calientesRetirar cánula venosa y aplicar vendaje compresivoElevación de la extremidad afectaPrimera línea de tratamiento: fentolamina subcutáneaOtras líneas: nitroglicerina tópica 2% o terbutalina subcutáneaAplicación de analgesia si precisaValoración por el servicio de cirugía plásticaNotificación a la agencia correspondiente del incidente médico. |
Protocolo de tratamiento de las extravasaciones por vasopresores por vía periférica de la Unidad de Reanimación del Hospital Neuro traumatológico de Granada.
La fentolamina es la primera línea farmacológica de tratamiento, es un antagonista alfa adrenérgico que promueve la vasodilatación y un aumento del flujo capilar, se considera efectiva durante las primeras 12 horas posextravasación40. La fentolamina no se encuentra disponible en nuestros hospitales al día de hoy; su disponibilidad es una necesidad para la administración segura de NA periférica. Se puede adquirir como medicamento extranjero con un precio de 603 euros (5 ampollas)40. La preparación es con 5 mg de fentolamina reconstituida con 5 ml de suero salino para conseguir una concentración final de 1 mg/ml. La dosis máxima de fentolamina es de 50 mg y se debe evitar su uso intravenoso. Se inyecta 0,5 ml de esta solución de fentolamina en cada punción (habitualmente se realizan 5 inyecciones) en el área de extravasación empleando agujas de 25 o 27G30.
Otras opciones alternativas incluyen nitroglicerina tópica al 2% y terbutalina subcutánea, aunque esta última no está comercializada en España y tampoco se encuentra disponible como medicamento extranjero41. La nitroglicerina 2% como polvo fino se encuentra disponible en Fagron con un precio de 110,38 euros (100 g), por lo que se podría elaborar la fórmula magistral tópica a partir de esta. La fórmula clásica consistiría en añadir 10 g de nitroglicerina 2% a 80 g de vaselina filante y bajo agitación adicionar 10 g de parafina líquida42.
No obstante, nuestra revisión presenta limitaciones. En ella se incluyeron solo artículos escritos en español e inglés, lo que puede suponer una pérdida de información relevante escrita en otros idiomas. Además, existe heterogeneidad entre los distintos estudios, ya que se llevan a cabo en distintos contextos y con pacientes con diferentes características. También existe un posible riesgo de sesgo por la calidad de los artículos originales.
ConclusionesEntre las conclusiones de este estudio consideramos que la administración de NA por vía periférica tanto en adultos como en población pediátrica podría ser una alternativa a tener en cuenta en la resucitación temprana, ya que se asocia a una reducción del tiempo necesario para manejar la inestabilidad hemodinámica, lo cual, a su vez, ha demostrado estar relacionado con una reducción en la morbimortalidad. Sin embargo, valoramos la necesidad de instaurar protocolos de administración segura de la NA por vía periférica para reducir las complicaciones asociadas a esta vía. La evidencia médica actual parece indicar que el estado basal y comorbilidades del paciente, la concentración de NA y el tiempo de infusión se correlacionan con la aparición de complicaciones.
Con todo ello, creemos oportuno la realización de amplios estudios prospectivos multicéntricos para identificar y resolver las múltiples áreas de penumbra en la administración de vasopresores por vía periférica.
Aportación a la literatura científicaEl tema planteado es novedoso, ya que actualmente no existe publicada en la literatura científica ninguna revisión sistemática sobre la administración de noradrenalina por vía periférica. Aunque la vía de elección sea la central, en determinadas ocasiones existe la necesidad de administrarla por vía periférica. Además, parece que reduce el tiempo requerido para tratar y controlar la inestabilidad hemodinámica y esto a su vez se ha asociado a una disminución de la morbimortalidad.
Por ello, parece imprescindible la existencia de directrices que faciliten su uso y disminuyan las complicaciones asociadas a esta vía. Este trabajo puede ser sumamente beneficioso en el ámbito clínico, ya que sintetiza la información disponible en la actualidad para garantizar su correcto uso y la seguridad del paciente.
FinanciaciónSin financiación.
Conflicto de interesesNo existen conflictos de intereses por parte de ningún autor.
Declaración de contribución de autoría CRediTF. Dámaso Fernández-Ginés: Writing – review & editing, Writing – original draft, Visualization, Validation, Supervision, Software, Resources, Project administration, Methodology, Investigation, Funding acquisition, Formal analysis, Data curation, Conceptualization. María T. Gómez Sánchez: Writing – review & editing, Writing – original draft, Visualization, Validation, Supervision, Software, Resources, Project administration, Methodology, Investigation, Funding acquisition, Formal analysis, Data curation, Conceptualization. Marina Sánchez Valera: Writing – review & editing, Writing – original draft, Visualization, Validation, Supervision, Software, Resources, Project administration, Methodology, Investigation, Funding acquisition, Formal analysis, Data curation, Conceptualization. Beatriz Tauste Hernández: Writing – review & editing, Writing – original draft, Visualization, Validation, Supervision, Software, Resources, Project administration, Methodology, Investigation, Funding acquisition, Formal analysis, Data curation, Conceptualization. Marta Garrido Ortiz: Writing – review & editing, Writing – original draft, Visualization, Validation, Supervision, Software, Resources, Project administration, Methodology, Investigation, Funding acquisition, Formal analysis, Data curation, Conceptualization. Manuel Cortiñas-Sáenz: Writing – review & editing, Writing – original draft, Visualization, Validation, Supervision, Software, Resources, Project administration, Methodology, Investigation, Funding acquisition, Formal analysis, Data curation, Conceptualization.