To develop an integrated computer software application for specialized nutritional support, integrated in the electronic clinical record, which detects automatically and early those undernourished patients or at risk of developing undernourishment, determining points of opportunity for improvement and evaluation of the results.
MethodsThe quality standards published by the Nutrition Work Group of the Spanish Society of Hospital Pharmacy (SEFH) and the recommendations by the Pharmacy Group of the Spanish Society of Parenteral and Enteral Nutrition (SENPE) have been taken into account. According to these quality standards, the nutritional support has to include the following healthcare stages or sub-processes: nutritional screening, nutritional assessment, plan for nutritional care, prescription, preparation and administration.
ResultsThis software allows to conduct, in an automated way, a specific nutritional assessment for those patients with nutritional risk, implementing, if necessary, a nutritional treatment plan, conducting follow-up and traceability of outcomes derived from the implementation of improvement actions, and quantifying to what extent our practice is close to the established standard.
ConclusionsThis software allows to standardize the specialized nutritional support from a multidisciplinary point of view, introducing the concept of quality control per processes, and including patient as the main customer.
Desarrollar una aplicacion informática integral en el soporte nutricional especializado, e integrado en la historia clínica electrónica, que detecte de forma automatizada y precoz a los pacientes desnutridos o en riesgo de desarrollar desnutrición, determinando puntos de oportunidad de mejora y evaluación de resultados.
MétodosSe han tenido en cuenta los estándares de calidad publicados por el grupo de trabajo de nutrición de la Sociedad Española de Farmacia Hospitalaria (SEFH) y las recomendaciones del grupo de farmacia de la Sociedad Española de Nutrición Parenteral y Enteral (SENPE). De acuerdo con dichos estándares de calidad, las etapas o subprocesos asistenciales que debe contemplar el soporte nutricional son: cribado nutricional, valoración nutricional, plan de cuidados nutricionales, formulación, elaboración y administración.
ResultadosLa aplicación permite, de forma automatizada, realizar una valoración nutricional específica a los pacientes con riesgo nutricional, instaurando, si fuese preciso, un plan de tratamiento nutricional y realizando el seguimiento y trazabilidad de los resultados derivados de la implantación de acciones de mejora y, cuantificando en qué medida nuestra práctica se aproxima a la establecida como estándar.
ConclusionesLa aplicación permite estandarizar el soporte nutricional especializado desde un punto multidisciplinar, introduciendo el concepto de control de calidad por procesos y al paciente como cliente principal.
La malnutrición en el paciente hospitalizado es el resultado de la compleja interacción entre enfermedad, alimentación y nutrición. Es importante entender la distinción entre malnutrición causada por desnutrición (inanición no complicada) o por sobre nutrición (obesidad), y la malnutrición relacionada con la enfermedad, ya que el éxito en el tratamiento de ésta última requiere tanto intervenciones nutricionales como médicas o quirúrgicas, pues las intervenciones nutricionales por sí solas no resuelven las anormalidades metabólicas relacionadas con la enfermedad o el traumatismo1.
La malnutrición se relaciona con múltiples factores. Por un lado, la misma enfermedad puede comportar ingesta inadecuada de nutrientes por anorexia, dificultad para la ingesta, problemas de masticación, disfagia, mucositis o falta de autonomía para comer. También dificulta la digestión y la absorción de los alimentos, y puede incluso aumentar los requerimientos nutricionales, bien por estrés metabólico o por existir pérdidas más o menos importantes de nutrientes. Por otro lado, determinados procesos diagnósticos o terapéuticos pueden asimismo contribuir al desarrollo de la desnutrición, bien porque se indique ayuno para realizar determinadas exploraciones, porque el paciente se encuentre en el postoperatorio o porque se le haya indicado reposo digestivo como parte del tratamiento de determinadas situaciones fisiopatológicas (pancreatitis, etc.)2–11.
El 23% de los pacientes ingresados en un hospital español están en riesgo de desnutrición, ésto indica que la desnutrición constituye un problema de seguridad del paciente hospitalizado, ya que repercute sobre las complicaciones de la enfermedad principal motivo de ingreso, y de las asociadas, eleva el riesgo de infecciones, debilita la capacidad de respuesta al tratamiento y disminuye el grado de respuesta inmune. Todo ello se traduce en un incremento de los costes y la estancia hospitalaria. En España supone un aumento de 4 días de media de estancia hospitalaria, un aumento de 1.409 € por enfermo, en aquellos pacientes que ingresaron con riesgo a sufrir desnutrición, y de unos 6.000 € en enfermos que se desnutrieron durante la estancia hospitalaria respecto
a los que no presentaron desnutrición en ningún momento(12).
El soporte nutricional especializado es un proceso de gran complejidad que ofrece múltiples oportunidades para la aparición de errores de medicación en sus distintas etapas: prescripción, formulación, elaboración, administración o monitorización del tratamiento(13). Estudios previos sitúan la proporción de problemas relacionados con la nutrición clínica entre el 30 y el 60%(14).
La nutrición parenteral está incluida en la clasificación de medicamentos de alto riesgo, ya que presenta una probabilidad elevada de causar daños graves a los pacientes en caso de utilización incorrecta(15). La United States Pharmacopeia (USP) tiene registrados más de 2.500 errores relacionados con la NP en un periodo de 5 años. Más recientemente, se ha publicado 9 casos de muertes asociadas con la administración de mezclas de NP contaminadas por Serratia marcenses(16). La Nutrición Enteral (NE), tampoco está exenta de complicaciones (mecánicas, infecciosas, gastrointestinales y metabólicas) y errores que afectan a la seguridad del paciente. La USP y ISMP comunicaron en un periodo de 6 años (2000-2006) 24 incidentes asociados a errores en la utilización de nutrición enteral, de los cuales el 33% correspondieron a sucesos centinela (daño permanente, situaciones potencialmente fatales, muerte)(17).
Tampoco debe olvidarse la falta de sensibilización existente ante este problema por parte de los profesionales sanitarios, tanto por la escasa formación recibida en materia de nutrición, por el desconocimiento de la trascendencia que reviste la malnutrición en la evolución del paciente, como por la inexistencia de recursos para adoptar sistemas de soporte nutricional.
Todo ello provoca que no se apliquen las medidas de detección y de control oportunas de los pacientes con problemas nutricionales, la utilización inadecuada de los recursos de soporte nutricional existentes, el aumento de la morbimortalidad y el de los costes de su atención2–11.
A pesar de las enormes dificultades metodológicas que pueden surgir en los estudios de intervención nutricional, existe evidencia de que la intervención nutricional puede mejorar la evolución clínica del paciente desnutrido y disminuir los gastos asociados a la enfermedad18–20. La Resolución del Comité de Ministros del Consejo de Europa Sobre alimentación y atención nutricional en hospitales aprobada el 12 de noviembre de 2003 pone de manifiesto la importancia de la desnutrición en los hospitales así como medidas encaminadas a su prevención y tratamiento21.
De acuerdo con lo expuesto, y con el fin de maximizar los recursos disponibles, sería recomendable utilizar aplicativos informáticos que permitan realizar una valoración inicial encaminada a detectar precozmente los pacientes desnutridos o en riesgo de desarrollar desnutrición y ,posteriormente, realizar una valoración nutricional más específica e instaurar, si es preciso, un plan de tratamiento nutricional. A pesar de que en nuestro entorno están disponibles varios programas informáticos relacionados con el soporte nutricional (Nutridata©, Kabisoft©, Nutriwin©, Multicomp©, Medical One©(22)(23)), ninguno reúne todas las recomendaciones para el control integral de la desnutrición hospitalaria. A modo de ejemplo no presentan sistema de cribado nutricional para paciente adulto y/o pediátrico, y la gran mayoría de ellos no permiten obtener la información necesaria para realizar un control de calidad adecuado a la hora de obtener los indicadores de los diferentes procesos implicados.
Objetivos- 1.
Describir las características de un nuevo programa informático para la prescripción electrónica asistida de la nutrición parenteral y enteral.
- 2.
Definir las diferentes ayudas a la prescripción implicadas en el proceso de soporte nutricional con el fin de estandarizar y protocolizar el soporte nutricional.
- 3.
Describir las integraciones realizadas con la historia clínica electrónica del Hospital Comarcal de Inca.
Para el desarrollo del aplicativo informático se tuvieron en cuenta las características que según el Grupo de Evaluación de Nuevas tecnologías (Grupo TECNO) de la Sociedad Española de Farmacia Hospitalaria (SEFH) entiende que debe reunir toda nueva tecnología aplicada al uso de los medicamentos24, así como los estándares de práctica publicados por el grupo de trabajo de nutrición de la SEFH. De acuerdo con dichos estándares de calidad, las etapas o subprocesos asistenciales que debe contemplar el soporte nutricional son: cribado nutricional, valoración nutricional, plan de cuidados nutricionales, formulación, elaboración, administración, monitorización y finalización del tratamiento13,25. A continuación se describen las características de cada subproceso junto con las diferentes ayudas a la prescripción implementadas.
El mapa del proceso asistencial del soporte nutricional de dicho aplicativo se incia con la inclusión de los pacientes vía integración informática desde el servicio de admisión. Todo paciente se cribará dentro de las primeras 48 horas de ingreso.
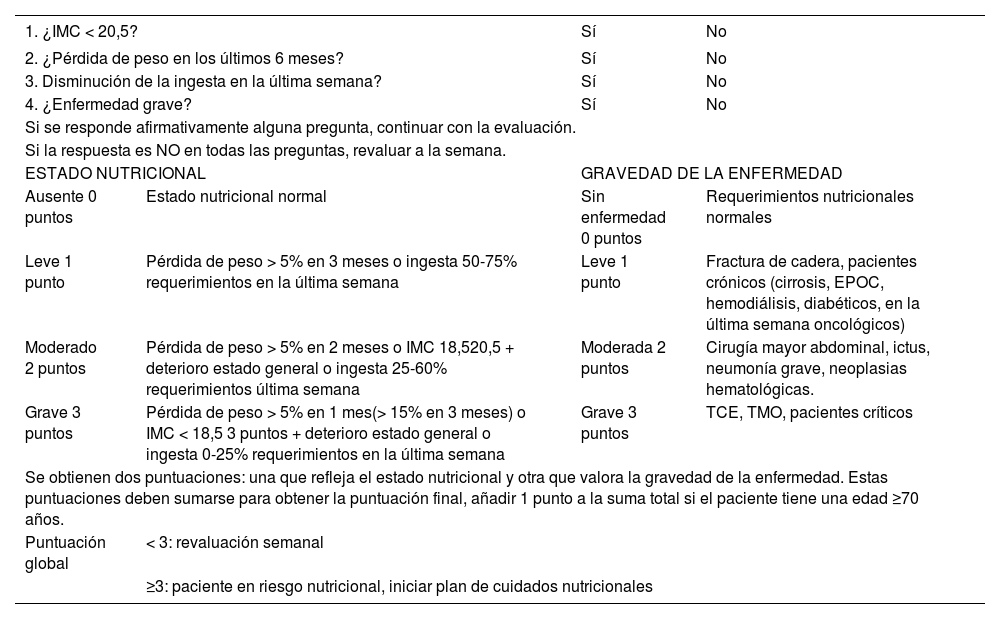
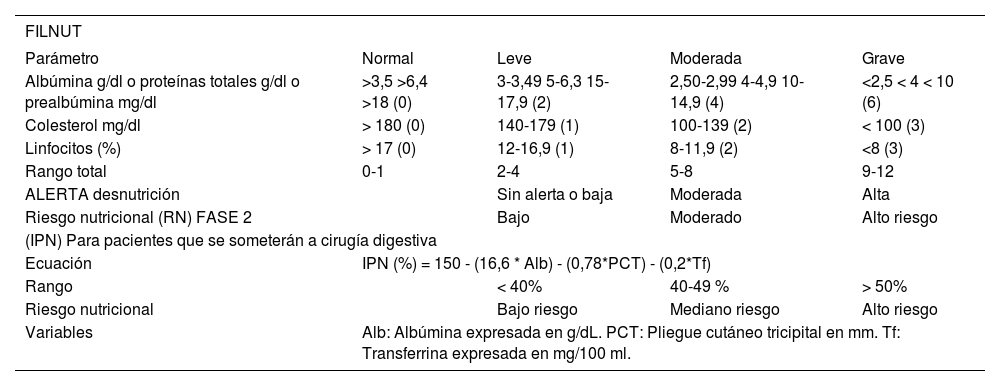
El cribado nutricional seleccionado para el paciente adulto fue el NRS-200226 (Tabla 1) y FILNUT como filtro informático27 (Tabla 2). Para el paciente pediátrico se seleccionó el sistema de cribado nutricional PYMS28 (Tabla 3). En este apartado también se incluyó un método alternativo desarrollado por la British Association for Parenteral and Enteral Nutrition (BAPEN), para determinar talla del paciente basado en la distancia olecranon estiloides, la edad y el sexo del paciente29.
NRS-2002 (Nutritional Risk Screening)
| 1. ¿IMC < 20,5? | Sí | No | |
|---|---|---|---|
| 2. ¿Pérdida de peso en los últimos 6 meses? | Sí | No | |
| 3. Disminución de la ingesta en la última semana? | Sí | No | |
| 4. ¿Enfermedad grave? | Sí | No | |
| Si se responde afirmativamente alguna pregunta, continuar con la evaluación. | |||
| Si la respuesta es NO en todas las preguntas, revaluar a la semana. | |||
| ESTADO NUTRICIONAL | GRAVEDAD DE LA ENFERMEDAD | ||
| Ausente 0 puntos | Estado nutricional normal | Sin enfermedad 0 puntos | Requerimientos nutricionales normales |
| Leve 1 punto | Pérdida de peso > 5% en 3 meses o ingesta 50-75% requerimientos en la última semana | Leve 1 punto | Fractura de cadera, pacientes crónicos (cirrosis, EPOC, hemodiálisis, diabéticos, en la última semana oncológicos) |
| Moderado 2 puntos | Pérdida de peso > 5% en 2 meses o IMC 18,520,5 + deterioro estado general o ingesta 25-60% requerimientos última semana | Moderada 2 puntos | Cirugía mayor abdominal, ictus, neumonía grave, neoplasias hematológicas. |
| Grave 3 puntos | Pérdida de peso > 5% en 1 mes(> 15% en 3 meses) o IMC < 18,5 3 puntos + deterioro estado general o ingesta 0-25% requerimientos en la última semana | Grave 3 puntos | TCE, TMO, pacientes críticos |
| Se obtienen dos puntuaciones: una que refleja el estado nutricional y otra que valora la gravedad de la enfermedad. Estas puntuaciones deben sumarse para obtener la puntuación final, añadir 1 punto a la suma total si el paciente tiene una edad ≥70 años. | |||
| Puntuación global | < 3: revaluación semanal | ||
| ≥3: paciente en riesgo nutricional, iniciar plan de cuidados nutricionales | |||
EPOC: enfermedad pulmonar obstructiva crónica; IMC: índice de masa corporal; TCE: traumatismo craneoencefálico; TMO: trasplante de médula ósea.
Filtros informáticos paciente adulto
| FILNUT | ||||
|---|---|---|---|---|
| Parámetro | Normal | Leve | Moderada | Grave |
| Albúmina g/dl o proteínas totales g/dl o prealbúmina mg/dl | >3,5 >6,4 >18 (0) | 3-3,49 5-6,3 15-17,9 (2) | 2,50-2,99 4-4,9 10-14,9 (4) | <2,5 < 4 < 10 (6) |
| Colesterol mg/dl | > 180 (0) | 140-179 (1) | 100-139 (2) | < 100 (3) |
| Linfocitos (%) | > 17 (0) | 12-16,9 (1) | 8-11,9 (2) | <8 (3) |
| Rango total | 0-1 | 2-4 | 5-8 | 9-12 |
| ALERTA desnutrición | Sin alerta o baja | Moderada | Alta | |
| Riesgo nutricional (RN) FASE 2 | Bajo | Moderado | Alto riesgo | |
| (IPN) Para pacientes que se someterán a cirugía digestiva | ||||
| Ecuación | IPN (%) = 150 - (16,6 * Alb) - (0,78*PCT) - (0,2*Tf) | |||
| Rango | < 40% | 40-49 % | > 50% | |
| Riesgo nutricional | Bajo riesgo | Mediano riesgo | Alto riesgo | |
| Variables | Alb: Albúmina expresada en g/dL. PCT: Pliegue cutáneo tricipital en mm. Tf: Transferrina expresada en mg/100 ml. | |||
Sistema Cribado Nutricional PYMS.
| 1.¿EL VALOR DEL IMC ES INFERIOR AL DE REFERENCIA? | NO | 0 | PUNTUACION |
|---|---|---|---|
| SI | 2 | ||
| NO | 0 | ||
| 2. ¿HA PERDIDO PESO RECIENTEMENTE? | SI | ||
| PERDIDA DE PESO NO INTENCIONADA | 1 | ||
| ROPA HOLGADA | |||
| BAJA GANANCIA DE PESO (SI < 2 AÑOS) | |||
| NO | 0 | ||
| INGESTA ORDINARIA | |||
| 3.¿SE HA REDUCIDO LA INGESTA AL MENOS DURANTE LA ÚLTIMA SEMANA? | SI | 1 | |
| DISMINUCIÓN INGESTA ORIDINARIA AL MENOS LA ÚLTIMA SEMANA | |||
| SI | |||
| NO INGESTA (O PEQUEÑOS SORBOS O ALIMENTOS) AL MESNO LA ÚLTIMA SEMANA | 2 | ||
| NO | 0 | ||
| SI | |||
| 4.¿SE VERÁ AFECTADA LA INGESTA AL MENOS DURANTE LA PRÓXIMA SEMANA DEBIDO A LA CAUSA DE INGRESO? | POR LO MENOS DURANTE LA PRÓXIMA SEMANA | ||
| DISMINUCIÓN INGESTA Y/O | 1 | ||
| AUMENTO DE LOS REQUERIMIENTOS Y/O | |||
| AUMENTO DE PÉRDIDAS | |||
| SI | |||
| NO INGESTA (O PEQUEÑOS SORBOS O INGESTA) AL MENOS LA PRÓXIMA SEMANA | 2 | ||
| 0: REPETIR PYMS EN UNA SEMANA | |||
| PUNTUACION GLOBAL:- | 1: REPETIR PYMS EN 3 DÍAS | ||
| ≥2: VALORACION NUTRICIONAL + REPETIR PYMS EN UNA SEMANA |
Si el paciente adulto no está en riesgo nutricional la aplicación no volverá a solicitar el cribado hasta dentro de una semana, siempre y cuando no exista un score de riesgo FILNUT; y en el paciente pediátrico dependerá de la puntuación del score PYMS (Tabla 3).
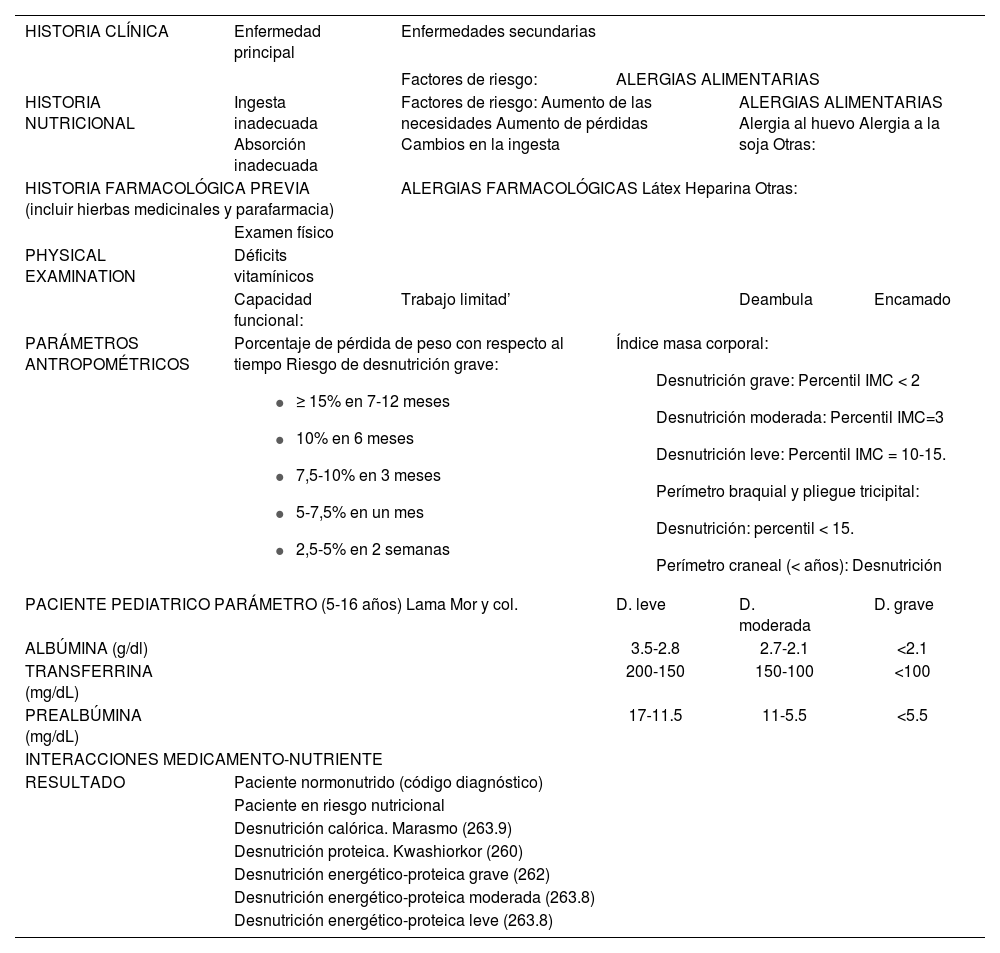
Los pacientes adultos con riesgo nutricional son valorados de acuerdo con el registro valoración nutricional (Tabla 4) y para el paciente pediátrico de acuerdo con las recomendaciones de Asociación Española de Pediatría (AEPED) (Tabla 5)25,30.
Registro de la Valoración Nutricional paciente adulto
| HISTORIA CLÍNICA | Enfermedad principal | Enfermedades secundarias | ||
|---|---|---|---|---|
| HISTORIA NUTRICIONAL | Ingesta inadecuada Absorción inadecuada | Factores de riesgo: Aumento de las necesidades Aumento de pérdidas Cambios en la ingesta | ALERGIAS ALIMENTARIAS Alergia al huevo Alergia a la soja Otras: | |
| HISTORIA FARMACOLÓGICA PREVIA (incluir hierbas medicinales y parafarmacia) | ALERGIAS FARMACOLÓGICAS Látex Heparina Otras: | |||
| Examen físico | ||||
| EXPLORACIÓN FÍSICA | Déficits vitamínicos | |||
| Capacidad funcional: | Trabajo limitado | Deambula | Encamado | |
| PARÁMETROS ANTROPOMÉTRICOS | Porcentaje de pérdida de peso con respecto al tiempo Riesgo de desnutrición grave:
| Índice de masa corporal (IMC)
| ||
| PARÁMETROS BIOQUÍMICOS | D. leve | D. moderada | D. grave | |
| Albúmina (g/dl) | 3,5-2,8 | 2,7-2,1 | < 2,1 | |
| Linfocitos (n.°/mm3) | 2.000-1.200 | 1.200-800 | < 800 | |
| Colesterol (mg/dl) | 179-140 | 139-100 | < 100 | |
| INTERACCIONES MEDICAMENTO-NUTRIENTE | ||||
| RESULTADO | Paciente normonutrido (código diagnóstico) | |||
| Paciente en riesgo nutricional | ||||
| Desnutrición calórica. Marasmo (263.9) | ||||
| Desnutrición proteica. Kwashiorkor (260) | ||||
| Desnutrición energético-proteica grave (262) | ||||
| Desnutrición energético-proteica moderada (263.8) | ||||
| Desnutrición energético-proteica leve (263.8) | ||||
Registro de la Valoración Nutricional paciente pediátrico
| HISTORIA CLÍNICA | Enfermedad principal | Enfermedades secundarias | |||
|---|---|---|---|---|---|
| Factores de riesgo: | ALERGIAS ALIMENTARIAS | ||||
| HISTORIA NUTRICIONAL | Ingesta inadecuada Absorción inadecuada | Factores de riesgo: Aumento de las necesidades Aumento de pérdidas Cambios en la ingesta | ALERGIAS ALIMENTARIAS Alergia al huevo Alergia a la soja Otras: | ||
| HISTORIA FARMACOLÓGICA PREVIA (incluir hierbas medicinales y parafarmacia) | ALERGIAS FARMACOLÓGICAS Látex Heparina Otras: | ||||
| Examen físico | |||||
| PHYSICAL EXAMINATION | Déficits vitamínicos | ||||
| Capacidad funcional: | Trabajo limitad’ | Deambula | Encamado | ||
| PARÁMETROS ANTROPOMÉTRICOS | Porcentaje de pérdida de peso con respecto al tiempo Riesgo de desnutrición grave:
| Índice masa corporal:
| |||
| PACIENTE PEDIATRICO PARÁMETRO (5-16 años) Lama Mor y col. | D. leve | D. moderada | D. grave | ||
| ALBÚMINA (g/dl) | 3.5-2.8 | 2.7-2.1 | <2.1 | ||
| TRANSFERRINA (mg/dL) | 200-150 | 150-100 | <100 | ||
| PREALBÚMINA (mg/dL) | 17-11.5 | 11-5.5 | <5.5 | ||
| INTERACCIONES MEDICAMENTO-NUTRIENTE | |||||
| RESULTADO | Paciente normonutrido (código diagnóstico) | ||||
| Paciente en riesgo nutricional | |||||
| Desnutrición calórica. Marasmo (263.9) | |||||
| Desnutrición proteica. Kwashiorkor (260) | |||||
| Desnutrición energético-proteica grave (262) | |||||
| Desnutrición energético-proteica moderada (263.8) | |||||
| Desnutrición energético-proteica leve (263.8) | |||||
Si el paciente no está desnutrido el programa lo clasifica como paciente sin riesgo nutricional.
En aquellos pacientes que presentan desnutrición se define el plan de cuidados nutricionales ,dotado de un sistema de alarmas, que informa si se superan los límites de aportes de los diferentes nutrientes (Tablas 6 y 7), y de la idoneidad de la vía de administración elegida de acuerdo con la duración del soporte nutricional especializado estimada (Tabla 8). Si durante los cálculos de los requerimientos la osmolaridad calculada para una nutrición parenteral es superior a 800 mOsm/L, el aplicativo indicará que la nutrición parenteral debe ser administrada por vía central. En las vías centrales, excepto en la umbilical de pediatría, se podrá seleccionar derecha o izquierda.
Plan de cuidados nutricionales en el paciente adulto
| Requerimientos energéticos GEB: gasto energético basal GER: gasto energético en reposo | GET (kcal) = GEB ó GER x FA x FE | |
|---|---|---|
| Para determinar los requerimientos energéticos, en el paciente adulto, todos los cálculos se realizan con el peso actual del paciente, con las excepciones siguientes: | ||
| — Pacientes obesos (peso actual > 20% del peso ideal o IMC ≥30 kg/m2): Se utilizará peso corporal ajustado (PCA = (peso ideal + 0,25 [peso real - peso ideal]).), salvo en las ecuaciones en las que específicamente se indique el empleo del peso real. Para determinar el peso ideal se utilizará la ecuación de Lorentz: | ||
| • Varón: peso ideal (kg) = talla (cm) - 100 - (talla [cm] - 150)/4 | ||
| • Mujer: peso ideal (kg) = talla (cm) - 100 - (talla [cm] - 150)/2 | ||
| — Pacientes desnutridos con IMC < 18 kg/m2: Se utilizará el peso real, hasta considerar mínimo el riesgo de síndrome de realimentación; a partir de entonces se utilizará el peso ideal. | ||
| Fórmula predictiva | Ecuación | |
| Harris y Benedict (HB)39Para estimar el gasto energético total, debe multiplicarse por un factor de corrección (1,3-1,5) | • Varón: GEB = 66,47 + (4,8 x altura [cm]) + (13,75 x peso[kg]) - (6,75 x edad [años]) | |
| Puede usarse en ancianos | • Mujer: GEB = 655 + (1,85 x altura [cm]) + 9,56 x peso kg]) - (4,67 x edad [años]) | |
| Mifflin-St. Peor40 | • Varón: GEB = 9,99 x peso + 6,25 x altura - 4,92 x edad + 5 | |
| Adultos con normopeso u obesos (peso real) no críticos | ||
| Cálculo del GER (gasto energético en reposo= 1,1-1,3 x GEB) | • Mujer: GEB = 9,99 x peso + 6,25 x altura - 4,92 x edad - 161 | |
| Penn State41 Pacientes críticos en ventilación mecánica | • HB x 0,85 + ventilación minuto (l) x 33 + temperatura corporal máxima (grados centígrados) x 175 - 6.433 | |
| GER = 15, 8 *MLG + 460 | ||
| Arligton42 Parálisis cerebral | • Varón: %MLG = 0,735 + (suma PCT + PCP (mm)) + 1 | |
| • Mujer: %MLG = 0,610 + (suma PCT + PCP (mm)) + 5,1 | ||
| IMC < 20 preembarazo GER = GEB + (8,8 x semana gestacional) | ||
| Butte43 | • IMC 20-26 preembarazo GER = GEB + (9,5 x semana gestacional) | |
| Embarazadas | • IMC > 26 preembarazo GER = GEB + (16,3 x semana gestacional) | |
| Roza y Shizgal44 | • Varón: 13,397 xpeso (kg) + 4,799 xestatura (cm) - 5,677 xedad (años) +88,362 | |
| Bajo peso (IMC < 18 kg/m2) | • Mujer:3,098 xestatura (cm) + 9,247 xpeso (kg) - 4,330 xedad (años) + 447,593 | |
| Factor Actividad (FA) | Reposo en cama: 1,0 | |
| Movimiento en cama: 1,2. | ||
| Deambulación: 1,3 | ||
| Factor Enfermedad (FE) | Cirugía complicada (mayor): 1,25-1,40. | Gran quemado: 2,10. |
| Cirugía programada (menor): 1,20. | Infecciones: 1,25-1,45. | |
| Desnutridos en general: 1,00. | Leucemia: 1,34. | |
| Enfermedad hepática: 1,00-1,17. | Linfomas: 1,25. | |
| Enfermedad inflamatoria intestinal: 1,05 en ambulatorios y 1,10 en hospitalizados. | Pancreatitis: 1,10 (crónica) y 1,12 (aguda). 1,20 si hay abscesos. | |
| Trasplantes: 1,20. | Quemaduras: 1,60. | |
| Traumatismos: 1,35. | Sepsis: 1,35-1,60. | |
| Tumores sólidos: 1,20 en hospitalizados y 1,00 en ambulatorios estables. | ||
| En todos los casos, además tendremos que añadir un FE de 1,1 por cada grado por encima de 37°C. | ||
| Requerimientos proteicos (g proteína/kg/día): Se calcularán en función de la patología de base y la situación del paciente. Ya que para alcanzar el máximo aprovechamiento de nitrógeno en los procesos de síntesis proteica la relación de calorías no proteicas/gramo de proteína deberá ser la adecuada. De ahí que en fases de estrés, la relación kcal no proteicas/g de nitrógeno será de 90-100; en pacientes con insuficiencia renal 160-200 y 120-160 en el resto de situaciones. | ||
| Requerimientos proteicos basales: | 0,8-1 g/kg/día | |
| Pacientes catabólicos | 1-2 g/kg/día | |
| Insuficiencia renal | 0,6-1 g/kg/día | |
| Insuficiencia renal + diálisis | 1-1,5 g/kg/día | |
| Insuficiencia renal + hemodiafiltración continua | 1,5-2,5 g/kg/día | |
| Hepatopatías | 0,6-1,5 g/kg/día | |
| Requerimientos proteicos (g proteína/kg/día): | ||
| Obesos (IMC 30-40 kg/m2) | 2,5 g/kg Pideal/día | |
| Obesos (IMC > 40 kg/m2) | 2 g/kg Pideal/día | |
| Requerimientos lipídicos: | ||
| Aporte 1-2,5 g/kg/día. La proporción recomendada de lípidos es del 30-40% de las calorías no proteicas. | ||
| Requerimientos hidratos de carbono (glucosa): | ||
| Aportes de glucosa 4-7 g/kg/día. No superar la velocidad de infusión de 5 mg/kg/min. La proporción recomendada de glucosa es del 60-70% de las calorías no proteicas. | ||
| ELECTROLITO | REQUERIMIENTO/kg de peso | DOSIS |
| SODIO | 1-2 mEq/kg | 80-150 mEq |
| POTASIO | 0,5-1 mEq/kg | 40-100 mEq |
| CLORO | 1,5-2 mEq/kg | 50-150 mEq |
| CALCIO | 0,15-0,3 mEq/kg | 10-15 mEq |
| MAGNESIO | 0,25-0,35 mEq/kg | 8-20 mEq |
| FÓSFORO | 0,14 mmol/kg+ajustes según aportes de energía y nitrógeno; función renal | 20-40 mmol |
| ACETATO | Cantidad necesaria para mantener el equilibrio ácido base | |
| Requerimientos oligoelementos | ||
| AMA/NAG | ||
| Cromo | 10-15 μg | |
| Cobre | 0,5-1,5 mg | |
| 0,3-0,5 mg* | ||
| Manganeso | 60-100 μg* | |
| Selenio | 20-60 μg* | |
| Cinc | 2,5-5 mg | |
| *Recomendaciones ASPEN | ||
| Requerimientos vitaminas | ||
| Vitaminas liposolubes | ||
| AMA/NAG | FDA | |
| A (retinol) | 3.300 UI | 3.300 UI |
| D (ergocalciferol) | 200 UI | 200 UI |
| E (alfatocoferol) | 10 mg | 10 mg |
| K (filoquinona) | 100 μg | 150 μg |
| Vitaminas hidrosolubles | ||
| Tiamina (B1 ) | 3 mg | 6 mg |
| Riboflavina (B2) | 3,6 mg | 3,6 mg |
| Piridoxina (B6) | 4 mg | 6 mg |
| Cianocobalamina (B12) | 5 μg | 5 μg |
| C (ácido ascórbico) | 100 mg | 200 mg |
| Ácido fóico | 400 μg | 600 μg |
| Nicotinamida | 40 mg | 40 mg |
| Ácido pantoténico | 15 mg | 15 mg |
| Biotina | 60 μg | 60 μg |
| Requerimientos líquidos: Holliday y Segar. | Edad < 50 años Volumen = 1.500 ml + 20 ml x (peso corporal (kg)- 20) | |
| En caso de hipertermia a estos cálculos el aplicativo adiciona la reposición de las pérdidas ocasionadas, estimadas en 360 ml/24 h por cada grado centígrado que supera los 37 °C. | Edad> 50 años Volumen = 1.500 ml + 15 ml x (peso corporal (kg)- 20) | |
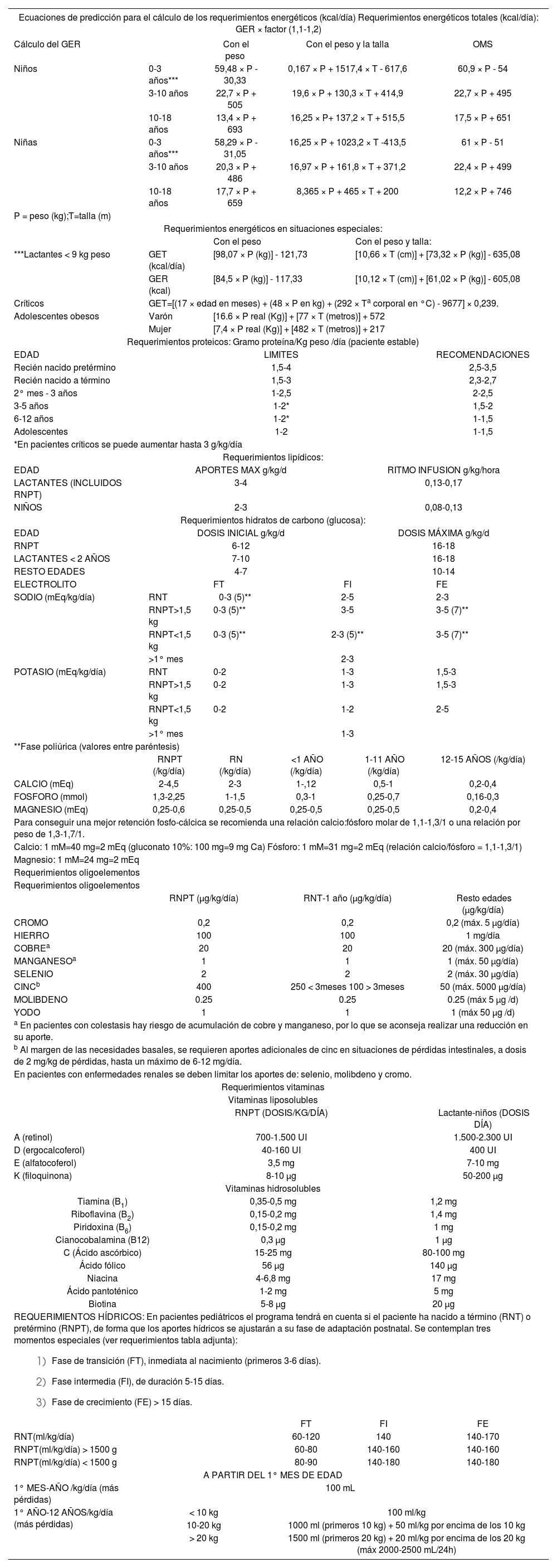
Plan de cuidados nutricionales en el paciente pediátrico
| Ecuaciones de predicción para el cálculo de los requerimientos energéticos (kcal/día) Requerimientos energéticos totales (kcal/día): GER × factor (1,1-1,2) | |||||
|---|---|---|---|---|---|
| Cálculo del GER | Con el peso | Con el peso y la talla | OMS | ||
| Niños | 0-3 años*** | 59,48 × P - 30,33 | 0,167 × P + 1517,4 × T - 617,6 | 60,9 × P - 54 | |
| 3-10 años | 22,7 × P + 505 | 19,6 × P + 130,3 × T + 414,9 | 22,7 × P + 495 | ||
| 10-18 años | 13,4 × P + 693 | 16,25 × P+ 137,2 × T + 515,5 | 17,5 × P + 651 | ||
| Niñas | 0-3 años*** | 58,29 × P - 31,05 | 16,25 × P + 1023,2 × T -413,5 | 61 × P - 51 | |
| 3-10 años | 20,3 × P + 486 | 16,97 × P + 161,8 × T + 371,2 | 22,4 × P + 499 | ||
| 10-18 años | 17,7 × P + 659 | 8,365 × P + 465 × T + 200 | 12,2 × P + 746 | ||
| P = peso (kg);T=talla (m) | |||||
| Requerimientos energéticos en situaciones especiales: | |||||
| Con el peso | Con el peso y talla: | ||||
| ***Lactantes < 9 kg peso | GET (kcal/día) | [98,07 × P (kg)] - 121,73 | [10,66 × T (cm)] + [73,32 × P (kg)] - 635,08 | ||
| GER (kcal) | [84,5 × P (kg)] - 117,33 | [10,12 × T (cm)] + [61,02 × P (kg)] - 605,08 | |||
| Críticos | GET=[(17 × edad en meses) + (48 × P en kg) + (292 × Ta corporal en °C) - 9677] × 0,239. | ||||
| Adolescentes obesos | Varón | [16.6 × P real (Kg)] + [77 × T (metros)] + 572 | |||
| Mujer | [7,4 × P real (Kg)] + [482 × T (metros)] + 217 | ||||
| Requerimientos proteicos: Gramo proteína/Kg peso /día (paciente estable) | |||||
| EDAD | LIMITES | RECOMENDACIONES | |||
| Recién nacido pretérmino | 1,5-4 | 2,5-3,5 | |||
| Recién nacido a término | 1,5-3 | 2,3-2,7 | |||
| 2° mes - 3 años | 1-2,5 | 2-2,5 | |||
| 3-5 años | 1-2* | 1,5-2 | |||
| 6-12 años | 1-2* | 1-1,5 | |||
| Adolescentes | 1-2 | 1-1,5 | |||
| *En pacientes críticos se puede aumentar hasta 3 g/kg/día | |||||
| Requerimientos lipídicos: | |||||
| EDAD | APORTES MAX g/kg/d | RITMO INFUSION g/kg/hora | |||
| LACTANTES (INCLUIDOS RNPT) | 3-4 | 0,13-0,17 | |||
| NIÑOS | 2-3 | 0,08-0,13 | |||
| Requerimientos hidratos de carbono (glucosa): | |||||
| EDAD | DOSIS INICIAL g/kg/d | DOSIS MÁXIMA g/kg/d | |||
| RNPT | 6-12 | 16-18 | |||
| LACTANTES < 2 AÑOS | 7-10 | 16-18 | |||
| RESTO EDADES | 4-7 | 10-14 | |||
| ELECTROLITO | FT | FI | FE | ||
| SODIO (mEq/kg/día) | RNT | 0-3 (5)** | 2-5 | 2-3 | |
| RNPT>1,5 kg | 0-3 (5)** | 3-5 | 3-5 (7)** | ||
| RNPT<1,5 kg | 0-3 (5)** | 2-3 (5)** | 3-5 (7)** | ||
| >1° mes | 2-3 | ||||
| POTASIO (mEq/kg/día) | RNT | 0-2 | 1-3 | 1,5-3 | |
| RNPT>1,5 kg | 0-2 | 1-3 | 1,5-3 | ||
| RNPT<1,5 kg | 0-2 | 1-2 | 2-5 | ||
| >1° mes | 1-3 | ||||
| **Fase poliúrica (valores entre paréntesis) | |||||
| RNPT (/kg/día) | RN (/kg/día) | <1 AÑO (/kg/día) | 1-11 AÑO (/kg/día) | 12-15 AÑOS (/kg/día) | |
| CALCIO (mEq) | 2-4,5 | 2-3 | 1-,12 | 0,5-1 | 0,2-0,4 |
| FOSFORO (mmol) | 1,3-2,25 | 1-1,5 | 0,3-1 | 0,25-0,7 | 0,16-0,3 |
| MAGNESIO (mEq) | 0,25-0,6 | 0,25-0,5 | 0,25-0,5 | 0,25-0,5 | 0,2-0,4 |
| Para conseguir una mejor retención fosfo-cálcica se recomienda una relación calcio:fósforo molar de 1,1-1,3/1 o una relación por peso de 1,3-1,7/1. | |||||
| Calcio: 1 mM=40 mg=2 mEq (gluconato 10%: 100 mg=9 mg Ca) Fósforo: 1 mM=31 mg=2 mEq (relación calcio/fósforo = 1,1-1,3/1) | |||||
| Magnesio: 1 mM=24 mg=2 mEq | |||||
| Requerimientos oligoelementos | |||||
| Requerimientos oligoelementos | |||||
| RNPT (μg/kg/día) | RNT-1 año (μg/kg/día) | Resto edades (μg/kg/día) | |||
| CROMO | 0,2 | 0,2 | 0,2 (máx. 5 μg/día) | ||
| HIERRO | 100 | 100 | 1 mg/día | ||
| COBREa | 20 | 20 | 20 (máx. 300 μg/día) | ||
| MANGANESOa | 1 | 1 | 1 (máx. 50 μg/día) | ||
| SELENIO | 2 | 2 | 2 (máx. 30 μg/día) | ||
| CINCb | 400 | 250 < 3meses 100 > 3meses | 50 (máx. 5000 μg/día) | ||
| MOLIBDENO | 0.25 | 0.25 | 0.25 (máx 5 μg /d) | ||
| YODO | 1 | 1 | 1 (máx 50 μg /d) | ||
| a En pacientes con colestasis hay riesgo de acumulación de cobre y manganeso, por lo que se aconseja realizar una reducción en su aporte. | |||||
| b Al margen de las necesidades basales, se requieren aportes adicionales de cinc en situaciones de pérdidas intestinales, a dosis de 2 mg/kg de pérdidas, hasta un máximo de 6-12 mg/día. | |||||
| En pacientes con enfermedades renales se deben limitar los aportes de: selenio, molibdeno y cromo. | |||||
| Requerimientos vitaminas | |||||
| Vitaminas liposolubles | |||||
| RNPT (DOSIS/KG/DÍA) | Lactante-niños (DOSIS DÍA) | ||||
| A (retinol) | 700-1.500 UI | 1.500-2.300 UI | |||
| D (ergocalcoferol) | 40-160 UI | 400 UI | |||
| E (alfatocoferol) | 3,5 mg | 7-10 mg | |||
| K (filoquinona) | 8-10 μg | 50-200 μg | |||
| Vitaminas hidrosolubles | |||||
| Tiamina (B1) | 0,35-0,5 mg | 1,2 mg | |||
| Riboflavina (B2) | 0,15-0,2 mg | 1,4 mg | |||
| Piridoxina (B6) | 0,15-0,2 mg | 1 mg | |||
| Cianocobalamina (B12) | 0,3 μg | 1 μg | |||
| C (Ácido ascórbico) | 15-25 mg | 80-100 mg | |||
| Ácido fólico | 56 μg | 140 μg | |||
| Niacina | 4-6,8 mg | 17 mg | |||
| Ácido pantoténico | 1-2 mg | 5 mg | |||
| Biotina | 5-8 μg | 20 μg | |||
REQUERIMIENTOS HÍDRICOS: En pacientes pediátricos el programa tendrá en cuenta si el paciente ha nacido a término (RNT) o pretérmino (RNPT), de forma que los aportes hídricos se ajustarán a su fase de adaptación postnatal. Se contemplan tres momentos especiales (ver requerimientos tabla adjunta):
| |||||
| FT | FI | FE | |||
| RNT(ml/kg/día) | 60-120 | 140 | 140-170 | ||
| RNPT(ml/kg/día) > 1500 g | 60-80 | 140-160 | 140-160 | ||
| RNPT(ml/kg/día) < 1500 g | 80-90 | 140-180 | 140-180 | ||
| A PARTIR DEL 1° MES DE EDAD | |||||
| 1° MES-AÑO /kg/día (más pérdidas) | 100 mL | ||||
| 1° AÑO-12 AÑOS/kg/día (más pérdidas) | < 10 kg | 100 ml/kg | |||
| 10-20 kg | 1000 ml (primeros 10 kg) + 50 ml/kg por encima de los 10 kg | ||||
| > 20 kg | 1500 ml (primeros 20 kg) + 20 ml/kg por encima de los 20 kg (máx 2000-2500 mL/24h) | ||||
RNPT: Recién nacido pretérmino
RNT: Recién nacido a término
Vías de administración
| VíA | TIPO | DURACION PREVISTA | PEDIATRIA | ADULTO |
|---|---|---|---|---|
| YUGULAR INTERNA | YUGULAR INTERNA | |||
| YUGULAR EXTERNA | SUBCLAVIA | |||
| SUBCLAVIA | FEMORAL | |||
| CENTRAL | 7-28 DÍAS | HUMERAL | ||
| PARENTERAL | HUMBILICAL | |||
| FEMORAL | ||||
| SAFENA | ||||
| PERIFÉRICA < 800 mOsm/L | < 7 DÍAS | BASÍLICA CEFÁLICA | ||
| SONDA OROGASTRICA | ||||
| SONDA NASOGASTRICA | ||||
| SONDAS | < 28 DÍAS | SONDA NASODUODENAL | ||
| ENTERAL | SONDA NASOYEYUNAL | |||
| GASTROSTOMIA | ||||
| OSTOMÍAS | >28 DÍAS | YEYUNOSTOMIA | ||
| GASTROYEYUNOSTOMIA | ||||
Tras establecer el plan de cuidados, se procederá a la validación de la prescripción por parte del farmacéutico.
En el caso específico de las nutriciones parenterales, de acuerdo con las presentaciones de las nutriciones tricamerales, bicamerales y sueros incluidos en la base de datos del programa junto con las condiciones de estabilidad que debe recoger toda preparación (Tabla 9)31–33, el programa genera automáticamente la preparación que se ajusta más a dichas condiciones. Si por criterio clínico se decidiese modificar dicha elaboración, ésta puede ser chequeada de nuevo con el fin de determinar su estabilidad físico-química. En caso de existir alguna incompatibilidad físico-química el programa alerta mediante las alarmas pertinentes.
Estabilidad físico-química de las preparaciones
| MACRONUTRIENTES | |||||
|---|---|---|---|---|---|
| AMINOÁCIDOS (%) 2-may | GLUCOSA (%) may-34 | LÍPIDOS (%) 1,5-5 | |||
| ELECTROLITOS (mezclas ternarias) | |||||
| POTASIO | 100 mEq/l | SODIO | 180 mEq/l | MAGNESIO | 15 mEq/l |
| CALCIO (mEq/l) + FOSFATO (mmol/l) | ≤30 mEq/l | ||||
| ACETATO | 85 mEq/l (no incluye acetato de las soluciones de aminoácidos). | ||||
| COMPATIBILIDAD CALCIO/FOSFATO | |||||
| En función del volumen en el que se añade el calcio y de la naturaleza química de los elementos. | |||||
| NATURALEZA QUÍMICA CALCIO/FOSFATO INORGÁNICA | |||||
| LÍMITES | |||||
| AMINOÁCIDOS (%) | > 1,5 | 1-1,5 | < 1 | ||
| CALCIO (mEq/l) + FÓSFORO (mmol/l) | ≤30 | ≤20 | Sólo CALCIO o sólo FÓSFORO | ||
| NATURALEZA QUÍMICA FOSFATO ORGÁNICA (glicerofosfato sódico) | |||||
| AMINOÁCIDOS (%) | < 0,5 | 0,5-1,25 | 1,25-2,5 | >2,5 | |
| CALCIO (mmol/l) | Sólo CALCIO | 20 | 35 | 56 | |
| FOSFATO (mmol/l) | o sólo FÓSFORO | 25 | 30 | 48 | |
Una vez seleccionada la preparación a elaborar se generan las correspondientes hojas de preparación y etiquetas, con el “modus operandi”, donde se indican: datos de identificación del paciente, localización del paciente (cama, servicio), fecha de elabor ación, volúmenes de las distintas soluciones que permiten establecer el orden de adición a la bolsa, identificación de los productos por lotes, códigos datamatrix para garantizar la identificación de productos y trazabilidad, firma del farmacéutico responsable, firma del personal elaborador, lote de elaboración y número de referencia.
Por último, el personal de enfermería valida la administración identificando el paciente y la preparación mediante la lectura de los códigos de barras (pulsera del paciente) y datamatrix (nutrición), respectivamente, permitiendo determinar si tanto la preparación como el paciente son los correctos.
Además se pueden notificar las complicaciones que pueden aparecer durante la administración documentando las causas y las acciones realizadas (Tabla 10).
Administración
| COMPLICACIONES | CAUSAS | ACTUACIONES |
|---|---|---|
| MECÁNICAS | ||
| Erosiones | Inadecuada colocación de la sonda | Comprobar/Modificar la colocación de la sonda |
| Calibre inapropiado de la sonda | Utilizar sondas de calibre inferior | |
| Aspiración | Inadecuada colocación de la sonda | Comprobar/Modificar la colocación de la sonda |
| Calibre inapropiado de la sonda | Utilizar sondas de calibre inferior | |
| Posición inadecuada del paciente | Elevar más de 30’ el cabecera de la cama o paciente semisentado | |
| Obstrucciones | Mantenimiento inadecuado | Limpiar adecuadamente la sonda |
| Textura no apropiada de los productos | Evitar grumos en el alimento. | |
| Irritación de la piel en ostomías | Pérdida de alimentos o jugos digestivos | Medidas higiénicas |
| GASTROINTESTINALES | ||
| Molestias abdominales | Exceso de velocidad en la infusión | Disminuir el ritmo de los bolos o administración continua |
| Temperatura inadecuada de las fórmulas | Administrar la dieta a temperatura ambiente | |
| Problemas de malabsorción | Eliminar de la dieta el componente malabsorbido | |
| Náuseas y vómitos | Exceso de velocidad en la infusión | Disminuir el ritmo de los bolos o administración continua |
| Exceso de contenido en grasas | Disminuir el aporte graso, <30-40% del total de calorías. | |
| Retención gástrica | Administrar fórmulas isotónicas. Valorar uso de antieméticos | |
| Diarrea | Contaminación del preparado | Medidas higiénicas y adecuada conservación dietas |
| Medicación concomitante (ej. Antibióticos, antiácidos con Mg) | Modificar la medicación, si es posible. En caso contrario, administrar antidiarreicos | |
| Hipoalbuminemia grave | Administrar fórmulas isotónicas | |
| Exceso de fibra en la dieta | Disminuir el aporte de fibra en la dicta o modificar el tipo de fibra | |
| Inadecuada velocidad de infusión | Disminuir el ritmo de los bolos o administración continua | |
| Hiperosmolaridad de la fórmula | Reducir la osmolaridad de la fórmula. Valorar antidiarreicos | |
| Malabsorción o intolerancia a alguno de los componentes de la dieta | Eliminar de la dieta el componente malabsorbido o no tolerado (ej. Fórmulas sin lactosa) | |
| Temperatura inadecuada de la fórmula | Administrar la dieta a temperatura ambiente | |
| Sonda rebasa el píloro | Comprobar/Modificar colocación de la sonda | |
| Estreñimiento | Impactación de fecalomas | El Tacto rectal y extracción |
| Escaso aporte de fibra | Administrar dieta enriquecida en fibra | |
| Falta de actividad física | Si es posible, incrementar el ejercicio físico (Deambulación) | |
| Medicación concomitante | Modificar la medicación, si es posible | |
| Falta de hidratación adecuada | Incrementar el aporte de líquidos | |
| INFECCIOSAS | ||
| Neumonía | Por aspiración | Verificar colocación y calibre de la sonda |
| Otras infecciones | Insuficientes medidas higiénicas del material o de las dietas | Adoptar medidas higiénicas (limpieza personal y de material) Controlar la adecuada conservación de las dietas |
| Inadecuada conservación de las dietas | ||
| METABÓLICAS | ||
| Hiperglucemia | Procesos asociados, ej. Diabetes “Rebote” por la realimentación | Ajustar aporte en función de la glucemia. Valorar fármacos Control de la glucemia hasta su estabilización |
| Hipoglucemia | Retirada brusca de la nutrición | Retirada paulatina de la dieta. Aporte de glucosa |
| Deshidratación | Insuficiente aporte hídrico Excesiva pérdida de líquidos Utilización de dietas hipertónicas | Aporte hídrico ajustado según balance hídrico, control de peso, de osmolalidad, de urea y de creatinina. Aporte hídrico adecuado y vigilancia de pérdidas anormales. Aporte hídrico adecuado y administración de fórmulas isotónicas |
| Niveles inadecuados de electrolitos | Composición inadecuada de la dieta Exceso de pérdidas (ej. diarrea) Medicación concomitante (especialmente insulina, diuréticos) | Controlar niveles en sangre y adecuar la composición de la dieta Tratar la causa del exceso de pérdidas Replantear el tratamiento, si es posible. Controlar niveles séricos |
| PSICOSOCIALES | ||
| Dificultades de adaptación a la situación | Cambio de imagen corporal Incapacidad de degustar alimentos | Información. Diálogo. Apoyo psicológico |
Para la monitorización del tratamiento se incluyó en el programa un apartado de recogida de constantes vitales (tensión sistólica, tensión diastólica, temperatura,frecuencia cardíaca, saturación parcial de oxígeno), balance hídrico y registro de analíticas.
En cuanto a la finalización del tratamiento se determinó como posibles causas las siguientes opciones: alta hospitalaria, exitus, transición oral o enteral, pérdida de vía, indisposición, empeoramiento del estado u otros. En este último caso existe un apartado de notas para poder especificar qué causa ha sido el motivo de la finalización del tratamiento.
Para la obtención de los indicadores de calidad, se optó por crear un módulo para realizar consultas a la base de datos del aplicativo para generar los indicadores que se estimen oportunos, ya que permite relacionar todas las variables recogidas en subprocesos así como todas las ayudas a la prescripción implementadas.
ResultadosEl programa informático desarrollado se caracteriza por: - Permitir el cribado nutricional de todos los pacientes, desde el ingreso hasta el alta hospitalaria, siendo la monitorización 24 horas los 365 días del año con cribados seriados hasta el alta hospitalaria.
- -
Incorporar sistemas de cribado nutricional automáticos (FILNUT) (Tabla 2), y de entrevista (NRS 2002 y PYMS) (Tablas 1 y 3), haciendo más eficiente el proceso.
- -
Incorporar el método indirecto de determinación de la altura de BAPEN, de interés sobre todo en pacientes encamados.
- -
Permitir el cálculo de los requerimientos energéticos en función del estrés metabólico y las características del paciente (parálisis cerebral, embarazo, bajo peso…) (Tablas 6 y 7).
- -
Proveer de diferentes ayudas a la prescripción en función de la evolución del paciente.
- -
Incluir un sistema de trazabilidad de las materias primas y las preparaciones estériles elaboradas, mediante sistema de codificación datamatrix así como de los pacientes mediante la impresión de pulseras identificativas.
- -
Permitir un control de estabilidad de las preparaciones de acuerdo con la información incluida en la base de datos del aplicativo (Tabla 9).
- -
Prevenir errores en la elaboración de las nutriciones parenterales al generar la hoja de preparación con el orden correcto de aditivación de los componentes, evitando la inestabilidad de la misma.
- -
Documentar las complicaciones del proceso de administración, orientando al personal de enfermería sobre las posibles causas, y ofreciendo las actuaciones a seguir para corregirlas (Tabla 10).
- -
Prevenir errores de administración al permitir la impresión de pulseras de pacientes controlando el proceso mediante la lectura del código datamatrix de la muestra y el código de barras de la pulsera del paciente.
- -
Incorporar un módulo estadístico que permite extraer toda la información necesaria para elaborar el cuadro de mandos de una unidad de nutrición, de acuerdo con los estándares publicados.
- -
Contemplar la multidisciplinaria de los procesos, definiendo diferentes accesos de acuerdo con el perfil del usuario: médico, farmacéutico, dietista, enfermería unidad y enfermería farmacia.
- -
Generar informes de alta con el resumen de todas las complicaciones presentadas y las respectivas actuaciones realizadas, junto con el resultado del soporte nutricional especializado.
- -
Permitir una integración con la historia clínica electrónica (balance hídrico y constantes vitales), censo hospitalario y laboratorio de análisis clínicos.
En cuanto a las integraciones, en el caso específico del hospital Comarcal de Inca, se utilizan el conjunto de estándares para el intercambio electrónico de información clínica HL7 versión 2.5. Se integra con la historia clínica del centro: constantes vitales (tensión sistólica, tensión diastólica, temperatura, frecuencia cardíaca, saturación parcial de oxígeno), servicio análisis clínicos (hemograma y bioquímica) y de admisión (ingreso, traslado y alta hospitalaria).
DiscusiónEl Instituto de Medicina (IOM) propone, como objetivos de calidad en la asistencia sanitaria, la seguridad del paciente, efectividad, eficiencia, orientación al paciente, oportunidad y equidad. Estos objetivos se corresponden o se relacionan, respectivamente, con los procesos del soporte nutricional especializado que se han incorporado en el aplicativo: cribado nutricional, formulación de las preparaciones, valoración del estado nutricional y plan de cuidados nutricionales, gestión y dispensación13.
En la literatura científica existen diferentes sistemas de cribado nutricional automatizados para pacientes adultos, CONUT y FILNUT, los cuales permiten la detección sistemática e identificación precoz de pacientes desnutridos al ingreso hospitalario y durante su hospitalización. En el aplicativo desarrollado se ha implementado el sistema FILNUT debido a que al analizar en el ingreso del paciente la relación existente entre el riesgo nutricional detectado por este método de cribado, la mortalidad, estancia hospitalaria y la tasa de reingresos, presentó una sensibilidad del 92,3%, un valor predictivo positivo del 94,1%, una especificidad del 91,2%, y una concordancia (índice kappa, estimado frente a un estándar de oro de valoración nutricional) de 0,83. Además, cabe destacar que entre los positivos a FILNUT quedan incluidos aquellos pacientes que cumplen los criterios para CONUT27,34.
De acuerdo con los resultados de nuestro artículo debemos tener en cuenta que en aquellos casos en los cuales no se pueda realizar la integración con el laboratorio de análisis clínicos del hospital, el sistema de cribado FILNUT pierde su ventaja, al tener que introducir manualmente los resultados de los parámetros bioquímicos. Por tanto, en estos casos es más eficiente el sistema de entrevista NRS-2002. En aquellos casos en que se puedan realizar las integraciones con el servicio de admisión y el laboratorio de análisis clínicos, se procederá de acuerdo con lo comentado el epígrafe métodos.
En el paciente pediátrico no existe ningún filtro automatizado basado en parámetros bioquímicos ya que éstos son mejores marcadores de inflamación o infección que de desnutrición, de tal forma que no reflejan el estado nutricional del paciente en caso de enfermedad35. Por ello, el cribado del paciente pediátrico se realiza mediante el sistema de entrevista PYMS, que considera como predictores de malnutrición el índice de masa corporal, la pérdida de peso reciente, la disminución de la ingesta en la última semana y cualquier otra condición o situación que pueda modificar el estado nutricional del paciente en la próxima semana, siendo estos criterios requisitos de los sistemas de cribado de la guía ESPEN28.
Para determinar el estado nutricional del paciente se ha adoptado el Documento SENPE-SEDOM sobre la codificación de la desnutrición hospitalaria para los pacientes adultos. Dicho consenso se ha adaptado al paciente pediátrico en cuanto a los parámetros bioquímicos y antropométricos36. Recientemente, se ha propuesto la siguiente clasificación para el diagnóstico nutricional en la práctica clínica: Desnutrición asociada a la inanición, cuando hay inanición crónica sin inflamación; desnutrición asociada a la enfermedad crónica, cuando la inflamación es crónica y de intensidad leve o moderada; y desnutrición asociada a la enfermedad aguda o al estrés, cuando la inflamación es aguda o de intensidad grave. Esta clasificación no ha sido tenida en cuenta ya que la primera versión del aplicativo ya estaba en producción, de ahí que será tenida en cuenta para sucesivas versiones37.
De acuerdo con el Institute for Safe Medicine Practices (ISMP) y como medida clave para reducir el riesgo de errores, el aplicativo protocoliza mediante un sistema de alarmas, al igual que la gran mayoría de los software actualmente comercializados en nuestro entorno, el rango de cantidades máximas y mínimas de nutrientes y aditivos de las mezclas de nutrición parenteral que garantizan su estabilidad y compatibilidad. Esta estandarización afectará además a aspectos clínicos como son los límites en los aportes de macronutrientes o el balance calorías/ proteínas que facilitan la validación del tratamiento ,por parte del farmacéutico permitiéndole comprobar que las nutriciones parenterales que prepara son coherentes y se adaptan a las necesidades del paciente38.
Finalmente cabe destacar que no se implementaron un módulo cerrado con los indicadores de calidad publicados hasta la fecha ya que dicho aplicativo de per se permite cumplir con algunos de ellos como por ejemplo cribado universal de toda la población hospitalaria, codificación del diagnóstico nutricional de los pacientes.
Para hacer más versátil la aplicación toda la información contenida en la misma puede ser explotada mediante la generación de tablas dinámicas combinandotodas las variables de los diferentes subprocesos, a modo de ejemplo se puede determinar la relación de pacientes en riesgo nutricional y grado de desnutrición, prevalencia de la desnutrición, días de soporte nutricional en función del grado de desnutrición etcétera.
Todos estos datos pueden ser exportados en formato excel, csv y pdf para poderlos tratar con otros sistemas de información para su posterior tratamiento si así se requiere.
En definitiva, con este aplicativo se introduce el concepto del control de calidad por procesos en el soporte nutricional especializado con el objetivo de determinar puntos de oportunidad de mejora así como la evaluación del resultado del mismo.
Una vez desarrollado el aplicativo se hace necesaria la puesta en producción del mismo para determinar si la estandarización del soporte nutricional especializado con dicha herramienta se traduce en una mejora en los estándares de calidad, y para evaluar sus limitaciones.