analizar el papel desempeñado por el farmacéutico clínico y su impacto en el ámbito de los programas de optimización de antimicrobianos ante la sospecha de alergia a antibióticos beta-lactámicos.
Métodose realizaron 2 búsquedas bibliográficas independientes. Se encontraron un total de 35 artículos incluyéndose 12. Se analizaron los artículos incluidos y se recogieron variables de eficacia, seguridad y aplicabilidad de herramientas de evaluación a pacientes con sospecha de alergia a beta-lactámicos. Además, se analizó la variación en el consumo y en el perfil de prescripción de antibióticos alternativos.
Resultadoslos estudios seleccionados analizaron cuestionarios, desetiquetado, test intradérmicos y pruebas de provocación oral realizados por farmacéuticos.
Se hallaron diferencias significativas en la variable principal de eficacia en 4 estudios incluidos a favor de la intervención farmacéutica. En un estudio cuasi experimental, la utilización de cefazolina aumentó tras la intervención farmacéutica (65 vs. 28%; p < 0,01). En otro estudio cuasi experimental, la dosis diaria definida media de aztreonam y la media de días de terapéutica por 1.000 pacientes/día disminuyeron (21,23 vs. 9,05; p < 0,01) y (8,79–4,24; p = 0,016), pre y postintervención, respectivamente, aumentando las desescaladas antibióticas (p ≤ 0,01). En otro estudio, disminuyó la prescripción de antibióticos de uso restringido (42,5 vs. 17,9%; p < 0,01) y en otro, la utilización de antibióticos profilácticos prequirúrgicos alternativos a cefazolina (81,9 vs. 55,9%; p < 0,01).
En otro estudio, el tiempo medio por entrevista fue de 5,2 minutos por paciente. No se reportaron eventos adversos en ningún estudio.
Conclusionesla intervención del farmacéutico en la evaluación del paciente con sospecha de alergia a beta-lactámicos resulta eficaz, segura y aplicable a la práctica clínica. La estandarización de protocolos para esclarecer la historia de alergias y desarrollo de herramientas de evaluación constituyen un sencillo cribado para realizar el desetiquetado o referenciar al servicio de inmunoalergología, mejorando el uso de penicilinas y reduciendo la necesidad de antibióticos de segunda línea. Son necesarios más estudios para uniformizar la realización de tests de desensibilización por farmacéuticos.
Sin embargo, a pesar de estos resultados, la implicación y liderazgo del farmacéutico en esta área es escasa y constituye un desafío futuro para la profesión.
To analyze the role played by the clinical pharmacist and its impact in antibiotic stewardship facing suspected allergy to beta-lactam antibiotics.
MethodWe performed two different independent bibliographic searches. A total of 35 articles were found, and the final number included in the study was 12. We analysed the articles and collected variables of efficacy, safety and applicability of evaluation tools applied to patients with suspected allergy to beta-lactams. Also, the variation in the consumption and prescription profile of alternative antibiotics was analyzed.
ResultsThe selected studies analysed questionnaires, allergy delabeling, intradermal tests and oral challenge tests performed by pharmacists.
Significant differences in the efficacy endpoint were found in 4 studies in favour of pharmaceutical intervention. In the study of Kwiatkowski et al, cefazolin use increased in surgical patients after pharmacist intervention (65 vs. 28%; p < 0.01). In a quasi-experimental study, the mean defined daily dose of aztreonam and the mean days of therapy per 1000 patients/day decreased (21.23 vs 9.05, p <0.01) and (8.79–4.24, p = 0.016), pre and post-intervention, respectively, increasing antibiotic de-escalations (p ≤ 0.01). In another quasi-experimental study, the prescription of restricted-use antibiotics decreased (42.5% vs. 17.9%, p < 0.01) and the use of pre-surgical prophylactic antibiotics alternative to cefazolin (81.9% vs 55.9%, p<0.01) in another study.
Other study showed that the mean time per interview was 5.2 minutes per patient. No adverse events were reported in any study.
ConclusionThe pharmacist intervention in the evaluation of the patient with suspected allergy to beta-lactams is effective, safe and feasible to implement on daily clinical practice. The standardization of protocols to clarify the history of allergies and development of evaluation tools represent simple screenings to perform delabelling or refer to the Immunoallergology service, improving penicilins use and reducing the need for second line antibiotics.
More studies are needed to standardize the desensitization tests made by pharmacists.
However, despite these results, the involvement and leadership of the pharmacist in this area is limited and constitutes a future challenge for the profession.
Los antibióticos beta-lactámicos son los de uso más frecuente en la enfermedad infecciosa con base en su eficacia, espectro y seguridad. En ocasiones, su prescripción está limitada por las resistencias bacterianas y por la aparición de reacciones adversas, entre las que destacan especialmente las de hipersensibilidad. La alergia a la penicilina es la más común entre los casos descritos de alergia a medicamentos1.
Cerca del 10% de los pacientes reportan historial de alergia; sin embargo, se estima que menos del 1% de la población es realmente alérgica. Según la Academia Americana de Alergia, Asma e Inmunologías, el 80% de los pacientes con alergias a penicilinas mediadas por anticuerpos IgE pierden la sensibilidad transcurridos 10 años2.
Por otro lado, la tasa de reactividad cruzada entre penicilinas y cefalosporinas es menor del 1%3.
A pesar de estos datos, en muchas ocasiones se evita por completo la terapia con beta-lactámicos en pacientes sin alergias reales o con reacciones leves.
De mayor relevancia son las reacciones alérgicas mediadas por IgE (reacciones alérgicas tipo I), que suelen ocurrir dentro de la primera hora de administración del medicamento. Sus síntomas incluyen urticaria, angioedema, falta de aire, sibilancias y anafilaxia. Otras reacciones severas, que no están mediadas por IgE (reacciones alérgicas tardías, tipo II, III y IV), incluyen síndrome de Stevens-Johnson, necrólisis epidérmica tóxica, nefritis intersticial, anemia hemolítica, enfermedad del suero aguda (serum sickness) o síndrome de sensibilidad a fármacos con eosinofilia y síntomas sistémicos (DRESS, en inglés).
Evitar un antibiótico beta-lactámico innecesariamente constituye una preocupación por varios aspectos: implica el uso de antibióticos potencialmente menos eficaces (por ejemplo, la vancomicina es menos eficaz contra Staphylococcus aureus meticilin sensible que la cloxacilina) y promueve el uso de agentes con un espectro más amplio y con mayor riesgo de desarrollo de resistencia, con una toxicidad potencialmente mayor (por ejemplo: selección de Clostridioides difficile, (CD) y Staphylococcus Aureus resistente a la meticilina). Además, las alergias mal caracterizadas están relacionadas con retrasos en la primera administración de la terapia antibiótica, mayores tasas de rehospitalización y hospitalizaciones prolongadas, mayor riesgo de infección en el lecho quirúrgico, aumento de reacciones adversas, mortalidad y mayores costes asociados4.
El farmacéutico como elemento de los programas de optimización de antimicrobianos (PROA)La resistencia a antibióticos es un problema de salud pública a nivel mundial. Se estima que anualmente en Estados Unidos ocurren 2,8 millones de infecciones causadas por bacterias resistentes, ocasionando sobre 35.000 muertes5. Los datos relativos a la Unión Europea muestran que cada año ocurren 670.000 infecciones por bacterias resistentes, ocasionando 33.000 óbitos6.
Se ha encontrado que el factor de riesgo modificable más importante para el desarrollo de resistencia es el uso inapropiado de antibióticos. Por lo tanto, es fundamental promover el uso adecuado de antibióticos en todos los escenarios clínicos y el rol del farmacéutico es vital para lograrlo. Los PROA consisten en un conjunto de estrategias dirigidas a promover el uso apropiado de antibióticos. Estas estrategias buscan optimizar la efectividad de los antibióticos, minimizar eventos adversos y toxicidades asociadas a su utilización, limitar el desarrollo de bacterias resistentes y reducir costes innecesarios asociados al uso excesivo e inapropiado de antibióticos7–10.
Organizaciones farmacéuticas como la American Society of Health System Pharmacists (ASHP) y Society of Infectious Diseases Pharmacists (SIDP) han publicado guías sobre el rol del farmacéutico en estos programas a nivel hospitalario y ambulatorio, respectivamente11–13.
Actualmente, los protocolos de actuación en caso de sospecha de alergia a los beta-lactámicos constituyen una prioridad para los grupos de control de infección hospitalarios, en donde, a pesar de la naturaleza multidisciplinar de los mismos, la intervención del farmacéutico no está muy desarrollada en este contexto.
El objetivo principal de esta revisión es analizar el papel desempeñado por el farmacéutico clínico y su impacto en el ámbito de los PROA ante la sospecha de alergia a antibióticos beta-lactámicos.
Material y métodosBúsqueda bibliográficaSe realizó una búsqueda bibliográfica por términos MeSH en las principales bases de datos biomédicas: MEDLINE (PubMed), EMBASE. Las estrategias y términos utilizados en las búsquedas se detallan a continuación: («beta-Lactams»[Mesh] AND «Hypersensitivity»[Mesh]) AND «Pharmacists»[Mesh]) AND/OR «Antimicrobial Stewardship»[Mesh]. El horizonte temporal establecido fueron los últimos 5 años: 2018–2022. Independientemente se solicitó una búsqueda bibliográfica al Centro de Información del Medicamento de la Ordem Dos Farmacêuticos de Portugal (CIM-OF).
Selección de estudiosLa selección de los estudios se basó en los siguientes criterios:
Criterios de inclusión: a) estudios que describieran el papel desempeñado por el farmacéutico clínico en el ámbito de los PROA ante la sospecha de alergia a antibióticos beta-lactámicos; b) que evaluaran los parámetros clínicos de los pacientes en términos de eficacia y/o seguridad; c) que analizaran viabilidad de los procedimientos implementados por el farmacéutico; d) que describieran información acerca de cambios en el patrón de utilización de antibióticos, coste, estancia hospitalaria y/o percepción de los pacientes.
Criterios de exclusión: se excluyeron aquellos estudios que: a) no contaban con la participación del farmacéutico; b) aquellos en los que se analizaban exclusivamente diferencias en el patrón de prescripción de antibióticos; c) aquellos en los que se analizaban solo costes; d) no estaban en lengua española, portuguesa o inglesa, y e) los que no se pudieron localizar los textos completos. Entre los estudios encuadrados en los 2 últimos criterios de exclusión (d y e) no hay ningún estudio que analice o describa el papel desempeñado por el farmacéutico clínico en el ámbito de los PROA ante la sospecha de alergia a antibióticos beta-lactámicos.
Análisis de los datosUna vez seleccionados los estudios a incluir basado en los criterios anteriores, un equipo formado por 2 investigadores analizaron de forma independiente los mismos, recogiéndose las siguientes variables: país de publicación, diseño, intervención farmacéutica, muestra de pacientes y resultados de la intervención (variables de eficacia, seguridad y/u otras como aplicabilidad o análisis de consumos).
Posteriormente se ponen en común por consenso y, si existe desacuerdo, participa un tercer investigador.
Se realizó el análisis y selección de los estudios tomando como referencia la guía Prisma 202014.
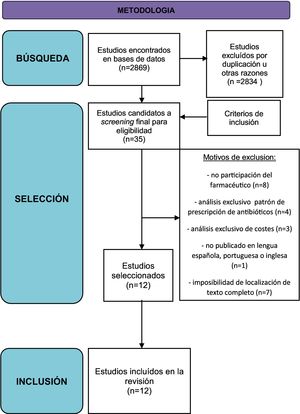
ResultadosEstudios incluidos: se identificaron 35 estudios que cumplían los criterios de búsqueda. Teniendo en cuenta los criterios de inclusión y exclusión, se seleccionaron finalmente 12 estudios. El proceso de selección de estudios se encuentra reflejado en la figura 1.
Se excluyeron 8 estudios por no contar con la participación del farmacéutico, 4 por analizar exclusivamente diferencias en el patrón de prescripción de antibióticos, 3 por analizar solo costes, uno por no encontrarse en lengua española, portuguesa o inglesa y 7 por no conseguir localizarse los textos completos.
De los estudios incluidos, 11 eran estudios cuasi experimentales y uno era un estudio observacional.
Los resultados de los estudios se encuentran recogidos en la tabla 1.
Resultados de los estudios
| Autor, año, país | Diseño | Intervención farmacéutica | n (muestra) | Desetiquetado Directo | Provocación oral/Test intradérmico | Referencia a inmunoalergología (IA) | Consumosdeantibióticos (AB) | Seguridad |
|---|---|---|---|---|---|---|---|---|
| Tanya du Plessis et al.15J Antimicrob Chemother2018 (Nueva Zelanda) | Cuasi experimental | Cuestionario estructurado, desetiquetado y provocación oral | 250adultos,ingresados | 64%, de los cuales 50% ya habían tolerado un antibiótico que contenía penicilina | 12,4% | 20%(47% con alergia confirmada) | N/A | Ningún efecto adverso notificado en 98% de los pacientes después de un año de seguimiento |
| Mitchell et al.16Fed Pract. 2021(EE. UU.) | Observacional | Cuestionario estructurado, desetiquetado y provocación oral | 278adultos, ingresados | 22% | 8,6% | N/A | N/A | N/A |
| Harmon S et al.17Hospital Pharmacy2020 (EE. UU.) | Cuasi experimental | Test intradérmico | 31adultos, ingresados | N/A | 96% | N/A | Ahorro medio diario de US $74,75 por paciente | 2 pacientes con efectos adversos tras el test intradérmico: erupción cutánea y reacción local |
| Turner NA et al.18JAMA,2021 (EE. UU.) | Cuasi experimental: caso control | Cuestionario estructurado, desetiquetado, administración e interpretación de test cutáneos de penicilina y referenciación a IA | 273adultos, ingresados | 17,2% | 68% | 0,4% | Reducción en AB de grupos alternativos y con alto riesgo de infección por CD tras aplicar el cuestionario (RR 0,87; 95% CI, 0,79–0,97); (0,91; 95% CI, 0,85–0,98) respectivamente | N/A |
| Mann KL et al.19J Antimicrob Chemother 2019(EE. UU.) | Cuasi experimental | Cuestionario estructurado, desetiquetado directo | 175adultos | 1,1%(a demanda del propio paciente)+ 13% | N/A | N/A | N/A | No hubo notificación de efectos adversos |
| Clark KE et al.20Journal of Pharmacy Practice2019 (EE. UU.) | Cuasi experimental | Cuestionario estructurado | 95 adultos preintervención vs. 65 post | N/A | N/A | N/A | Disminución de DDD aztreonam/1.000 pacientes/día:21,23 vs. 9,05 p = 0,003) | No hubo notificación de efectos adversos |
| Devchand M et al.21J Antimicrob Chemother2019 (Australia) | Cuasi experimental | Cuestionario estructurado, desetiquetado, provocación oral y test cutáneos | 106adultos, ingresados | 13% | 18,8% (oral)3,8% (cutáneos) | 25,4% | N/A | Un paciente notificó rash cutáneo tardio a amoxicilina tras provocación oral, con nuevo registro en la historia de alergias |
| Vaisman et al.22J Antimicrob Chemother2017 (Canadá) | Cuasi experimental | Cuestionario estructurado | 485 adultos, previo a cirugía electiva | N/A | N/A | N/A | Disminución de AB alternativos 81,9% vs. 55,9%(p = 0,001) pre- postintervención | No hubo notificación de efectos adversos tras administración de cefazolina |
| Ham Y et al.23Allergy and Asthma Proceedings2021 (EE. UU.) | Cuasi experimental | Cuestionario estructurado y provocación oral | 50adultos, ingresados | 40% | 56% | N/A | N/A | 2 pacientes con efectos adversos leves tras provocación oral |
| Louden NJ et al.24J PPT, 2021(EE. UU.) | Cuasi experimental | Cuestionario estructurado, desetiquetado directo y referenciación a IA | 11Pacientes pediátricos | 18% | N/A | 82% | N/A | N/A |
| Kwiatkowski S et al.25Am J Health Syst Pharm2021 (EE. UU.) | Cuasi experimental: caso control | Cuestionario telefónico previo a cirugía electiva | 87adultos | N/A | N/A | N/A | Utilización de cefazolina aumentó (p = 0,001) 65% vs. 28% | N/A |
| Song YC et al.262021(EE. UU.) | Cuasi experimental | Cuestionario estructurado | 66adultos, ingresados | 18% | N/A | N/A | N/A | N/A |
N/A: No aplicable / sin mención del resultado.
En 11 estudios el farmacéutico realizó entrevista al paciente con sospecha de alergia a beta-lactámicos, recogiéndose la historia completa de la reacción alérgica y evaluación de la misma a través de cuestionarios estandarizados15,16,27 y en un estudio fueron realizados test cutáneos sin entrevista previa17.
Las intervenciones realizadas, tras la entrevista fueron: desetiquetado directo (en 6 estudios), realización de pruebas para provocación oral (en 4), realización de tests epicutáneos/intradérmicos para pacientes hospitalizados o ambulatorios (en 3) y referenciación al servicio de inmunoalergología (en 2).
En 10 estudios, se realizaron intervenciones en pacientes hospitalizados con registro de alergia a beta-lactámicos. Solo 2 se realizaron a pacientes que aún no habían ingresado antes de procedimientos quirúrgicos electivos y en solo un estudio se incluyeron pacientes pediátricos.
Identificación de pacientes candidatos a entrevistaLos candidatos eran identificados a través del registro de sospecha de reacción alérgica a beta-lactámicos existente en la historia clínica electrónica.
Algunos autores refieren la creación por parte del farmacéutico de una herramienta automatizada que facilitase la búsqueda diaria de estos pacientes16,17,19,26.
En el estudio de Kwiatkowsk et al.25 se incluyeron pacientes con cirugía electiva que tenían registro de alergia y que tenían previsión de utilización de un antibiótico beta-lactámico en la profilaxis quirúrgica. Los pacientes con criterios eran informados de la realización del cuestionario una semana antes de la consulta de anestesia preoperatoria.
Cuestionarios, estratificación del riesgo y formación previaLos cuestionarios estructurados referidos en los estudios detallaban sobre el antibiótico implicado, características y tiempo desde que sucedió la reacción y posibles administraciones subsecuentes de antibióticos beta-lactámicos que permitiesen asumir que era bien tolerado16,19–21,24,26.
La estratificación del riesgo subsecuente se realizaba en 3 o 4 niveles: sin riesgo, bajo, moderado y alto. Cada categoría se asociaba a una actuación recomendada: desetiquetado, provocación oral, test cutáneo seguido de provocación o evitar la utilización de beta-lactámicos.
El resultado del cuestionario, así como la recomendación eran registrados en la historia clínica electrónica16,19–21,24,26.
Louden et al.24 crearon una herramienta informática que retiraba información del proceso clínico, categorizando el riesgo de forma automática.
En varios estudios se hace referencia a formación previa por parte de los farmacéuticos con duración variable20,24, que era impartida por infectólogos22 o inmunoalergólogos23, que estaban siempre disponibles para resolver dudas. Tenían 2 componentes: uno teórico y otro práctico, con discusión caso a caso.
Test cutáneosLos test cutáneos se describieron detalladamente en un estudio17, consistiendo en 3 fases: test epicutáneo, test intradérmico con penicilina diluida y administración oral de 250 mg de amoxicilina o ampicilina endovenosa (si no hubiese tolerancia oral). Estos test eran realizados por farmacéuticos residentes y especialistas previamente formados, siguiendo un protocolo aprobado por la Comisión de Farmacia y Terapéutica.
Así mismo, en otros estudios, se identificaban potenciales fármacos que pudiesen enmascarar la liberación de histamina16.
DesetiquetadoCuando había indicación para realizar desetiquetado, el farmacéutico del PROA registraba el resultado de la evaluación, actualizando la información relativa al registro de alergia en el proceso clínico16,18,21. En el estudio de Mitchell et al.16 esta información complementaba al registro original. En algunos casos, se entregaba al paciente una tarjeta para informar al médico de familia de esta actualización18.
EficaciaVariables de eficaciaLas principales medidas de resultado que evaluaron la eficacia de la intervención fueron: el porcentaje de desetiquetado (en 8 estudios), el consumo de antibióticos (B-lactámicos o alternativos) (en 4); la tasa de CD (en uno) y la mortalidad general (en uno).
Otras variables de eficacia medidas fueron: el número de pacientes cuyo régimen antibiótico fue desescalado, el coste del tratamiento antibiótico y probabilidad de prescripción de beta-lactámicos, cefalosporinas de primera generación o de antibióticos con elevado riesgo de aparición de CD.
DesetiquetadoEl porcentaje de pacientes a los que se realizó desetiquetado directo (tras ser realizada la aclaración de la historia de alergias mediante entrevista) varió entre un 13 y un 64%, siendo la mediana del 18%. En el estudio de Tanya du Plessis et al.15que presentó el mayor porcentaje de desetiquetado, el 50% había tolerado un ciclo de un antibiótico con penicilina antes de la inclusión en el mismo.
Tras la realización de pruebas cutáneas o de provocación oral las tasas de desetiquetado variaron entre 8,6% (Mitchell et al.16) y 96% (Harmon S. et al.17).
Consumo de antibióticosSe hallaron diferencias significativas en la variable principal en 4 estudios incluidos, a favor de la intervención farmacéutica.
En el estudio de Clark KE et al.20, la dosis diaria definida (DDD) media de aztreonam por 1.000 pacientes-día y la media de días de terapéutica por 1.000 pacientes/día disminuyeron (21,23 vs. 9,05; p < 0,01) y (8,79–4,24; p = 0,016), datos pre y postimplementación del cuestionario y recomendaciones asociadas, respectivamente. En el estudio de Devchamd et al.21 hubo una disminución significativa en la prescripción de antibióticos de uso restringido (42,5 vs. 17,9%; p < 0,01). Vaisman et al.22 reportaron una disminución en la utilización de antibióticos profilácticos prequirúrgicos alternativos a cefazolina (81,9 vs. 55,9%; p < 0,01). En el estudio de Kwiatkowski S et al.25 hubo un aumento en el uso de cefazolina de 28 a 65% (p < 0,01). En el estudio de Turner NA et al.18 no se encontraron diferencias significativas en el consumo de b-lactámicos de espectro estrecho (amoxicilina, amoxi-clavulanico) y antibióticos de uso restringido, incluyendo antibióticos asociados a alto riesgo de infección por CD (por ejemplo, ceftazidima, ceftriaxona, ciprofloxacina, clindamicina comparando los periodos pre y postintervención). Solo se consiguió demostrar una reducción en el consumo de antibióticos alternativos a penicilinas (aztreonam, ciprofloxacina, etc.) reportándose una mayor probabilidad de prescripción de b-lactámicos antes del alta.
SeguridadVariables de seguridadNi en el estudio de Mann KL et al.19 ni en el de Clark et al.20 se reportaron eventos adversos durante los mismos ni durante el seguimiento anual postintervención según Tanya du Plessis et al.15. El 98% de los pacientes que fueron «desetiquetados» no tuvieron ningún evento adverso tras la administración repetida de antibióticos que contenían penicilina. Así mismo, no hubo reacciones adversas tras la administración de cefazolina según Vaisman et al.22.
Sin embargo, hubo notificación de efectos adversos en algunos estudios incluidos: según el trabajo de Devchand M et al.21 un paciente desarrolló erupción cutánea tardía; en el de Ham et al.23 2 pacientes sufrieron efectos adversos leves tras provocación oral y en el Harmon et al.17 fueron notificados 2 pacientes con efectos adversos tras test intradérmico: rash cutáneo y reacción local.
Otros parámetrosEn el estudio de Harmon S et al.17 hubo una reducción media del gasto global en terapéutica antibiótica de 74,75 USD por día.
En el estudio de Song YC et al.26 el tiempo medio utilizado por cada entrevista fue de 5,2 minutos por paciente.
DiscusiónLa protocolización de actuación frente a pacientes con sospecha de alergia a antibióticos beta-lactámicos constituye uno de los objetivos principales de los grupos de control de infección y existen numerosas publicaciones recientes que analizan la eficacia, seguridad y coste – efectividad de estas medidas24–26.
El farmacéutico clínico forma parte de estos grupos y coopera en esta actividad con el resto del equipo; sin embargo, es escasa la literatura publicada donde este profesional la lidera.
En nuestra revisión, las principales intervenciones farmacéuticas fueron la realización de una entrevista estructurada (telefónica o presencial) a los pacientes con sospecha de alergia, realización de test cutáneos y test de provocación oral bajo vigilancia, «desetiquetado» directo en pacientes considerados no alérgicos previa confirmación de la historia clínica y referenciación al especialista de inmunoalergología para realizar más test específicos.
Analizando los resultados de los estudios incluidos en esta revisión conseguimos identificar que estos datos apenas consiguen orientar o recomendar acerca de cuál es la mejor forma de actuación frente a pacientes con sospecha de alergia, pero no son determinantes ni tienen la suficiente robustez científica para decidir si es viable que el farmacéutico sea el profesional de referencia para llevar a cabo esta actividad.
A pesar de no existir resultados concluyentes, la presencia y visibilidad del farmacéutico en los grupos de control de infección está en auge, y se encuentra apoyado por normativa internacional y nacional. Tal es el caso, en Portugal, de la Normativa de la Direçao geral de Saude (DGS) de septiembre 202228, que obliga a la implementación de estos grupos en todos los hospitales, tanto públicos como privados, para potenciar la actividad relacionada con los PROA y disminuir el riesgo de resistencias antimicrobianas. Estos grupos son constituidos de forma obligatoria por, al menos, un farmacéutico especialista.
A la luz de los resultados, aplicando medidas simples como cuestionarios a los pacientes para esclarecer la historia de la reacción alérgica o herramientas informáticas29 se consigue realizar, en aquellos de «bajo riesgo», desetiquetado y referenciarlos a profesionales de inmunoalergología mejorando el uso de penicilinas y reduciendo la necesidad de antibióticos de segunda línea. Es probable que este enfoque reduzca el riesgo de infecciones iatrogénicas, infecciones multirresistentes y reduzca los costes de atención médica.
Sin embargo, no existe consenso acerca de los criterios para realizar desetiquetado y considerar las «falsas» alergias como intolerancias, siendo que muchas de estas herramientas como PenFast29no se encuentran validadas específicamente para ser utilizadas por profesionales no médicos
Relativamente a la actividad de provocación oral por penicilinas u oral challenge y realización de test cutáneos de desensibilización, aunque existen publicaciones donde son los farmacéuticos las que las realizan, se trata de contextos muy específicos ya que recibieron formación especializada por parte de profesionales de inmunoalergología. Sin embargo, no son detallados los pormenores de esta formación, ni en objetivos, tiempo ni competencias que se deben adquirir15–18,21,23,30,31. Además la elevada heterogeneicidad de los marcos sanitarios y políticos de estos trabajos hace difícil su transversalización a la práctica diaria de los farmacéuticos de hospital.
En el caso de España y Portugal esta actividad es realizada por profesionales de inmunoalergología.
Por otro lado, apenas 7 de los 12 estudios incluidos en esta revisión hacen referencia a variables de seguridad y los resultados no se encuentran definidos. Si bien, el número de notificaciones de efectos adversos es escasa y fueron considerados leves.
FortalezasEsta revisión aporta una visión conjunta y actual de los estudios publicados hasta la fecha, centrándose en la parte más relevante desde el punto de vista del papel del farmacéutico clínico convenientemente formado, con el objetivo de evaluar el impacto de este rol en pacientes con sospecha o registro de reacción alérgica a beta-lactámicos, concretamente como elemento clave para poder realizar desetiquetado directo o referenciación a los especialistas de inmunoalergología.
LimitacionesLa limitación principal de esta revisión es que no existen ensayos clínicos aleatorizados y que, algunas de las conclusiones alcanzadas, son limitadas ya que se basan en estudios cuasi experimentales, de una calidad más deficiente. Además, en esta revisión, no se realizó la valoración de los diferentes sesgos de los estudios incluidos y al aplicar los criterios de exclusión, el número finalmente incluido se reduce considerablemente.
Otra limitación importante constituye el hecho de haberse utilizado apenas 2 bases de datos para realizar la búsqueda bibliográfica. Con el objetivo de obtener la evidencia más reciente sobre este asunto se estableció el horizonte temporal de los últimos 5 años, sin embargo, se solicitó una búsqueda adicional al CIM-OF para minimizar el riesgo de sesgo de inclusión o selección.
ConclusiónLa implicación del farmacéutico en la evaluación del paciente con sospecha de alergia a beta-lactámicos, según la evidencia científica más reciente, parece resultar eficaz, segura y aplicable a la práctica clínica. La estandarización de protocolos para esclarecer la historia de alergias y desarrollo de herramientas de evaluación, como cuestionarios estructurados, constituyen un sencillo cribado para realizar desetiquetado o referenciar al servicio de inmunoalergología en situaciones específicas. La aplicación de esta actividad permite, desde el punto de vista individual del paciente, desetiquetar falsas alergias y la utilización segura de estos antibióticos de primera línea, y a nivel global, reducir el consumo de antibióticos alternativos, con mayor potencial en desarrollar resistencias.
Sin embargo, estos beneficios potenciales se basan en estudios altamente heterogéneos en cuanto a la metodología de poca calidad, sería conveniente la existencia de ensayos clínicos aleatorizados con la metodología correcta que puedan dar una mayor calidad en la evidencia disponible.
Una formación específica en esta área permitiría aportar más valor y ampliar el mapa de competencias de nuestra especialización, tanto en Portugal como en España, constituyendo un futuro desafío para la profesión farmacéutica.
FinanciaciónNinguna.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
Contribuciones de los autoresLos autores Jesus Cotrina Luque, Maria José Rei, y Miriam Capoulas han contribuido con el concepto, diseño, definición del contenido intelectual, preparación, revisión y edición del manuscrito y son garantes del presente trabajo.
Los autores Jesus Cotrina Luque y Maria José Rei han contribuido búsqueda de la literatura, obtención y análisis de los datos.