Analizar el perfil de tratamientos y preparaciones parenterales (antineoplásicas y de soporte) dispensados y devueltos al servicio de farmacia, las causas de no administración, su reutilización y los costes directos asociados.
MétodoEstudio longitudinal, prospectivo, durante 8 meses (octubre 2004-mayo 2005) en un hospital terciario con centralización de la preparación de esquemas antineoplásicos (incluye tratamiento de soporte) en el servicio de farmacia. Las variables estudiadas, descargadas del aplicativo Oncofarm®, fueron: a) pacientes y diagnósticos; b) tratamientos devueltos, diferenciando por causa, esquema farmacoterapéutico, ciclo y día; c) preparaciones devueltas (antineoplásicos y soporte) y reutilizadas, y d) costes directos. Los datos se presentan con sus frecuencias absolutas, relativas e intervalos de confianza (IC) del 95%, normalizado a 1.000 pacientes/día.
Resultados84 tratamientos devueltos de 66 pacientes con un total de 139 preparaciones correspondientes a 3.429 pacientes/día. Este dato representa 24,5 (IC del 95%, 19,6 a 30,2) de tratamientos preparados y no administrados por 1.000 pacientes/día, debido, mayoritariamente, a causas clínicas (n=47).
La neoplasia de colon y el esquema de 5-fluorouracilo y ácido levofolínico presentan el mayor número de devoluciones. Las preparaciones devueltas suponen el 1,45% (IC del 95%, 1,2 a 1,7) de las elaboradas. El porcentaje de reutilización es del 98%, con un coste ahorrado que asciende a 10.432,55 € (90% del coste de los tratamientos devueltos).
ConclusionesLa aplicación de criterios de calidad, eficacia y seguridad a los tratamientos antineoplásicos preparados y devueltos al servicio de farmacia permite incrementar la eficiencia en el proceso de preparación.
Analyse the profile of parenteral preparation and treatment (anti-neoplastic and supplementary) that were dispensed and returned to the Pharmacy Department, the reasons why they were not administered, their reuse and the associated direct costs.
MethodLongitudinal study over eight months (October 2004-May 2005) in a tertiary hospital with centre for preparing anti-neoplastic agents (including supplementary treatment) in its Pharmacy Department. The variables studied, downloaded from the Oncofarm® application, are as follows: a) patients and diagnostics; b) returned treatments, classified by reason returned, pharmaco-therapeutic scheme, cycle and day; c) returned preparations (anti-neoplastic and supplementary) that were reused; and d) direct costs.
Data is presented with its absolute and relative frequencies and confidence intervals of 95% normalised at 1000 patients/day.
Results84 treatments were returned by 66 patients for a total of 139 preparations corresponding to 3,429 patients/day. This figure represents 24.5 (CI 95%, 19.6 to 30.2) treatments that were prepared and not administered per 1,000 patients/day, mainly due to clinical causes (n=47).
Colon neoplasia and treatment with 5-fluorouracil and levofolinic acid presented the highest number of returns. The returned preparations made up 1.45% (CI 95%, 1.2 to 1.7) of those produced. The percentage of reuse is 98%, which results in savings of € 10,432.55 (90% of the cost of the treatments that are returned).
ConclusionsThe application of quality, effectiveness and safety criteria to anti-neoplastic treatments that are prepared and returned to the Pharmacy Department allows a more efficient preparation process.
Las dosis de cada fármaco, recibidas finalmente por los pacientes, con independencia de los parámetros posológicos manejados, permiten cuantificar el cumplimiento del tratamiento prescrito y sus consecuencias potenciales. En el paciente ambulatorio no oncológico, el porcentaje de medicamentos devueltos no alcanza el 1 % del total de medicamentos distintos prescritos1. Este porcentaje se sitúa entre el 8 y el 15 % cuando se refiere a mezclas intravenosas (MIV) preparadas en el ámbito hospitalario2,3, sin que se disponga de información sobre devoluciones de tratamientos antineoplásicos.
Los pacientes oncológicos raramente cumplen en todos sus parámetros posológicos los tratamientos quimioterápicos programados; unas veces se modifican los días, otras el número de ciclos, otras los componentes de los esquemas farmacoterapéuticos (EFT). En terapia adyuvante para cáncer de mama (FEC y AC) sólo entre el 30 y el 40 % de las pacientes alcanza un cumplimiento del 100 %4. La modificación de dosis en estos EFT por debajo de los niveles demostrados efectivos se correlaciona con una pérdida de beneficio5.
Así, unas veces por fallo en criterios logísticos, otras por efectos adversos o por falta de respuesta en el paciente, un porcentaje de los tratamientos programados confirmados, preparados y dispensados no se llega a administrar al paciente.
Operativamente, ante la devolución de tratamientos quimioterápicos, caben dos actuaciones: intentar su recuperación o propiciar directamente su desecho. Consideraciones éticas subyacen en esta decisión, por lo que se ha propuesto que cualquier tratamiento, completo o parte del mismo, que no se administre al paciente para el que se preparó, sea destruido mediante incineración1. También se defiende la opción opuesta (recuperar) ya que, por su elevado coste, potencial reducción de carga asistencial en el servicio de farmacia (SF), costes para su desecho y potencial contaminación medioambiental, propiciar su reutilización, una vez garantizada su validez terapéutica en términos de efectividad y seguridad, no cabe duda de que es una práctica lícita, profesionalmente respetable y coste efectiva2,6,7. Lógicamente, cualquier condición que altere en estas MIV devueltas los criterios de calidad (fisicoquímica, microbiológica y posológicos) es motivo para su destrucción, siguiendo los criterios establecidos para este fin8.
En este escenario, los estándares de la JCAHO (MM.4.80)9, y más recientemente los de la ISOPP (sección 20)8, establecen que las MIV de antineoplásicos, preparadas y devueltas a la unidad centralizada del SF, deben de cumplir con los criterios de calidad establecidos si se plantea su posterior reutilización, ya sea en el mismo paciente o diferente. Esta situación es aplicable con carácter general, dado que un mismo fármaco puede formar parte de los diferentes protocolos de quimioterapia.
El objetivo del presente trabajo es conocer el perfil de las preparaciones parenterales (antineoplásicas y de soporte) devueltas al SF. Además, se analizan las causas que determinan su no administración al paciente oncológico, el destino final (reutilización o desecho) y los costes directos. Con el objetivo de proporcionar las bases para la gestión de la devolución de tratamientos quimioterápicos no administrados y su posterior reutilización.
MétodoEstudio longitudinal, prospectivo, durante un período de 8 meses (octubre 2004-mayo 2005), realizado en un hospital universitario terciario (535 camas). La preparación de todos los tratamientos se realiza de forma centralizada en la unidad de terapia intravenosa del SF, siguiendo los estándares de calidad (5.901 tratamientos, 18.290 preparaciones y 632 pacientes oncológicos/año). Los EFT requeridos para tratar a los pacientes oncológicos incluyen tanto los fármacos antineoplásicos como de soporte necesarios para garantizar la efectividad y la seguridad del tratamiento, y han sido diseñados de forma protocolizada y consensuada entre los servicios clínicos de farmacia y de oncología médica.
Los pacientes incluidos en este estudio fueron atendidos tanto en el hospital de día (10 sillones/3 camas) como en la unidad de hospitalización (20 camas). En al menos una ocasión su tratamiento, confirmado, preparado, dispensado y no administrado, fue devuelto al SF según el protocolo normalizado de trabajo (PNT).
Los procesos de la cadena terapéutica, desde la programación hasta la administración de los tratamientos y, su devolución justificada, están informatizados y doblemente validados con dispositivos auxiliares (tecnología de código de barras). La figura 1 muestra el mapa de procesos integrados para la reutilización de las preparaciones parenterales de esquemas antineoplásicos. De ellos cabe destacar:
- 1.
Sistema de información de las preparaciones no administradas y devueltas al SF.
- –
La historia farmacoterapéutica del paciente que no recibe su tratamiento se actualiza electrónicamente con ayuda de la tecnología de código de barras manejando variables: a) del paciente (nombre del paciente, número de historia clínica, servicio al que pertenece, diagnóstico); b) del tratamiento (acrónimo del esquema empleado, ciclo y día del tratamiento, medicación, fecha y hora de preparación, fecha y hora de devolución, coste, y c) de las preparaciones (códigos identificativos, estabilidad de los principios activos, posibilidad de reutilización, caducidad y causa de la devolución). Se ha considerado tratamiento la combinación de preparaciones (fármacos antineoplásicos y de soporte) correspondientes a un día del EFT prescrito al paciente.
- –
Validación farmacéutica (VF) de las preparaciones devueltas y criterios de calidad y seguridad manejados10.
- –
- 2.
Tecnológicos: integridad del envase, etiquetado correcto y legible, y funcionamiento del sistema de administración, si procede (infusores, etc).
- 3.
Fisicoquímicos: control visual (coloración y/o precipitación), condiciones de conservación del preparado fuera del SF (temperatura, humedad y fotoprotección, si fotosensible), y fecha de caducidad, establecida de forma individualizada para cada preparación sobre la base de fuentes bibliográficas sobre estabilidad y ficha técnica aprobada, en función del ámbito de concentración final, vehículo, y condiciones recomendadas de almacenamiento.
- 4.
Microbiológicos: riesgo minimizado por aplicación de estándares de calidad11. Existen tres niveles de riesgo establecidos en función de la seguridad en el paciente12-16. Las MIV que componen los EFT están clasificadas en nivel de riesgo I (bajo): mezclas simples preparadas en condiciones estériles (cabina flujo laminar), almacenadas a temperatura ambiente y administradas dentro de las 24 h desde su preparación o conservadas a 2-8 °C durante un máximo de 7 días, antes de su completa administración al paciente en un período máximo de 24 h. Los criterios de reutilización establecidos incluyen los niveles I y II.
La VF de las preparaciones devueltas determina su potencialidad para ser reutilizadas (conformidad de todos los criterios) o desechadas (no conformidad de uno cualquiera de los criterios). El resultado de la VF se registra y facilita con el aplicativo Oncofarm® versión 4.0 (IMF SL, Valencia, España).
- 5.
Gestión de las preparaciones devueltas y potencialmente reutilizables. El sistema informático Oncofarm® gestiona la fecha de caducidad y la posibilidad de reutilización de las mezclas devueltas y de las preparaciones disponibles en la base de datos del aplicativo. El proceso se activa y se hace visible al farmacéutico, en el momento que éste valida el tratamiento antineoplásico de cualquier paciente, en el que al menos uno de los componentes (fármaco) del mismo es coincidente y está disponible en mezcla lista para su reutilización. Los datos indicados son vehículo, volumen y sistema de administración (p. ej., infusor elastomérico). Las dosis del principio activo en las preparaciones que se ofrecen al validador se deben situar en el intervalo (banda de dosis) aceptado (± 5 % de la dosis prescrita); también ofrecen el sistema aquellas preparaciones cuya dosis sea inferior a la dosis prescrita, ya que son susceptibles de añadir a éstas la dosis restante. Una vez es aceptada la preparación que se debe recuperar, quedan registrados el profesional responsable, la fecha y hora, el paciente, el esquema farmacoterapéutico, el ciclo y el día del tratamiento.
Las variables estudiadas, descargadas de Oncofarm® fueron:
- –
Pacientes totales atendidos y que no han recibido algún componente del tratamiento prescrito.
- –
Tratamientos totales preparados y devueltos, diferenciados por tipo de causa predefinida: tecnológicos (identificación dificultada y pérdida de estanqueidad del envase), clínicos (efecto adverso por quimioterapia, progresión o situación clínica del paciente), y logísticos (error de programación y en la citación del paciente) y causa no especificada o desconocida, diagnóstico, tipo de esquema, ciclo y día.
- –
Preparaciones totales y devueltas, diferenciadas por principio activo, porcentaje de reutilización y fármacos implicados.
- –
Costes directos totales y diferenciados por las preparaciones reutilizadas y desechadas.
Todos los datos extraídos del aplicativo se han exportado (Excel) para validar su seguridad y la del sistema de información manejado. Este proceso ha permitido eliminar los tratamientos correspondientes a pacientes no oncológicos (Oncofarm® gestiona pacientes con otras afecciones distintas del cáncer). Una vez depurada la base de datos, se ha utilizado el programa SPSS® versión 12.0 para obtener frecuencias absolutas, frecuencias relativas e intervalos de confianza (IC) del 95 % (macros diseñadas para SPSS)17, como medida de precisión. Los datos se han normalizado a 1.000 pacientes/día, que equivalen a 1.000 tratamientos/día.
ResultadosCuatrocientos cuarenta y ocho pacientes oncológicos recibieron tratamiento antineoplásico y de soporte durante el período de estudio (8 meses) que, al normalizarlos a pacientes/día, alcanza un valor de 3.429 pacientes/día.
Cerca del 15 % de los pacientes (n = 66) no reciben el tratamiento completo en al menos uno de los días del total de ciclos confirmados. De este subgrupo de pacientes, al 23 % (n = 15) no se les administra el tratamiento previsto en dos o más de los días del ciclo confirmado.
En este período de tiempo, 84 de los 3.429 tratamientos confirmados, preparados y dispensados fueron no administrados y se devolvieron al SF. Este valor representa el 2,45 % (IC del 95 %, 1,96 a 3,02).
Las causas de devolución de estos tratamientos, normalizadas a 1.000 pacientes/día, se representan en la figura 2. Destacan los motivos de tipo clínico (n = 47) como causas mayoritarias, seguido de motivos logísticos (n = 15) y tecnológicos (n = 3). En 19 tratamientos devueltos no se especificó el motivo al documentar la devolución del tratamiento no administrado al paciente.
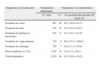
Por diagnóstico, los tratamientos preparados y devueltos se recogen en la tabla 1. Las frecuencias absolutas y relativas de los tratamientos devueltos describen las diferencias entre los diferentes diagnósticos de localización tratados.
Tratamientos antineoplásicos devueltos. Datos brutos y ajustados a diagnóstico de localización por 1.000 pacientes/día (1 de octubre de 2004-31 de mayo de 2005)
| Diagnóstico de localización | Tratamientos dispensados | Tratamientos no administrados | |
| N.° total | N.° | %o pacientes/día ajustado (IC del 95 %) | |
| Neoplasia de colon | 907 | 26 | 28,7 (18,8 a 41,7) |
| Neoplasia de recto | 395 | 14 | 35,4 (19,5 a 58,7) |
| Neoplasia de pulmón no microcítico | 441 | 12 | 27,2 (14,1 a 47,0) |
| Neoplasia de vejiga urinaria | 154 | 9 | 58,4 (27,1 a 108,0) |
| Neoplasia de estómago | 250 | 7 | 28,0 (11,3 a 56,8) |
| Otras neoplasias (n ≤ 4*) | 1.282 | 16 | 12,4 (7,1 a 20,2) |
| Total tratamientos | 3.429 | 84 | 24,5 (19,6 a 30,2) |
IC: intervalo de confianza.
La tabla 2 resume los datos crudos y ajustados (normalizado a 1.000 pacientes/día) de los tratamientos preparados y devueltos, agrupados por tipo de esquema antineoplásicos. De forma global, el esquema con mayor número de devoluciones es el que combina 5-fluorouracilo (5FU) con levofolínico; sin embargo, al ajustar los datos por EFT, es la combinación de cisplatino con gemcitabina la que presenta mayor probabilidad de no administración del tratamiento preparado.
Tratamientos antineoplásicos devueltos. Datos brutos y ajustados a esquema farmacoterapéutico por 1.000 pacientes/día (1 de octubre de 2004-31 de mayo de 2005)
| Esquemas | Tratamientos dispensados | Tratamientos no administrados | |
| N.° total | N.° | %o pacientes/día ajustado (IC del 95 %) | |
| Fluorouracilo (5FU) + LVa | 692 | 26 | 37,6 (24,7 a 54,6) |
| Oxaliplatino + 5FUb | 234 | 9 | 38,4 (17,7 a 71,7) |
| Cisplatino + gemcitabinac | 107 | 7 | 65,4 (26,7 a 130,1) |
| Otros esquemas (n ≤ 4) | 2.396 | 42 | 17,5 (12,7 a 23,6) |
| Total tratamientos | 3.429 | 84 | 24,5 (19,6 a 30,2) |
FU: fluorouracilo; IC: intervalo de confianza; LV: ácido levoflovínico.
Al analizar los tratamientos no administrados en función del número de ciclo, se han devuelto al SF tratamientos desde el primer al noveno ciclos. Destacan por su mayor frecuencia, 20 (23,81 %) tratamientos correspondientes al primer ciclo y 15 (17,86 %) al cuarto ciclo del esquema antineoplásico.
La evaluación de los días del ciclo indica que para los dos EFT con mayor incidencia de devoluciones según datos ajustados (oxaliplatino + 5FU y cisplatino + gemcitabina), el tratamiento correspondiente al día 8 del ciclo es el que se devuelve con mayor frecuencia (preparaciones de 5FU o gemcitabina, respectivamente).
Al analizar los tratamientos dispensados y no administrados en relación con el número total de preparaciones parenterales dispensadas, se computan 139 preparaciones devueltas (81 de antineoplásicos y 58 de soporte) respecto a 9.575 preparaciones parenterales elaboradas durante el período de estudio, lo que representan el 1,45 % (IC del 95 %, 1,22 a 1,7) de las preparaciones. Este dato equivale a 40,54 preparaciones devueltas por 1.000 pacientes/día (IC del 95 %, 34,18 a 47,69) o 4,05 devoluciones por cada 100 pacientes con tratamiento por día; de éstas 23,62 por 1.000 pacientes/día (IC del 95 %, 18,80 a 29,27) corresponden a antineoplásicos y 16,92 por 1.000 pacientes/día a tratamiento de soporte (IC del 95 %, 12,87 a 21,81).
De manera similar a la tablas anteriores, las tablas 3 y 4 muestran los principios activos utilizados, antineoplásicos y de soporte, en las preparaciones devueltas al SF, normalizados a 1.000 preparaciones/día.
Preparaciones devueltas. Datos brutos y ajustados a principio activo por 1.000 preparaciones/día (1 de octubre de 2004-31 de mayo de 2005)
| Principio activo antineoplásico | Tratamientos dispensados | Tratamientos no administrados | |
| N.° total | N.° | %o pacientes/día ajustado (IC del 95 %) | |
| 5FU | 1.720 | 43 | 25,0 (18,1 a 33,5) |
| Gemcitabina* | 3.567 | 21 | 5,9 (3,6 a 9,0) |
| Ciclofosfamida | 180 | 3 | 16,7 (3,4 a 47,9) |
| Docetaxel* | 187 | 3 | 16,4 (3,3 a 46,2) |
| Etopósido | 220 | 3 | 13,6 (2,8 a 39,3) |
| Irinotecan | 210 | 3 | 14,3 (3,0 a 41,2) |
| Epirubicina | 147 | 2 | 8,1 (0,9 a 28,9) |
| Carboplatino | 217 | 1 | 4,6 (0,1 a 25,4) |
| Cetuximab | 50 | 1 | 20,0 (0,5 a 106,5) |
| Cisplatino | 341 | 1 | 2,9 (0,1 a 16,2) |
| Total preparaciones | 5.180 | 81 | 15,6 (12,4 a 19,4) |
FU: fluorouracilo; IC: intervalo de confianza.
Preparaciones devueltas. Datos brutos y ajustados a principio activo por 1.000 pacientes/día (1 de octubre de 2004-31 de mayo de 2005)
| Principio activo soporte | Tratamientos dispensados | Tratamientos no administrados | |
| N.° total | N.° | %o pacientes/día ajustado (IC del 95 %) | |
| Ácido levofolínico* | 1.174 | 23 | 19,5 (12,5 a 29,2) |
| Dexametasona | 1.380 | 16 | 11,6 (6,6 a 18,7) |
| Ondansetrón | 1.125 | 10 | 8,9 (4,3 a 16,3) |
| Atropina | 196 | 6 | 30,6 (11,3 a 65,4) |
| Granisetrón | 238 | 3 | 12,6 (2,6 a 36,4) |
| Total preparaciones | 4.395 | 58 | 13,2 (10,0 a 17,0) |
IC: intervalo de confianza.
Tras aplicar los criterios de reutilización predefinidos, 133 (97,84 %; IC del 95 %, 93,82 a 99,55 %) preparaciones dispensadas y devueltas al SF se reciclaron para otros pacientes en tratamiento antineoplásico. Las 3 preparaciones desechadas no cumplían el criterio tecnológico de integridad y estanqueidad del envase.
El coste directo en medicamentos antineoplásicos y de soporte manejados para la preparación de los tratamientos preparados para los pacientes oncológicos atendidos por el servicio de oncología, durante el período de estudio, ascendió a 1.274.718,14 € (371.746,32 € por cada 1.000 pacientes/día). Los costes directos de los tratamientos devueltos representan 0,91 % del total del período de estudio. De este valor, el 90 % se ahorra (10.432,55 €) por la reutilización de estas preparaciones. Las pérdidas por no administración de los tratamientos ascendieron a 1.219,92 €.
DiscusiónEn este estudio, el bajo porcentaje de devolución de tratamientos (2,45 %) registrado informa del alto grado de cumplimiento del esquema de tratamiento confirmado a los pacientes oncológicos.
La devolución de tratamientos oncológicos es, mayoritariamente, por motivos de tipo clínico (56 %) y engloba a causas no siempre predecibles. Así, el cambio de esquema por progresión de la enfermedad, los efectos adversos asociados a la quimioterapia y cualquier situación del paciente, no óptima para recibir la quimioterapia (p. ej., catarro o gastroenteritis) se evalúan, en general, después de la confirmación de los tratamientos por el oncólogo.
Como estrategias de mejora propuestas, la integración del aplicativo informático con los sistemas de soporte a la decisión y la historia clínica informatizada18 son de utilidad. También disponer de un procedimiento de trabajo integrado facilita la comunicación interdisciplinar y el registro de las causas de devolución en el aplicativo; no obstante, en este estudio hasta en el 23,6 % de las devoluciones se desconocía el motivo real, ya que se utilizó el término por defecto "sin especificar", lo que motivó una revisión, actualización y difusión del procedimiento actual en el marco del programa de calidad implantado19. Las causas de devolución registradas en este estudio no difieren de las publicadas en atención primaria o hospitalaria (efectos adversos y cambio de tratamiento)20.
Los diagnósticos con mayor número de preparaciones devueltas son las neoplasias de colon y recto, hecho que explica por qué los dos principios activos más frecuentemente devueltos son el 5FU y el ácido levofolínico. Estos datos se correlacionan con las neoplasias de mayor prevalencia21 y justifican el alto porcentaje de reutilización de estas MIV. Esta situación ya se ha evidenciado en anteriores publicaciones sobre devoluciones de medicación10.
El análisis ajustado de las devoluciones indica que la neoplasia de vejiga es el diagnóstico con mayor probabilidad con 5,8 tratamientos devueltos por cada 100 tratamientos preparados (tabla 1).
En relación con los ciclos, se observa que los ciclos 1 y 4 destacan al coincidir con la inadecuada situación clínica del paciente para iniciar el tratamiento (desfase temporal entre programación y confirmación) y con toxicidad secundaria a la quimioterapia en el cuarto ciclo, respectivamente.
En el ámbito hospitalario, la devolución de tratamientos representa entre el 8 y el 15 % del total de mezclas parenterales preparadas2,3,10. En este estudio el porcentaje de unidades devueltas es de 5 y 10 veces inferior al publicado. Esta diferencia puede explicarse por un procedimiento de trabajo integrado y por la informatización de procesos clave, entre los SF y servicio de oncología médica22.
Una segunda dimensión que se debe evaluar en el proceso de devolución de tratamientos antineoplásicos y de soporte es su potencial reutilización que se sitúa en el ámbito no hospitalario entre el 20 y 46 % de los devueltos, tras aplicar al período de validez criterios de calidad1,23; este porcentaje se eleva al 80-88 % en el ámbito hospitalario10,24.
En este estudio la reutilización de los tratamientos no administrados es del 97 % de las preparaciones debido a que la medicación permanece desde la dispensación hasta la devolución en condiciones ambientales controladas. A este resultado contribuye, además, la normalización de concentraciones, el tipo y volumen de vehículo, como sucede con las MIV con dexametasona y ondansetrón, que se reutilizan en el 100 % de las devoluciones.
En oncología se ha documentado que un 1,33 % de los citostáticos pueden reutilizarse para otros pacientes, dato similar al presente estudio25.
El proceso de reutilización establecido permite ahorrar el 1 % del coste en esta medicación (15.000 € por año), por lo que un adecuado programa de reutilización es apoyado por diferentes autores2,26,27.
Todos los criterios de la ISOPP para la reutilización de fármacos antineoplásicos se cumplen en este trabajo8. Sin embargo, debemos destacar como sesgo del presente estudio el limitado tamaño muestral de los tratamientos y preparaciones devueltas al SF y que, al igual que en otros trabajos, se han considerado solamente los costes directos de la medicación2.
Este trabajo ha sido presentado parcialmente como comunicación tipo póster al 50 Congreso Nacional de la Sociedad Española de Farmacia Hospitalaria celebrado en Oviedo del 27 al 30 de septiembre de 2005.