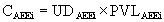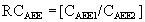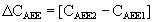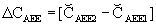La transferencia directa de los resultados de estudios farmacoeconómicos de un país a otro no es adecuada si no se procede previamente a una adaptación de los datos a cada territorio, debido a la diversidad de utilización de recursos así como a las diferencias de costes entre países.
ObjetivoEstimar el coste en España del tratamiento de la anemia secundaria a insuficiencia renal crónica con epoetina alfa o darbepoetin alfa, a partir de una revisión y un análisis de la información actualmente disponible. Además, se analiza el papel de la vía de administración como factor modulador del coste del tratamiento.
MétodoPoblación: pacientes con anemia secundaria a insuficiencia renal crónica. Extracción de datos: búsqueda en Medline y Embase de estudios de comparación directa de los agentes estimulantes de eritropoyesis. Tipo de análisis: análisis probabilístico de minimización de costes. Perspectiva: servicio de farmacia del hospital (costes farmacológicos). Variable principal: diferencia del coste medio por paciente del tratamiento de 30 días con epoetina alfa respecto de darbepoetin alfa.
Resultadosa) Hemodiálisis: la sustitución de epoetina alfa por darbepoetin alfa se asocia a una reducción mensual de costes del 8,67 %; intervalo de confianza (IC) del 95 %, −1,34 a 17,92 (17,48 €; IC del 95 %, −1,38 a 36,13); el análisis probabilístico mostró una probabilidad del 94,9 % de que la utilización de darbepoetin alfa estuviera asociada a una reducción del coste. Mediante la administración por vía intravenosa, la disminución es del 16,00 %; IC del 95 %, −2,38 a 36,77 (41,78 €; IC del 95 %, −6,21 a 96,04). b) Prediálisis: la reducción de costes con darbepoetin alfa se sitúa en el rango más probable del 11-32 %.
ConclusionesLa utilización en España de darbepoetin alfa en el tratamiento de la anemia secundaria a insuficiencia renal crónica (hemodiálisis y prediálisis) presenta una eficiencia superior a la estimada con epoetina alfa; esta diferencia en costes aumenta con la administración por vía intravenosa.
The direct transfer of the results of pharmaco-economic studies between countries may not be suitable if the proper adaptations are not made to take into account differences in treatment patterns, resource use and costs from country to country.
ObjectiveTo estimate the cost in Spain of treating anaemia secondary to chronic renal failure with darbepoetin alpha or epoetin alpha from a review and analysis of available current information. In addition, the role of the route of administration as a main driver of the cost will be analysed.
MethodPopulation: patients with chronic kidney failure induced anaemia. Data: Medline and Embase search of studies directly comparing erythropoiesis stimulating agents. Analysis: Cost minimization analysis from the perspective of a hospital pharmacy department. The main outcome chosen was the difference between the average cost per patient undergoing a 30-day treatment with epoetin alpha versus darbepoetin alpha.
Resultsa) haemodialysis: changing from epoetin alpha to darbepoetin alpha is associated with a cost reduction of 8.67 %; CI 95 %, −1.34 to 17.92 (€ 17.48; CI 95 %, −2.70 to 36.13); probabilistic analysis showed that the use of darbepoetin alpha could be associated with a cost-saving probability of 94.9 %. The IV administration yielded a decrease in costs of about 16.00 %; CI 95 %, −2.38 to 36.77 (€ 41.78, CI 95 %: −6.21 to 96.04). b) Pre-dialysis: darbepoetin alpha is associated with a cost reduction of about 11-32 %.
ConclusionsThe use of darbepoetin alpha for the treatment of chronic renal failure induced anaemia (haemodialysis and pre-dialysis) shows higher cost efficiency than epoetin alpha in Spain; these differences increase with IV administration.
La insuficiencia renal crónica (IRC) es un problema de salud de extraordinaria relevancia en España, especialmente en su estadio terminal1. La anemia, complicación habitual en estos pacientes, ha precisado de frecuentes transfusiones de sangre que deterioraban de forma significativa la calidad de vida de éstos, además de exponerles a riesgo de contagio de infecciones virales.
La aparición de los agentes estimulantes de la eritropoyesis (AEE) ha reducido la necesidad de las transfusiones y ha aumentado el bienestar de los pacientes, lo cual ha originado un amplio uso de estos fármacos. La epoetina alfa (EPO) fue el primer AEE que apareció en el arsenal terapéutico; posteriormente, han aparecido otros agentes similares, como epoetina beta, darbepoetin alfa (DBT) o epoetina delta, y más recientemente epoetina pegilada. Tanto la EPO como la eritropoyetina endógena poseen 3 cadenas de azúcares, mientras que DBT presenta 5 cadenas. Esta variación influye decisivamente en su vida media; así las epoetinas se pueden administrar semanalmente y la DBT, mensualmente. Otro aspecto diferencial lo constituye la vía de administración que se utilice: tanto epoetinas como DBT se pueden utilizar por vía subcutánea (SC) o intravenosa (IV); sin embargo, las epoetinas presentan una menor eficiencia en su administración IV respecto de la SC2, mientras que DBT presenta una eficiencia similar por ambas vías.
Se han efectuado diversos análisis farmacoeconómicos con el fin de establecer cuál sería la utilización más eficiente de los AEE. Sin embargo, la casi totalidad de los estudios se han efectuado en países como EE.UU. Se ha descrito que la extrapolación geográfica de las evaluaciones farmacoeconómicas no es posible, principalmente porque se presentan diversidades importantes de práctica clínica entre diferentes países3-6. Concretamente con los AEE se han evidenciado divergencias manifiestas en los resultados económicos originados por diferentes actuaciones clínicas entre países, incluso próximos7, o por variaciones temporales relevantes en los determinantes del coste8. Varios autores9-11 han revisado los ensayos clínicos existentes con EPO y DBT con el fin de analizar, mediante un análisis de minimización de costes, la eficiencia comparada entre ambos. En dicho análisis, la valoración de costes farmacológicos se realiza a partir de los valores extraídos del Average Wholesale Price (AWP), que representa el coste medio de venta de los fármacos en EE. UU., que difiere muy notablemente del establecido en España. No sólo el coste de 1 U EPO y de 1 μg DBT es en ese país netamente superior al del nuestro (el 159 y el 298 %, respectivamente), sino que la relación de costes (1 μg DBT: 200 U EPO) es en EE. UU. de 1,87, mientras que en España es de 1,00. Por todo ello, los resultados de estas evaluaciones farmacoeconómicas no pueden trasladarse a España sin un ajuste a la práctica habitual y a los precios de nuestro país.
El objetivo del presente trabajo fue estimar el coste en España del tratamiento de la anemia secundaria a IRC mediante la administración de EPO o DBT a través de la revisión y análisis de la información actual. Un objetivo secundario fue analizar los factores que modulan el coste de ambas alternativas terapéuticas.
MétodoDiseño del estudioEl estudio se desarrolló en pacientes que presentaban anemia secundaria a IRC; se establecieron 2 subgrupos diferenciados de pacientes: a) en diálisis y b) en prediálisis. En el primer grupo, dado que la mayoría de los pacientes dializados se hallan en HD (7,85:1 sobre los de DP), sólo se consideraron éstos. En todos ellos, el AEE se dispensó a través de los servicios de farmacia de los hospitales correspondientes, de acuerdo con la legislación española. Se trata de pacientes naive (prediálisis) o que una vez estables respecto de la dosis con un AEE y del nivel de hemoglobina (Hb), se transferían a otro (diálisis).
Al no hallarse diferencias significativas respecto de la efectividad de los diferentes AEE en el tratamiento de la anemia secundaria a IRC, el análisis farmacoeconómico utilizado en este estudio fue el de minimización de costes, asumiendo resultados similares y estableciendo la diferencia de eficiencia a partir de los costes.
En España, los AEE se dispensan exclusivamente a través de los servicios de farmacia hospitalaria. Por dicha causa, el estudio se realizó desde la perspectiva del servicio de farmacia del hospital. Ello condiciona que los costes incorporados al estudio sean los de adquisición de los AEE administrados.
El horizonte temporal para el tratamiento de la anemia se ajustó al de los estudios publicados, habitualmente 24 semanas.
Las alternativas terapéuticas consideradas inicialmente fueron las de todos los AEE que presentan indicación de anemia asociada a IRC (EPO, epoetina beta, epoetina delta, epoetina pegilada y DBT), requiriendo únicamente que se hubieran evaluado de forma simultánea en el mismo estudio para permitir una comparación directa. Las vías de administración analizadas fueron las habitualmente utilizadas: IV y SC. Las pautas posológicas se corresponden con las autorizadas en las fichas técnicas de cada AEE.
Extracción de datosSe realizó una búsqueda bibliográfica en Medline, Embase e Índice Bibliográfico Español en Ciencias de la Salud, sin limitación de tiempo, de publicación ni idioma del estudio. Se extrajeron los estudios que cumplían con los criterios de comparación directa, en paralelo o consecutiva, del coste del tratamiento con los AEE, así como los que realizaban un análisis de eficacia de cada alternativa, hacían mención expresa de las dosis administradas para obtener un objetivo de Hb y utilizaban posologías recomendadas en nuestro país; por el contrario, se excluyeron los estudios realizados según recomendaciones de dosis no autorizadas en las fichas técnicas aprobadas en España. Posteriormente, se revisaron las citas bibliográficas de los artículos seleccionados, extrayendo igualmente de ellas los estudios que cumplían con los criterios antes especificados. Dada la limitada información de las comunicaciones a congresos, no se utilizaron éstas en el estudio.
Los datos correspondientes a los niveles de Hb, así como las dosis utilizadas, se extrajeron finalmente de los estudios que se habían seleccionado. Igualmente se extrajeron datos acerca del tamaño de cada muestra analizada y la vía de administración empleada.
Datos de eficaciaEn el subgrupo de diálisis, la variable resultado fue el valor de Hb en el momento del cambio de AEE, así como el valor final observado, medidos ambos como g/dl. Dichos valores se combinaron finalmente de forma ponderada para establecer un valor medio de Hb en el momento del cambio y al final del estudio. Finalmente, se comprobó la igualdad de eficacia entre ambos parámetros, que justifica la elección del análisis de minimización de costes.
Estimación de costesDada la perspectiva del presente estudio, el modelo incorporó sólo el coste de los AEE utilizados en el tratamiento de la anemia (véase Anexo).
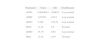
El coste del tratamiento de la anemia (CAEEi) se estimó mediante:
siendo UDAEEi el número de unidades de dosificación administradas (μg o unidad internacional [U]) de cada AEE en 30 días y PVLAEEi el precio medio unitario de cada AEE. Éste se calculó como el coste medio de cada μg o UI estimado a partir de: siendo PVLAEEz el PVL de cada presentación comercializada para cada producto z y nz el número unidades contenidas en dichas presentaciones.En el subgrupo de diálisis, los CAEEi fueron: para EPO (CEPO) fue el coste correspondiente a la dosis utilizada en el momento de la conversión a DBT, una vez estabilizado el paciente respecto de la dosis de fármaco administrada y su nivel de Hb, minimizando así el efecto de regresión a la media, y para DBT (CDBT) correspondió al coste de la dosis de DBT utilizada en el momento de la evaluación final.
El resultado final se expresó como coste por paciente y mes. Posteriormente, se combinaron ponderadamente los resultados de cada estudio para estimar el coste medio por paciente y mes de cada AEE analizado.
Finalmente, se calculó la ratio de costes de tratamiento RCAEE como:
correspondiendo 1 a DBT y 2 a los demás AEE. De esta forma, una ratio inferior a 1 indicaría un menor coste de DBT, y por lo tanto, una mejor eficiencia relativa, y una ratio superior favorecería al AEE evaluado.Para expresar la eficiencia de forma absoluta se procedió a estimar la diferencia de costes (ACaee) mediante:
de modo que un valor mayor de 0 indicaría un mayor coste de EPO, y, por tanto, una menor eficiencia absoluta, mientras que si es menor de 0 mostraría una mayor eficiencia de DBT. El análisis probabilístico se realizó mediante el diseño de sendas funciones de distribución para cada variable relevante de coste (C) y resultado (R) (tabla A1). A continuación, se procedió a una simulación de Monte Carlo mediante 1.000 remuestreos aleatorios, estimando nuevos valores para cada variable (CAEEi*, RAEEi*) en cada remuestreo y procediendo a calcular a continuación los valores medios (ČAEEi, ŘAEEi) y sus medidas de dispersión correspondientes. Finalmente, se estimó la diferencia de costes (ΔCaee) mediante:Funciones de probabilidad de los parámetros del modelo
| Parámetro | Valor | DE | Distribución |
| cEPO | 0,0084044 | 0,00013 | Log normal |
| cDBT | 1,67292 | 0,015 | Log normal |
| nEPO | 5.596 | 192,22 | Log normal |
| Hbt0 | 11,44 | 0,4 | Normal |
| nDBT | 25,39 | 0,86 | Log normal |
| Hbte | 11,44 | 0,39 | Normal |
cDBT: coste de 1 μg DBT (a PVL); cEPO: coste de 1 U EPO (a PVL); Hbt0: nivel de hemoglobina al cambio; Hbte: nivel de hemoglobina a las 24 semanas; nDBT: dosis de DBT a las 24 semanas; nEPO: dosis de EPO al cambio (en proporción 200:1 respecto de DBT).
Con el fin de incorporar no sólo la incertidumbre derivada de los resultados (incertidumbre de primer orden), sino también la asociada a las distribuciones de probabilidad de aquéllos (incertidumbre de segundo orden), se procedió a un análisis probabilístico.
Análisis de subgruposEPO y epoetina beta han mostrado diferente comportamiento en función de la vía de administración utilizada2; sin embargo, DBT puede utilizarse con la misma eficiencia, tanto IV como SC12. Este aspecto diferencial justifica un análisis diferenciado de los pacientes en función de la vía de administración utilizada en cada estudio. Por ello, después de un análisis de conjunto de todos los pacientes, se procede a un subanálisis para cada una de las vías, SC e IV.
ResultadosHemodiálisisEstudios incluidosEl análisis farmacoeconómico se efectuó a partir de los estudios que evaluaban directamente EPO frente a DBT, bien en un ensayo clínico13-15 o en estudios observacionales, en donde, una vez estabilizados los pacientes respecto de la dosis administrada de EPO, así como su valor de Hb para minimizar el efecto de regresión a la media, se procedía a la sustitución por DBT16-28.
No se pudo incluir epoetina beta en el análisis dado que sólo se halló un único estudio que analizara conjuntamente los 3 AEE27. Tampoco se incluyeron la epoetina pegilada ni la epoetina delta porque no se disponía de estudios comparativos con DBT, además de porque no se había comercializado esta última en España en el momento de hacer el estudio. Los datos extraídos de utilización de recursos farmacológicos se muestran en las tablas 1-3.
Sumario de resultados de utilización de agentes estimulantes de eritropoyesis y valores alcanzados de hemoglobina en los ensayos clínicos de evaluación de efectividad
| Autor | Ref. | n* | Vía | DBT | EPO | Ratio dosis** | ||
| Dosis/semana (μg) | Hb (g/dl) | Dosis/semana (U) | Hb (g/dl) | |||||
| Nissenson et al | 13 | 169 | IV | 54,18 | 11,4 | 12.636 | 11,2 | 233 |
| Vanrenterhem et al | 14 | 134 | IV | 27 | 10,94 | 6.700 | 11,0 | 248 |
| 213 | SC | 28 | 10,97 | 5.000 | 11,0 | 179 | ||
| Locatelli et al | 15 | 76 | IV | 21,5 | 11,9 | 5.040 | 11,3 | 234 |
| 267 | SC | 22,7 | 11,2 | 4.160 | 11,2 | 183 | ||
EPO: epoetina alfa; DBT: darbepoetin alfa; Hb: hemoglobina; IV: intravenosa; SC: subcutánea.
Sumario de resultados de utilización de agentes estimulantes de eritropoyesis y valores alcanzados de hemoglobina en los estudios de sustitución terapéutica, vía intravenosa
| Autor | Ref. | n* | DBT | EPO | Ratio dosis** | ||
| Dosis/semana (μg) | Hb (g/dl) | Dosis/semana (U) | Hb (g/dl) | ||||
| Martínez et al | 17 | 260 | 29,63 | 11,8 | 7.407 | 11,6 | 250 |
| Del Vecchio et al | 18 | 146 | 28,56 | 11,3 | 5.793 | 11,1 | 203 |
| Molina et al | 19 | 20 | 62,58 | 12,1 | 12.315 | 11,3 | 197 |
| Brunkhorst et al | 20 | 900 | 19,92 | 11,7 | 4.659 | 11,5 | 234 |
| Ardevol et al | 21 | 34 | 35 | 12,1 | 11.081 | 12,0 | 317 |
| Kessler et al | 22 | 217 | 22,32 | 11,6 | 5.452 | 11,4 | 244 |
| Pérez et al | 23 | 24 | 34,6 | 13,0 | 8.697 | 12,6 | 251 |
| Mann et al | 24 | 196 | 13,3 | 11,4 | 2.520 | 11,4 | 189 |
| Icardi et al | 25 | 40 | 24,6 | 11,4 | 8.000 | 11,4 | 325 |
| Raymond et al | 26 | 482 | 53,1 | 11,4 | 12.939 | 11,4 | 244 |
| Bock et al | 27 | 29 | 24,3 | 11,8 | 6.758 | 11,9 | 278 |
EPO: epoetina alfa; DBT: darbepoetin alfa; Hb: hemoglobina.
Sumario de resultados de utilización de agentes estimulantes de eritropoyesis y valores alcanzados de hemoglobina en los estudios de sustitución terapéutica, vía subcutánea
| Autor | Ref. | n* | DBT | EPO | Ratio dosis** | ||
| Dosis/semana (μg) | Hb (g/dl) | Dosis/semana (U) | Hb (g/dl) | ||||
| Martínez et al | 17 | 566 | 24,74 | 11,5 | 5.124 | 11,6 | 207 |
| Del Vecchio et al | 18 | 804 | 25,43 | 11,2 | 5.122 | 11,4 | 201 |
| Molina et al | 18 | 19 | 33,74 | 12,4 | 8.753 | 12,1 | 259 |
| Brunkhorst et al | 20 | 602 | 21,61 | 11,4 | 4.632 | 11,4 | 214 |
| Kessler et al | 22 | 791 | 23,32 | 11,3 | 4.585 | 11,4 | 197 |
| Shaheen et al | 28 | 33 | 20,8 | 12,8 | 7.454 | 11,6 | 358 |
| Mann et al | 24 | 905 | 16,1 | 11,3 | 3.080 | 11,6 | 191 |
EPO: epoetina alfa; DBT: darbepoetin alfa; Hb: hemoglobina.
El análisis se realizó desde la perspectiva del servicio de farmacia del hospital. Por este motivo, se han incluido como costes relevantes únicamente los asociados con los AEE, expresados como PVL en euros (€) del año 200829. De esta manera, el coste medio mensual estimado por paciente tratado en el sistema de salud español con EPO fue de 201,56 € y con DBT fue de 183,97 €, calculándose un coste incremental mensual (EPO - DBT) de 17,59 €.
Análisis probabilísticoLa simulación de Monte Carlo mediante 1.000 iteraciones (fig. 1) mostró una igualdad en el resultado clínico ({Prob (HbDBT - HbEPO) > 0} = 0,516; {Prob (HbEPO - HbEBT) > 0} = 0,484), justificando la elección del análisis de minimización de costes, mientras que evidenció una diferencia de costes entre EPO y DBT de 17,48 € (intervalo de confianza [IC] del 95 %, −2,7 a 36,13) (tabla 4).
Coste medio mensual estimado por paciente del tratamiento con EPO y DBT
| Fármaco | Coste/paciente/30 días (€) | IC del 95 % (€) |
| DBT | 184,16 | 171,73 a 197,87 |
| EPO | 201,64 | 187,20 a 215,87 |
| Diferencias de costes (EPO-DBT) | 17,48 | −2,7 a 36,13 |
| IV-DBT | 219,38 | 188,70 a 253,38 |
| IV-EPO | 261,17 | 239,93 a 301,11 |
| Diferencias de costes (EPO-DBT) | 41,78 | −6,21 a 96,04 |
| SC-DBT | 162,81 | 145,80 a 183,25 |
| SC-EPO | 164,61 | 146,01 a 184,71 |
| Diferencias de costes (EPO-DBT) | 1,80 | −25,84 a 28,02 |
EPO: epoetina alfa; DBT: darbepoetin alfa; IV: vía intravenosa; SC: vía subcutánea.
El análisis de la probabilidad de reducción de costes por la sustitución terapéutica de EPO por DBT mostró un 94,9 % de probabilidad de que la administración de DBT sea menos costosa. Así, de su representación gráfica se deduce que existe un 50 % de probabilidad de producirse una reducción de costes de 17,91 € mensuales por paciente (fig. 2).
La desagregación de los datos extraídos en función de la vía de administración del AEE puso de manifiesto el distinto comportamiento de los medicamentos analizados. Un nuevo análisis probabilístico, mediante simulación de Monte Carlo con 1.000 iteraciones para cada subgrupo, puso de manifiesto que la conversión de EPO IV a DBT IV mostraba un ahorro de dosis con DBT sustancialmente mayor (41,78 €/paciente/mes; IC del 95 %, −6,21 a 96,04) (tabla 4), mientras que la conversión de EPO SC a DBT SC revelaba una diferencia de costes no significativa (1,80 €/paciente/mes; IC del 95 %, -25,84 a 28,02).
La representación gráfica de la curva de probabilidad de reducción de costes determinó una probabilidad del 94,9 % de que se genere algún ahorro mediante la sustitución de EPO por DBT (fig. 2), estimándose un ahorro de 40,84 €, con una probabilidad del 50 % por vía IV.
Análisis de sensibilidadDado que la variable relevante es el coste de los AEE, se efectuó un análisis de sensibilidad reduciendo el coste del AEE menos eficiente (EPO) hasta un 50 % (fig. 3). Con una administración IV o SC, EPO precisa de un 8,7 % de descuento adicional para alcanzar igual eficiencia que DBT; en el caso de administración IV, dicha reducción adicional de precio debería incrementarse hasta el 16,1 %.
PrediálisisEstudios incluidosEn el subgrupo de pacientes en prediálisis se analizaron los datos de estudios que evaluaban la eficacia de DBT frente a EPO26,30-38 (tabla 5). Sin embargo, dada su heterogeneidad, principalmente sobre la base de las diferentes posologías administradas, no fue posible combinar adecuadamente los resultados obtenidos.
Sumario de resultados de DBT frente a EPO en el tratamiento de la anemia secundaria a IRC en prediálisis
| Ref. | n.° (EPO/DBT) | EPO | DBT | Ratio costea | Ratio dosisb | |||
| Dosis/semana (U) | Coste (€) | Dosis/semana (μg) | Coste (€) | |||||
| Vekeman et alc | 30 | 66.822 | 26.509 | 228,8 | 118,6 | 198,5 | 0,89 | 223 |
| Locatelli et ald | 31 | 129/37 | 7.000 | 58,83 | 31,5 | 52,70 | 0,89 | 200 |
| 3.983 | 33,47 | 23,8 | 39,81 | 1,19 | 167 | |||
| Papatheofanis et ald | 32 | 396/393 | 11.639 | 97,81 | 45,2 | 75,56 | 0,77 | 257 |
| Duh et ald | 33 | 595/260 | 11.536 | 96,95 | 42,5 | 71,10 | 0,73 | 271 |
| Duh et ald | 34 | 293/102 | 12.748 | 107,10 | 43,5 | 72,77 | 0,68 | 293 |
| Papatheofanis et ald | 35 | 200/200 | 10.155 | 85,34 | 37,6 | 62,87 | 0,74 | 270 |
| Molina et ale | 36 | 39 | 2.500 | 21,02 | 11,20 | 18,73 | 0,89 | 223 |
| Raymond et ale | 26 | 111 | 5.516 | 46,36 | 25,20 | 42,16 | 0,91 | 219 |
| Hertel et ale | 37 | 524 | 10.369 | 87,14 | 24,5 | 40,90 | 0,47 | 423 |
| Hymes et ale | 38 | 153 | 7.090 | 59,58 | 24,7 | 41,32 | 0,69 | 287 |
EPO: epoetina alfa; DBT: darbepoetin alfa.
Por ese motivo, el análisis se centró en la estimación de la ratio de dosis EPO/DBT; se observó que se situaba en el rango 200-293 en la mayoría de los casos, lo que indicó que la relación teórica de 200 U EPO:1 μg DBT no se mantenía en la práctica clínica. Posteriormente, se valoraron los costes, estimando una ratio de costes DBT/EPO 0,68-0,89 (tabla 5), lo que se traduce en una reducción de costes del 11-32 % mediante el empleo de DBT respecto de EPO.
DiscusiónEl análisis de minimización de costes que analiza el escenario de práctica clínica en España de DBT frente a EPO en el tratamiento de la anemia secundaria a IRC muestra una reducción de costes con la utilización de DBT en sustitución de EPO, tanto en el grupo de pacientes sometidos a hemodiálisis como en aquellos en prediálisis; en el primer grupo, la administración por vía IV presenta una eficiencia superior. Así, en un hospital que atiende a 100 pacientes anualmente, el ahorro estimado se sitúa en 20.976 € (8,67 % de reducción; IC del 95 %, -1,34 a 17,92), pudiendo alcanzar hasta 50.136 € anuales (16,01 %; IC del 95 %, -2,38 a 36,77) si se administra exclusivamente por vía IV en hemodiálisis. Asimismo, el coste de EPO debería ser un 8,7 % inferior al de DBT para obtener un nivel de isoeficiencia, en el caso global de administración SC e IV; si la administración se realiza por vía IV, dicho descuento incremental alcanzaría hasta el 16,1 %.
Este resultado difiere muy significativamente de los realizados en otros ámbitos geográficos, lo que demuestra que la extrapolación geográfica directa de los datos de evaluaciones económicas no es posible39. Así, Morreale et al9 determinaron que el coste anual medio con DBT es 1,2-3,0 veces superior a EPO, debido principalmente a que dichos precios son significativamente superiores a los existentes en nuestro país. Por ello, adaptando la revisión mencionada a precios españoles, el resultado se invierte, pasando de una ratio de costes DBT/EPO de 1,49 a otra de 0,79 en uno de los estudios que analizan y de 1,40 hasta 0,72 en otro. Un análisis de impacto presupuestario40 publicado posteriormente a la realización del presente estudio indica también que DBT puede generar ahorros en el sistema de salud español.
Sin embargo, sólo la diferencia de precios no explica totalmente el ahorro de costes con DBT. Scott41 había apuntado previamente que, por encima de un valor umbral de dosis de EPO, que situó en 7.000 U, la transferencia de pacientes de EPO a DBT requiere de una dosis menor a la equivalente teórica de la clásica relación 200 U EPO: 1 μg DBT, observándose una ratio de hasta 280:1 con dosis iniciales de EPO de 7.000-15.000 U. Dicha modificación de la mencionada ratio se ha corroborado en otros ámbitos geográficos, como Australia, Asia o Europa23,27,28, incluyéndose España entre ellos21.
Adicionalmente, la vía de administración influye decisivamente en la mayor eficiencia de DBT respecto de EPO. En el caso de la administración IV, ésta aporta una eficiencia adicional a DBT.
Este estudio presenta algunas limitaciones. La primera es que los costes estimados para España se han calculado a partir del coste medio de 1 U de EPO y 1 μg de DBT y no del número de viales utilizados, porque no se describía este dato en los estudios publicados. No obstante, este sesgo se minimiza porque afecta por igual a ambos fármacos y se ha incluido el coste unitario a una función de distribución de probabilidad log-normal. La segunda limitación es que el coste medio por paciente se ha basado en consumos globales, sin considerar las variaciones habidas para el ajuste de dosis; ello conlleva una pérdida de información, si bien no afecta al resultado global. En tercer lugar, los patrones de práctica real pueden diferir sensiblemente de los observados en los estudios evaluados; sin embargo, entre ellos se hallaban algunos españoles de tipo observacional que sí reflejaban dicha situación, además, las dosis utilizadas se han incluido en una función de distribución de probabilidad log-normal que minimice dicho efecto.
Como fortalezas del estudio se puede citar la exhaustiva revisión global y actualizada de toda la bibliografía disponible, sin limitación geográfica, lingüística o temporal. También se ha utilizado la metodología actualmente recomendada de análisis probabilístico, que permite analizar la incertidumbre de segundo orden asociada a las distribuciones de probabilidad de los parámetros relevantes.
En conclusión, este estudio pone de manifiesto que no es posible una transferencia directa de los resultados de estudios farmacoeconómicos entre diversos países sin proceder a una readaptación de los mismos en función de las diferencias habitualmente halladas. En este caso, la sustitución en España de EPO por DBT en el tratamiento de la anemia secundaria a IRC conlleva una reducción de costes. En hemodiálisis el ahorro medio anual se estima en 20.976 € por 100 pacientes (8,7 % de reducción) y alcanza hasta 50.136 € con administración IV (16,1 %); en prediálisis, la reducción más probable se sitúa en el 11-32 %. Estos resultados deberían confirmarse en estudios naturalísticos en nuestro país, en donde se comparen directamente la eficacia y la eficiencia de las estrategias terapéuticas descritas.
Conflicto de interesesEstudio realizado mediante financiación sin restricción alguna de Amgen S.A.