La púrpura trombocitopénica inmune (PTI) es una alteración autoinmune caracterizada por una destrucción plaquetaria mediada por anticuerpos1. El recuento de plaquetas (RP) en los pacientes con PTI suele presentar valores inferiores a 50×109/l, con el consiguiente riesgo de hemorragia.
Los tratamientos disponibles actualmente, como la esplenectomía, los corticosteroides e inmunoglobulinas, reducen la destrucción de las plaquetas mediante un mecanismo de modulación del sistema inmunitario. Sin embargo, recientemente se ha indicado que en la PTI también estaría implicado un mecanismo alterado en la producción de las mismas1,2.
Este hecho ha motivado a buscar nuevas estrategias dirigidas a potenciar la producción plaquetaria más que en modular el sistema inmunitario1,3,4.
Romiplostim es un péptido que señala y activa las rutas de transcripción intracelular a través del receptor de trombopoyetina para aumentar la producción de plaquetas3,5.
En estudios previos se concluyó que romiplostim es comparativamente favorable en relación con otras terapias contra la PTI. Los efectos adversos más frecuentes fueron cefalea, fatiga, epistaxis, artralgias y petequias. Los más graves fueron sangrado, episodios tromboembólicos, incremento de reticulina medular y neoplasias1,3–5.
Romiplostim fue aprobado en España en 2009 para aquellos pacientes adultos esplenectomizados con PTI crónica resistentes a otros tratamientos y como tratamiento de segunda línea en pacientes no esplenectomizados en los que la cirugía está contraindicada5.
Recientemente se ha aprobado eltrombopag, agonista del receptor de trombopoyetina que se administra por vía oral, a diferencia de romiplostim que se administra por vía subcutánea. Ambos son bien tolerados y con un perfil de seguridad a corto plazo favorable pues no son inmunosupresores ni aumentan el riesgo de infecciones6.
El objetivo de este estudio es describir la experiencia del uso de romiplostim en pacientes que no responden a los tratamientos de primera línea en nuestro centro, ya que no hay recomendaciones estándares de tratamiento en pacientes resistentes a esplenectomía.
Descripción del estudioEstudio retrospectivo y descriptivo, en un hospital de tercer nivel, con los casos con PTI tratados con romiplostim desde agosto de 2009 hasta agosto de 2010 en el departamento de Hospital de Día de Oncología-Hematología. Se recogieron datos demográficos y referentes a la clínica y seguridad a partir de las historias clínicas, resultados de laboratorio y sistema de prescripción electrónica.
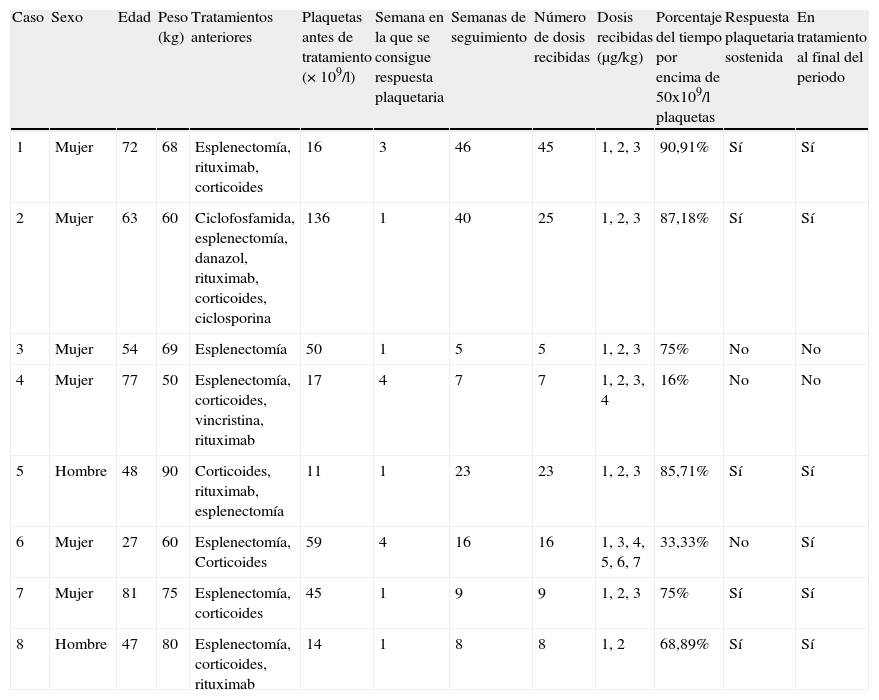
Se registraron los datos demográficos y clínicos reflejados en la tabla 1 y se comprobó que las dosis se ajustaban al algoritmo indicado por el fabricante.
Datos demográficos y clínicos de los pacientes del estudio
| Caso | Sexo | Edad | Peso (kg) | Tratamientos anteriores | Plaquetas antes de tratamiento (× 109/l) | Semana en la que se consigue respuesta plaquetaria | Semanas de seguimiento | Número de dosis recibidas | Dosis recibidas (μg/kg) | Porcentaje del tiempo por encima de 50x109/l plaquetas | Respuesta plaquetaria sostenida | En tratamiento al final del periodo |
| 1 | Mujer | 72 | 68 | Esplenectomía, rituximab, corticoides | 16 | 3 | 46 | 45 | 1, 2, 3 | 90,91% | Sí | Sí |
| 2 | Mujer | 63 | 60 | Ciclofosfamida, esplenectomía, danazol, rituximab, corticoides, ciclosporina | 136 | 1 | 40 | 25 | 1, 2, 3 | 87,18% | Sí | Sí |
| 3 | Mujer | 54 | 69 | Esplenectomía | 50 | 1 | 5 | 5 | 1, 2, 3 | 75% | No | No |
| 4 | Mujer | 77 | 50 | Esplenectomía, corticoides, vincristina, rituximab | 17 | 4 | 7 | 7 | 1, 2, 3, 4 | 16% | No | No |
| 5 | Hombre | 48 | 90 | Corticoides, rituximab, esplenectomía | 11 | 1 | 23 | 23 | 1, 2, 3 | 85,71% | Sí | Sí |
| 6 | Mujer | 27 | 60 | Esplenectomía, Corticoides | 59 | 4 | 16 | 16 | 1, 3, 4, 5, 6, 7 | 33,33% | No | Sí |
| 7 | Mujer | 81 | 75 | Esplenectomía, corticoides | 45 | 1 | 9 | 9 | 1, 2, 3 | 75% | Sí | Sí |
| 8 | Hombre | 47 | 80 | Esplenectomía, corticoides, rituximab | 14 | 1 | 8 | 8 | 1, 2 | 68,89% | Sí | Sí |
Se programaron visitas semanales y se ajustaron las dosis en función del RP previo a la dosis.
Según la ficha técnica, el tratamiento se debe ajustar para conseguir un RP de entre 50×109/l a 200×109/l (respuesta plaquetaria). La dosis inicial es de 1μg/kg. El algoritmo de mantenimiento es: RP de 50×109/l o menor, se incrementa la dosis en 1μg/kg; recuento de 200×109/l a 400×109/l, se reduce en 1μg/kg; si es mayor a 400×109/l no se administra la dosis programada y si el recuento es de 50×109/l a 200×109/l se administra la misma dosis que la anterior5.
Se determinó el tiempo necesario para alcanzar la respuesta plaquetaria y la respuesta plaquetaria sostenida, definida como aquella en la que se consiguen RP superiores o iguales a 50×109/l durante 6 semanas. Además se calculó el porcentaje del tiempo que los pacientes permanecían por encima de 50×109/l.
Se incluyeron 8 pacientes esplenectomizados y resistentes a otros tratamientos. El RP al inicio del tratamiento era inferior a 50×109/l en 6 pacientes. Una paciente inició tratamiento con más de 100×109/l plaquetas tras tratamiento con corticosteroides e inmunoglobulinas para un episodio de hemorragias.
Dos pacientes no respondieron adecuadamente a pesar de los incrementos de dosis. Por criterio médico, se decidió suspender el tratamiento a la cuarta y sexta semana y seguir con tratamientos alternativos.
No se describieron durante el tratamiento efectos adversos graves relacionados con romiplostim. Solo en un paciente se refirió cefalea al inicio del tratamiento.
Dos pacientes requirieron ingreso hospitalario: uno por un episodio de diátesis hemorrágica con plaquetopenia al mes de tratamiento, y el otro por un cuadro de infección.
Respecto al algoritmo de dosis especificado en ficha técnica, 6 pacientes recibieron dosis semanales. Un paciente no recibió una dosis que, según ficha técnica, le hubiera correspondido. El otro paciente no cumplidor del algoritmo recibió una dosis cada 15 días o cada mes. En cuanto a la dosis especificada en el algoritmo para cada rango de plaquetas, 3 pacientes recibieron todas las dosis ajustadas correctamente, mientras que el resto recibió más o menos dosis.
DiscusiónEn la forma crónica de la PTI solo el 25% de los pacientes responde al tratamiento inicial y un elevado porcentaje recae7. Romiplostim constituye una alternativa para los pacientes con PTI resistentes a los tratamientos convencionales.
En nuestra experiencia, romiplostim fue utilizado en las indicaciones aprobadas pero no siempre según el algoritmo recomendado.
Se observó, del mismo modo que en estudios previos, un aumento dependiente de la dosis del RP, excepto en los pacientes no respondedores. En estos no se encontró el motivo de la no respuesta al tratamiento pero podría estar relacionado con la inmunogenicidad o el aumento de reticulina en la médula ósea1,3,4.
Romiplostim parece ser un tratamiento bien tolerado en los pacientes de nuestro centro. Aun así, no se deben olvidar los casos de tromboembolias y neoplasias, entre otros, descritos en estudios previos5,8. Se debe valorar el beneficio-riesgo teniendo en cuenta que se desconocen los efectos adversos a largo plazo y que es necesario el tratamiento continuado5.
Las principales limitaciones del estudio son el escaso número de pacientes evaluados y que, al tratarse de un estudio observacional, la efectividad y la seguridad no pueden ser establecidas adecuadamente al no disponer de un grupo control de referencia.
No hay estudios que comparen romiplostim con eltrombopag. Factores como el coste, la comodidad del paciente, las cormobilidades, las interacciones medicamentosas y la seguridad deberían considerarse a la hora de prescribir uno u otro fármaco6.
En conclusión, los datos obtenidos parecen indicar que romiplostim puede ser una buena alternativa en pacientes resistentes a otros tratamientos para la PTI5, teniendo en cuenta que no es útil en todos los pacientes.
Parte de este trabajo ha sido comunicado previamente en el 39th European Symposium on Clinical Pharmacy. Lyon 2010.