Diseñar un protocolo de intercambio terapéutico de antidepresivos y evaluarlo clínicamente a través de variables como: grado de cumplimiento, frecuencia de casos con aumento clínicamente significativo en la escala de morbilidad psicofarmacológica Udvalg-für-Kliniske-Undersogelser (UKU), análisis de eventos adversos, análisis de la evolución global de la puntuación en la UKU y grado de aceptación de los pacientes; objetivos secundarios fueron correlacionar aspectos del tratamiento psicofarmacológico con el grado de morbilidad farmacoterapéutica y evaluar el impacto clínico de medidas de optimización farmacoterapéuticas.
MétodoEl protocolo se diseñó de acuerdo con una revisión bibliográfica y fue aprobado por la Comisión de Farmacia y Terapéutica. Se realizaron, sobre una muestra de 30 pacientes seleccionados secuencialmente, 3 mediciones (basal, a las 48-72h y a las 1-3 semanas) en las que se cuantificó la morbilidad farmacoterapéutica mediante la escala UKU y la Impresión Clínica Global, implantando medidas de optimización farmacoterapéutica en aquellos sujetos con niveles de morbilidad farmacoterapéutica elevada.
ResultadosEl grado de cumplimiento fue del 73,3%. Un paciente experimentó un aumento ≥ 25% en la escala UKU y otro paciente experimentó un evento adverso. La puntuación final en la escala UKU alcanzó la significación estadística en comparación con las medidas realizadas a las 48-72h (p=0,032) y con la medida basal (p=0,007). El grado de aceptación de los pacientes fue del 90%. El impacto de las medidas de optimización sobre el nivel de morbilidad farmacoterapéutica fue clínica y estadísticamente significativo (p<0,001).
ConclusionesEl protocolo propuesto presenta una amplia aceptación y puede considerarse seguro para su implementación en un hospital general.
To design a therapeutic exchange protocol for antidepressants and clinically assess variables, such as: compliance level, frequency of cases with clinically significant increase on the Udvalg-für-Kliniske-Undersogelser (UKU) psychopharmacological scale, adverse effects analysis, overall analysis of UKU rating development and patients’ level of acceptance. Secondary objectives were to correlate psychopharmacological treatment aspects with the pharmacological morbidity level, and evaluate the clinical impact of pharmacotherapeutic optimisation measures.
MethodThe protocol is designed in accordance with a bibliographical review, which was approved by the Pharmacy and Therapeutics Commission. Sequential study was carried out with a sample of 30 patients. Three measurements were taken (base line, at 48-72hours and at 1-3weeks) to calculate the pharmacotherapeutic morbidity with the UKU rating scale and the Global Clinical Impression. Pharmacotherapeutic optimisation measures were used for those patients with high pharmacotherapeutic morbidity levels.
ResultsThe compliance level was 73.3%. One patient experienced ≥25% increase on the UKU rating scale and another patient suffered from an adverse effect. The final UKU rating reached statistical significance compared with the measurements taken at 48-72hours (P=.032) and with the base line measurement (P=.007). Patient acceptance was 90%. The impact of optimisation measurements on the pharmacotherapeutic morbidity level was clinically and statistically significant (P<.001).
ConclusionsThe proposed protocol has been widely accepted and it is quite certain that it is to be introduced in at a general hospital level.
La selección de medicamentos no es una medida de austeridad, sino un ejercicio de inteligencia clínica. Joan Ramon Laporte
El sistema sanitario tiene que lidiar con cuestiones a menudo no resueltas por los ensayos clínicos sobre los que se fundamenta la comercialización de un nuevo medicamento. Una de las más importantes tiene que ver con la construcción de una perspectiva sistémica de la farmacoterapia. Actualmente hay en circulación un número importante de antidepresivos de segunda generación con indicaciones extendidas a la ansiedad generalizada1 o los trastornos de la alimentación2. El resultado es que un número nada desdeñable de pacientes ingresan estando en tratamiento con antidepresivos por lo que vemos esencial establecer un posicionamiento terapéutico de antidepresivos de segunda generación (ADSG) en el contexto de un hospital general.
Los resultados de la bibliografía revisada1–17 por el grupo de trabajo formado con el objetivo de confeccionar un Protocolo de Intercambio Terapéutico (PIT) muestran, en líneas generales, una ausencia de diferencia significativa en cuanto a eficacia, efectividad y calidad de vida en el tratamiento del episodio de depresión mayor, independientemente de su manifestación, entre las distintas moléculas incorporadas al análisis5,6. La respuesta de los pacientes al tratamiento con ADSG es variable y limitada: más del 50% no alcanzarán la remisión que es el principal objetivo clínico del tratamiento; además, casi un 40% de los pacientes tratados no alcanzarán respuesta clínica, que es un parámetro menos riguroso. Actualmente se desconocen los factores predictivos de respuesta6. Además, hay que tener en cuenta que los antidepresivos rara vez se emplean en situaciones de urgencia (por ejemplo, riesgo de suicidio) donde existen otras modalidades de tratamiento más efectivas. Por el contrario, sí se documentan diferencias en el perfil de seguridad5,6,17 y por tanto este fue el aspecto fundamental que rigió el proceso de selección de medicamentos, confiriendo una especial importancia al síndrome de abstinencia (SA) a ADSG dado el contexto de aplicación del PIT (un hospital general) y la presunción de la relativa frecuencia con que se dan interrupciones de tratamiento por la vía oral secundarias a procesos médicos/quirúrgicos. La incidencia del SA a ADSG es más alta para aquellos fármacos con semivida de eliminación plasmática más corta (paroxetina y venlafaxina) por lo que para fluoxetina se estima que es 100 veces menor que para paroxetina17.
Nuestro objetivo principal es iniciar las bases de un proceso de selección de ADSG mediante la confección de un PIT y la evaluación clínica del mismo a través de las siguientes variables:
- –
Grado de cumplimiento con el PIT.
- –
Frecuencia de casos que experimentan un aumento clínicamente significativo en la escala de morbilidad psicofarmacológica Udvalg-für-Kliniske-Undersogelser18 (UKU) (≥ 25%) asociado al PIT.
- –
Análisis de efectos adversos relacionados con el PIT.
- –
Análisis de la evolución global de la puntuación UKU a lo largo del estudio.
- –
Evolución en la escala Impresión Clínica Global19 (ICG).
- –
Grado de aceptación de los pacientes.
- –
Duración media del intercambio terapéutico.
- –
Impacto del PIT sobre la selección del ADSG al alta.
Los objetivos secundarios son:
- –
Correlacionar ciertos aspectos del tratamiento psicofarmacológico (carga anticolinérgica total, número de fármacos sedantes, dosis diarias definidas, etc.) con el grado de morbilidad farmacoterapéutica.
- –
Analizar el efecto de medidas de optimización farmacoterapéutica sobre la iatrogenia psicofarmacológica.
La confección del PIT de ADSG fue realizada por un grupo de expertos -constituido por las personas referenciadas en «agradecimientos» más los autores del presente estudio- y se basó en un trabajo de revisión bibliográfica cuyas características están descritas en la tabla 1. La versión final (tabla 2) obtuvo la aprobación en Comisión de Farmacia y Terapéutica para su aplicación preliminar e indicó que era viable para un estudio de evaluación clínica.
Metodología de confección del protocolo de intercambio terapéutico
| Fármacos evaluados | Mianserina, mirtazapina, reboxetina, fluvoxamina, fluoxetina, paroxetina, sertralina, citalopram, escitalopram, venlafaxina, duloxetina, bupropión y trazodona | |
| Indicaciones psiquiátricas | Diagnóstico | Código DSM-IV |
| Episodio de depresión mayor | 296.2 y296.3 | |
| Trastorno de pánico (o angustia) | 300.01300.21 | |
| Trastorno de estrés postraumático | 309.81 | |
| Trastorno obsesivo-compulsivo | 300.3 | |
| Trastorno de ansiedad generalizada | 300.02 | |
| Fobia social | 300.23 | |
| Bulimia nerviosa | 307.51 | |
| Fuentes de información | Biblioteca Cochrane Plus 2007 número 4 | |
| Pharmacy Benefits Management Service. United States Department of Veteran Affairs | ||
| Agency for Healthcare Research and Quality (AHQR) | ||
| PubMed. US National Library of Medicine | ||
| 1974-2007 Thomson Micromedex® | ||
| Uptodate ® online 15.3 | ||
| Criterios de selección de estudios | Revisiones sistemáticas y/o meta-análisis y ensayos clínicos aleatorizados posteriores (no incluidos en meta-análisis) | |
| Criterios de exclusión | Adolescentes y trastornos psiquiátricos infantiles | |
| Variables analizadas | Eficacia, efectividad, calidad de vida, perfil de efectos adversos, farmacocinética (linealidad, interacciones), perfil farmacológico (actividad anticolinérgica) | |
DSM-IV: The Diagnostic and Statistical Manual of Mental Disorders, cuarta edición.
Protocolo de intercambio terapéutico de ADSG del HGUA
| Medicamentos incluidos | Medicamentos no incluidos | ||||
| Fluoxetina | Citalopram | Escitalopram | Fluvoxamina | Paroxetina | Sertralina |
| - | 10 mg | 5 mg | 50 mg | 10 mg | 25 mg |
| 20 mg | 20 mg | 10 mg | 100 mg | 20 mg | 50 mg |
| 40 mg | 30 mg | 15 mg | 200 mg(2-3 tomas) | 40 mg | 100 mg |
▪ Valorar previamente posibles interacciones medicamentosas clínicamente significativas. En este sentido, el cambio de paroxetina a fluoxetina, carece de riesgo. | |||||
▪ Dosis más altas de las indicadas deben intercambiarse siguiendo la estrategia del cross-tapering (asociar ambos antidepresivos e ir disminuyendo progresivamente la dosis del que se quiere retirar al tiempo que se va aumentando progresivamente el que se va a iniciar) y convendría asegurarse que el paciente tenga un alto grado de adherencia al tratamiento previamente al intercambio. | |||||
▪ Pacientes con terapia psicofarmacológica compleja (asociación de antidepresivos, otros psicotropos, etc.) serán valorados por psiquiatría. | |||||
| Medicamento incluido (hipnótico-sedante) | Medicamentos no incluidos | |
| Trazodona | Mianserina | Mirtazapina |
| 150mg (2-3 tomas) | 30 mg | 15 mg |
| 300mg (2-3 tomas) | 60 mg | 30 mg |
| Siempre iniciar el intercambio con trazodona 50mg en dosis única por la noche, con aumentos progresivos c/3-4 días | ||
| Medicamento incluido (IRNS) | Medicamentos no incluidos |
| Venlafaxina | Duloxetina |
| 75 mg | 30 mg |
| 150 mg | 60 mg |
| Duloxetina: mantener cuando la indicación sea tratamiento del dolor neuropático periférico diabético | |
El estudio tuvo lugar en un período comprendido entre marzo y julio de 2008. Se incluyeron los pacientes cuyas prescripciones médicas recogieran un antidepresivo que no estuviese incluido en la guía farmacoterapéutica y la selección de los pacientes fue secuencial según orden de llegada de las prescripciones. El momento en que esto se producía por primera vez en un paciente ingresado fue considerado el momento basal; la valoración se repetía en una visita a las 48-72h y otra que se producía entre la primera y la tercera semana. Por motivos de recursos que se podían dedicar al estudio y por las características del mismo (3 mediciones en 3 tiempos distintos por paciente), como máximo se incorporaron de uno a 2 pacientes por semana. En total 30 pacientes conformaron la muestra de estudio.
La visita basal consistió en revisión de la historia clínica, entrevista del farmacéutico con el paciente de unos 15-20min de duración, y posterior entrevista con el médico a cargo del paciente. Los parámetros registrados en cada momento se detallan en la tabla 3. La escala UKU empleada fue una versión reducida y consensuada con menos número de ítems en el dominio de «otros síntomas».
Parámetros registrados en visitas (basal, 24-48 h y 1-3 semanas)
| Parámetro | Basal | 24-48 h | 1-2 semanas |
| Edad, sexo | x | ||
| Fecha de ingreso | x | ||
| Motivo de ingreso | x | ||
| Unidad de hospitalización | x | ||
| Diagnóstico asociado al ADSGa | x | ||
| Fecha inicio del ADSG | x | ||
| Comorbilidades | x | ||
| ADSG prescrito no incluido en GFT | x | ||
| FDPADSG=DP ADSG / DDD ADSGb | x | ||
| CAT=EAI1+2+…n. (EAI=FDP anticolinérgico * Panticolinérgico) | x | ||
| Número de fármacos sedantes | x | ||
| FDPBZD=DP BZD / DDD BZD | x | ||
| Grado de adherencia al tratamientoc | X | ||
| ¿Intercambio fuera de PIT?; motivo | X | ||
| Aceptación del paciente | X | X | X |
| Puntuación escala UKU | X | X | X |
| Imputabilidad farmacológica de sintomatología según la escala UKU | X | X | X |
| Síndromes psicofarmacológicos | X | X | X |
| Otros acontecimientos adversos relacionados con PIT | X | X | X |
| Puntuación escala ICG | X | X | X |
| Intervenciones de optimización farmacoterapéuticas | X | X | X |
| ¿Interrupción del ADSG durante ingreso? | X | X | X |
| ADSG seleccionado al alta | x | x |
ADSG: antidepresivo de segunda generación; BZD: benzodiazepinas; CAT: carga anticolinérgica total; DDD: Dosis diaria definida de mantenimiento; DP: dosis prescrita; EAI1+2+…n: efecto anticolinérgico intrínseco (sumatorio de cada fármaco; FDP: factor de dosis prescrita; GFT: guía farmacoterapéutica; ICG: escala de Impresión Clínica Global; Panticolinérgico: potencia anticolinérgica del fármaco (véase tabla 4). PIT: protocolo de intercambio terapéutico; UKU: escala Udvalg-für-Kliniske-Undersogelser.
En todo momento el paciente y/o médico podían expresar su deseo o conveniencia de abandono del PIT, en cuyo caso el servicio de farmacia gestionaría la dispensación del antidepresivo original.
La carga anticolinérgica total (CAT) se calculó de la manera que se indica en la tabla 3; la potencia anticolinérgica fue cuantificada entre 0 y 3 de acuerdo con 4 referencias bibliográficas4,13,21,22. Sin embargo, ya que no había concordancia entre ellas, el grupo de trabajo consensuó la potencia anticolinérgica (tabla 4) en aquellos casos discordantes entre las fuentes mencionadas.
Potencia anticolinérgica consensuada de acuerdo con bibliografía referenciada
| Psicofármaco | Potencia* | Referencias bibliográficas |
| Amitriptilina | 3 | 13, 21, 22 |
| Butilescopolamina | 0 | 4 |
| Clorpromazina | 3 | 13, 21, 22 |
| Escitalopram | 0 | 13 |
| Fluvoxamina | 1 | 13 |
| Haloperidol | 1 | 13, 22 |
| Hidroxicina | 3 | 22 |
| Levomepromazina | 3 | 13 |
| Melitraceno-Flupentixol | 3 | 4 |
| Mianserina | 1 | 4, 13 |
| Mirtazapina | 1 | 4, 21, 22 |
| Paroxetina | 1 | 21, 22 |
| Quetiapina | 1 | 13, 21, 22 |
| Risperidona | 0 | 13, 21 |
| Sertralina | 0 | 14, 21 |
| Trazodona | 0 | 21 |
| Venlafaxina | 0 | 21 |
Los resultados del estadístico inferencial se expresaron como media e intervalo de confianza al 95% y con el parámetro p, considerando que se alcanza la significación estadística cuando su valor es inferior a 0,05. En la comparación de la media de días de ingreso de nuestra muestra con respecto a la del hospital, se ha utilizado una prueba de contraste de muestras no relacionadas T-test. Para el contraste entre las 3 medidas UKU se ha realizado la prueba para k muestras relacionadas ANOVA de Friedman y para compararlas 2 a 2, la prueba para 2 muestras relacionadas de Wilcoxon. Para el contraste de la variación en la escala UKU según si había intervenciones de optimización farmacoterapéuticas, se ha efectuado una prueba para 2 muestras no relacionadas U de Mann-Whitney. Se han efectuado correlaciones de Pearson y rho de Spearman. El análisis estadístico se llevó a cabo con el programa SPSS versión 13.0 (Apache Software Foundation, USA).
ResultadosLas características sociodemográficas y clínicas basales de la muestra estudiada se reflejan en la tabla 5. La media de estancia hospitalaria es significativamente superior a la media de la muestra hospitalaria (7,0 días) para el mismo período (p<0,001). Las características del tratamiento antidepresivo basal se detallan en la tabla 6.
Características sociodemográficas y clínicas basales de la muestra estudiada (n=30)
| Edada | 64 (49-79) |
| Sexo, mujeresb | 16 (53,3) |
| Estancia hospitalaria (en días)c | 18,9±17,3 |
| Trastornos psiquiátricos (%)b | |
| SAD | 23 (76,7) |
| Conducta adictiva a drogas | 2 (6,7) |
| Demencia senil+SAD | 2 (6,7) |
| Trastorno de angustia | 1 (3,3) |
| Síndrome de abstinencia alcohólica | 1 (3,3) |
| Potomanía+SAD | 1 (3,3) |
| Motivo de ingreso (%)b | |
| Fractura de cadera por caída | 3 (10,0) |
| Descompensación ICC | 3 (10,0) |
| Fractura L3 por caída | 1 (3,3) |
| Otros motivos | 23 (76,7) |
| Unidades de hospitalización (%)b | |
| Unidades médicas | 25 (83,3) |
| Unidades quirúrgicas | 5 (16,7) |
SAD: síndrome ansioso-depresivo.
Características del tratamiento antidepresivo basal
| Antidepresivo basala | |
| Paroxetina | 13 (43,3) |
| Sertralina | 6 (20,0) |
| Mirtazapina | 4 (13,3) |
| Otros | 7 (23,4) |
| Duración del tratamiento antidepresivoa | |
| Inicio en hospital | 2 (6,7) |
| < 1 año | 8 (26,7) |
| ≥ 1 año | 20 (66,7) |
| Grado de adherencia al antidepresivoa | |
| < 80% | 4 (13,3) |
| 80-100% | 24 (80,0) |
| No procede | 2 (6,7) |
| Médico prescriptor del antidepresivoa | |
| Psiquiatría | 9 (30,0) |
| Médico de atención primaria | 8 (26,7) |
| Otros | 13 (43,3) |
| FDP antidepresivo basalb | 1,09±0,38 |
| FDP benzodiazepinas basalb | 0,77±0,74 |
| Carga anticolinérgica totalb | 1,05±0,90 |
| N.° de fármacos sedantesc | 2 (2-3,25) |
| Tratamiento coadyuvante basal | n (%) | % acum |
| BZD | 12 (40,0) | 40,0 |
| BZD+opiáceos | 4 (13,3) | 53,3 |
| Ninguno (sólo AD) | 3 (10,0) | 63,3 |
| BZD+antipsicótico | 3 (10,0) | 73,3 |
| BZD+antagonista NMDA | 2 (6,7) | 80,0 |
| Otros | 6 (20,0) | 100,0 |
% acum: frecuencia acumulativa; FDP: factor de Dosis Prescrita.
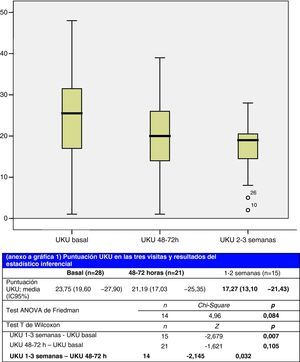
El grado de cumplimiento con el PIT y los motivos de individualización del intercambio terapéutico se detallan en la tabla 7. Los acontecimientos adversos y otras variables de evaluación del PIT se detallan en la tabla 8. La variación en la puntuación de la escala UKU a lo largo del seguimiento está reflejada en la figura 1; la medida final a las 2-3 semanas alcanzó la significación estadística en comparación con las medidas realizadas a las 48-72h (p=0,032) y con la medida basal (p=0,007).
Grado de cumplimiento con el protocolo de intercambio terapéutico y motivos de individualización
| Grado de cumplimiento; n (%) | 22 (73,3) |
| Motivos de individualización del intercambio | N.° de casos |
| Bajo grado de adherencia al antidepresivo | 2 |
| Indicación médica distinta al PIT | 2 |
| Asociación de 2 antidepresivos | 1 |
| Asociación de 3 antidepresivos | 1 |
| Antidepresivo no ajustado a indicación | 1 |
| Antidepresivo no incluido en el protocolo | 1 |
PIT: protocolo de intercambio terapéutico.
Otras medidas de evaluación del protocolo de intercambio terapéutico
| Aumento puntuación UKU clínicamente significativo (≥ 25%) relacionado con PITa | 1 (3,3%)b |
| Número de acontecimientos adversos relacionados con PIT | 1c |
| ICG basald | 5 (4-6) |
| ICG finald | 3 (2-4) |
| Grado de aceptación de pacientesa | 27 (90,0) |
| Antidepresivo al altaa | |
| El mismo que al ingreso | 15 (50,0) |
| El antidepresivo intercambiado según el PIT | 9 (30,0) |
| Sin antidepresivo | 6 (20,0) |
| Interrupción del antidepresivo durante ingresoa | 6 (20,0)e |
| Duración media del intercambio (días)f | 10,0±7,8g |
UKU: escala Udvalg for Kliniske Unders∅gelser.
La puntuación UKU basal y el porcentaje de variación de la UKU según grupos de intervención, así como los resultados de análisis estadístico inferencial, se reflejan en la tabla 9. Considerando una variación clínicamente significativa aquella inferior o superior al 25%, podemos observar cómo la relevancia clínica en la escala de morbilidad psicofarmacológica UKU se obtiene para el grupo en el que se implementan medidas de optimización farmacoterapéutica, el cual experimenta una disminución del 38,7% (IC 95% -50,33 al -27,07).
Puntuación UKU basal y porcentaje de variación de la UKU según grupos de intervención
| Grupo con intervenciones (n=12) | Grupo sin intervenciones (n=16) | |
| UKU basal; media (IC 95%)a | 28,17 (23,94 - 32,39) | 20,44 (14,00−26,88) |
| % variación UKU; media (IC 95%)b | -38,70 (-50,33−-27,07) | +5,52 (-9,12−+20,17) |
aParámetros estadísticos de la prueba U de Mann-Whitney: U=48,0; Z=-2,231; p=0,026.
bParámetros estadísticos de la prueba U de Mann-Whitney: U=6,0; Z=-3,581; p<0,001.
Un 63,4% de los pacientes presentaron al menos un síntoma grave (grado 3 en la escala UKU) probablemente relacionado con la medicación psicotrópica a lo largo del estudio. Este grado de morbilidad farmacoterapéutica se manifestó en la esfera de lo psíquico en un 42,1% de las ocasiones, siendo de carácter autonómico en un 31,6%, del dominio neurológico en un 12,3% y de otro tipo en un 14,0%. Se detectaron 11 síndromes psicofarmacológicos (tabla 10). Los SA se solían manifestar con llantos frecuentes y sin causa aparente, deterioro de la función cognitiva, alteración del ciclo del sueño, pesadillas y una alternancia entre estados de ansiedad y estados de somnolencia. En lo autonómico se observaban cuadros diarreicos, náuseas/vómitos, alteraciones de la micción y aumento de la sudoración. En lo neurológico se observaba cierto grado de distonía, rigidez, cefalea y estados hipocinéticos; una paciente experimentó vértigo. Dos pacientes desarrollaron un síndrome anticolinérgico que se manifestó entre otros síntomas con alucinaciones visuales, delirio, agitación, alteraciones mnésico-cognitivas y sequedad de mucosas (uno de ellos que además estaba en tratamiento con opiáceos desarrolló íleo paralítico y retención urinaria severa). Además 2 pacientes desarrollaron un síndrome confusional agudo y estaban en tratamiento con psicofármacos capaces de inducir delirio.
Síndromes psicofarmacológicos detectados durante el seguimiento
| Síndrome | UKUa | Causa probable (número de casos) |
| Abstinencia de paroxetina | 29,75±3,09 | Interrupción antidepresivo (3)Intercambio paroxetina-citalopramb(1) |
| Anticolinérgico | 43,50±6,36 | Carga anticolinérgica media=2,75 (2) |
| Confusional agudo multifactorial | 29,50±4,94 | Demencia+infección+inicio ISRS+BZD (1)Demencia+hepatopatía+FAE+ISRS (1) |
| Extrapiramidal | 28,00±4,24 | Sertralina (1)Paroxetina (1) |
| Abstinencia de sertralina | 14,00 | Interrupción del antidepresivo (1) |
PIT: protocolo de intercambio terapéutico; UKU: escala Udvalg for Kliniske Unders∅gelser; ISRS: inhibidor selectivo de la recaptación de serotonina; BZD: benzodiazepinas; FAE: fármacos antiepilépticos.
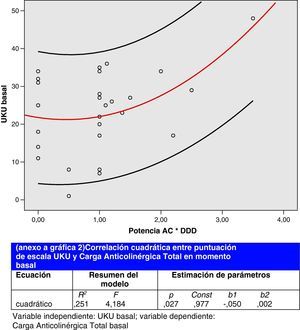
Por último, se presentan los resultados del análisis de correlación entre la UKU basal (variable independiente) y la CAT basal (variable dependiente) en la figura 2. Otras correlaciones significativas entre aspectos del tratamiento psicofarmacológico fueron:
- –
Número de fármacos sedantes – CAT (R2=0,44; p<0,001; rho Spearman=0,704; p<0,001).
- –
FDP de benzodiazepinas – FDP de antidepresivos (R2=0,19; p=0,016).
Tras la evaluación de los casos en seguimiento, podríamos afirmar que el PIT de ADSG elaborado es seguro y presenta una amplia aceptación por parte del médico y paciente. Es notable que un 50% de los tratamientos antidepresivos al alta difieran del basal por preferencias del médico y paciente, si bien, esto es asimismo un reflejo de las intervenciones de optimización farmacoterapéuticas. Un paciente mostró su deseo de volver a su antidepresivo inicial tras efectuar el intercambio de mirtazapina a trazodona porque tenía la sensación de que el cambio lo desestabilizó; este caso fue evaluado posteriormente por el psiquiatra quien relacionó el episodio con otras causas médicas (infección de un desfibrilador). Trazodona (antidepresivo sedante seleccionado) manifiesta su actividad hipnótica a través del antagonismo de los receptores 5-HT2a, 5HT2c y/o mecanismos alfa-1-adrenérgicos, mientras que el efecto hipnótico de mirtazapina se atribuye a un fuerte mecanismo antihistamínico H1 (como amitriptilina), aunque también antagoniza los receptores alfa-1-adrenérgicos, 5-HT2a, 5HT2c y 5-HT3. Trazodona, a diferencia de mirtazapina, ha sido estudiada en el insomnio primario23, además de haber sido un fármaco evaluado en el trastorno conductual y psiquiátrico en pacientes con demencia, que es una indicación frecuente en un hospital general. Aunque en la revisión sistemática14 no se mostró eficaz (como la gran mayoría de psicofármacos estudiados en trastornos conductuales asociados a demencia), tampoco se obtuvieron datos que contraindiquen su uso y valoramos su bajo22 o nulo21 potencial anticolinérgico. Nuestra conclusión a este respecto es continuar utilizando trazodona como antidepresivo sedante, así como seguir con la evaluación de resultados.
No hemos detectado ningún caso más de aumento clínicamente significativo en la UKU con ninguno de los intercambios realizados ni hemos observado casos de síndromes serotoninérgicos, rebotes colinérgicos o SA asociados al intercambio según el PIT, que eran los riesgos potenciales del intercambio de antidepresivos. Por el contrario, hemos detectado 11 síndromes psicofarmacológicos asociados a otras causas.
La importancia del reconocimiento del SA a ADSG radica en que: a) en ocasiones requiere hospitalización; b) el espectro de síntomas que induce son en su mayoría inespecíficos, por lo que existe el riesgo de incurrir en errores diagnósticos y de exponer al paciente a pruebas y/o intervenciones diagnósticas innecesarias, y c) los pacientes que lo sufren pueden abandonar el tratamiento24 (en nuestro estudio, 2 de los 3 pacientes que no aceptaron el PIT fue por temor al SA que habían experimentado en alguna ocasión previa). El problema potencial del SA a venlafaxina (de incidencia y significación clínica considerables) sigue sin estar del todo resuelto, ya que es probable que el fármaco sea interrumpido a lo largo del ingreso. Asimismo no hemos adquirido experiencia con el intercambio terapéutico de duloxetina a venlafaxina, si bien parece que no comportaría problemas a las dosis usuales12 (hasta 150mg de venlafaxina y 60mg de duloxetina).
Los resultados de nuestro estudio indican que las intervenciones de optimización farmacoterapéuticas dan como resultado una mejoría clínica y estadísticamente significativa mediante una disminución en la morbilidad farmacoterapéutica. Las medidas instauradas contaban, como es evidente, con la aceptación del paciente y del médico, y consistieron fundamentalmente en disminuir la complejidad psicofarmacológica, reduciendo la carga benzodiazepínica, psicotrópica-sedante y anticolinérgica, en aquellos casos en los que la situación clínica global del paciente lo permitía.
El análisis de correlación mostró una asociación entre el número de fármacos sedantes y la CAT, lo cual no es más que una forma de expresar un acontecimiento que hemos observado: el uso de psicofármacos hipnóticos no benzodiazepínicos (antipsicóticos, antihistamínicos, antidepresivos) añade de una forma acumulativa carga anticolinérgica, la cual puede dar como resultado en sujetos ancianos un síndrome anticolinérgico que en el dominio psiquiátrico se expresa como un delirio anticolinérgico. En nuestro estudio hemos encontrado una correlación cuadrática entre la CAT y la puntuación en la escala UKU, lo que indica una repercusión clínica que puede ser grave (ver gráfica 2). De hecho, hemos detectado dos síndromes anticolinérgicos con una puntuación UKU media superior a la de otros síndromes. La actividad sérica anticolinérgica (ASA) es cuantificable en el laboratorio y ha demostrado ser un factor de riesgo independiente de delirio, donde además, un mayor número de síntomas de delirio se asocian a ASAs más altas, lo cual puede ser un reflejo más preciso de la correlación hallada en nuestro estudio entre la carga anticolinérgica y el nivel de morbilidad farmacoterapéutica25. En cuanto a los movimientos hipercinéticos secundarios a ADSG, es una entidad clínica asociada sobre todo a los inhibidores selectivos de la recaptación de la serotonina como resultado de una interacción farmacomoduladora entre el sistema de neurotransmisión serotoninérgico y el dopaminérgico26. En nuestro estudio registramos 2 casos, uno asociado a sertralina y otro a paroxetina.
Sólo un 10% de los pacientes estaba en monoterapia antidepresiva en el momento basal, el resto llevaba asociado un tratamiento más complejo, mayoritariamente a base de benzodiazepinas siendo la mediana del número de fármacos sedantes de 2 (benzodiazepinas y otros psicofármacos). Esto parece indicar que los sujetos ingresados con un antidepresivo tienen problemas de insomnio y/o ansiedad y/o se agitan y/o presentan alteraciones comportamentales que precisan una intervención psicofarmacológica hipnótica. Los estudios indican que la dificultad para dormir no está correlacionada con la edad, sino con factores psicosociales y con problemas de salud: un 36% de sujetos mayores de 65 años sin comorbilidades manifiestan problemas de sueño, porcentaje que aumenta a un 69% cuando los sujetos tienen 4 o más comorbilidades. Lo interesante es que la propia medicación basal y la que se añada para combatir el insomnio (antidepresivos sedantes, antipsicóticos sedantes, antihistamínicos, etc.) pueden repercutir en un aumento de morbilidad (de causa medicamentosa) y como consecuencia, en una peor funcionalidad del sujeto que es la consecuencia a evitar con el tratamiento del insomnio27. Por otro lado, la depresión es la condición médica que más se asocia al insomnio de manera que la dificultad de sueño es un factor de riesgo de depresión: en nuestro estudio observamos una correlación significativa entre el FDP de benzodiazepinas y el FDP de antidepresivos, lo cual viene a concluir lo mismo desde el punto de vista del uso de medicamentos. El meta-análisis de Glass et al28 que evalúa beneficios y riesgos del uso de hipnóticos en sujetos mayores de 60 años muestra un number needed to harm (NNH) de 6 (4,7-7,1), a costa de un mayor deterioro cognitivo, deterioro de la psicomotricidad (con fracturas por caídas) y deterioro de la funcionalidad diurna. Existe una correlación entre el uso de hipnóticos y caídas en hospitales y los datos parecen indicar que los antidepresivos son los psicofármacos que más riesgo presentan de caídas29.Queda por tanto, para nuevas líneas de trabajo, el análisis de los resultados clínicos del uso de hipnóticos observado en nuestra muestra.
Consideramos nuestra propuesta de PIT de ADSG una base segura para ser implementada en el contexto de un hospital general y recomendamos su instauración desde el primer día del ingreso hospitalario con el fin de reducir el riesgo de SA. El tratamiento psicofarmacológico es susceptible de ser optimizado, sobre todo con medidas encaminadas a disminuir el riesgo de delirio de origen medicamentoso. La aceptación del médico y del paciente es alta con este tipo de propuestas.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
Al Dr. Emilio Pol-Yanguas (Centro asistencial Dr. Esquerdo), Dra. Concepción Martín Serrano (Neumología), Dr. José Manuel Carratalá (Urgencias/UCE), Dr. Fernando Quirce Andrés (Medicina Familiar y Comunitaria, C.E. Babel), Dra. Lucía Llanos (Farmacología Clínica) y Dr. Francisco Gracia Fleta (Neurología).