En personas mayores la prescripción de medicamentos potencialmente inapropiados (PIM) es muy elevada y se asocia con mayor riesgo de eventos adversos, morbilidad y utilización de recursos sanitarios. El objetivo del presente estudio es conocer la prevalencia y tipo de PIM en pacientes ancianos polimedicados al ingreso y alta hospitalaria, los factores asociados a su prescripción y la aplicabilidad de distintos criterios explícitos seleccionados de la bibliografía y adaptados a nuestro ámbito.
MétodoSe realiza estudio observacional transversal durante 12 meses (marzo 2010-febrero 2011), sobre 179 pacientes ancianos polimedicados, ingresados en un servicio de Medicina Interna. Como herramienta para detectar la prescripción inadecuada se seleccionaron 50 PIM a partir de la bibliografía (criterios Beers, Stopp, BMC y Priscus) utilizando una técnica Delphi. A través de entrevista con el paciente, revisión de historias clínicas e informe de conciliación se identificaron los PIM previamente seleccionados. Posteriormente se analizó la relación entre distintos factores y la prescripción de PIM.
ResultadosLa prevalencia de pacientes con PIM al ingreso fue de 71% y al alta de 48%. De 50 PIM seleccionados, sólo se detectaron 27 y 26 tipos (55,5% y 57,69% criterios STOPP) al ingreso y al alta respectivamente. Los factores asociados a la prescripción de PIM al alta fueron: dependencia severa-total (OR = 1,8; IC 95% 1,0-3,4) y n° de medicamentos mayor de 11 (OR = 2; IC 95% 1,1-3,7).
ConclusionesLa prevalencia de PIM en nuestra población es muy elevada (70%) especialmente al ingreso hospitalario, estos resultados apoyan la necesidad de adoptar medidas enfocadas a mejorar la calidad de la prescripción prioritariamente en pacientes dependientes y polimedicados.
Potentially inappropriate medication (PIM) prescribing in older adults is quite prevalent and is associated with an increased risk for adverse drug events, morbidity, and utilization of health care resources. The aim of this study was to determine the prevalence and type of PIM in polypharmacy elderly patients on admission and discharge and the factors associated with their prescription. Just as the applicability of various explicit criteria selected from the literature and adapted to our area.
MethodsWe performed a cross-sectional study for 12 months (March 2010-February 2011) on 179 polypharmacy elderly patients admitted to an Internal Medicine Department. We created a list of 50 PIM using a Delphi approach based on previous published criteria (Beers, Stopp, BMC and Priscus). Through patient interviews, review of medical records and discharge reconciliation report, we identified the prevalence of PIM in the patients. We also analyzed the relationship between different factors and the prescription of PIM.
ResultsThe prevalence of patients with PIM on admission and discharge were 71% and 48%, respectively. Out of the 50 selected PIM, 27 and 26 were detected on admission and discharge, respectively (55.5% and 57.69% included on STOPP criteria). We detected two factors associated with PIM prescription at discharge: severe-total dependence (OR = 1.8) and prescription of more than 11 drugs (OR = 2).
ConclusionsPIM prevalence in our population is very high (70%), especially at hospital admission. These findings support the need for measures aimed at improving the quality of prescriptions, especially on dependent patients with polypharmacy.
En la actualidad en España los mayores de 65 años representan el 17% de la población. Esta población anciana es la que acumula mayor prevalencia de enfermedades crónicas y discapacidad constituyendo un grupo de gran importancia en la terapéutica actual ya que consumen entre el 25-50% de los medicamentos prescritos y son responsables del 70% del gasto farmacéutico total1.
La evidencia sugiere que el uso de medicamentos en las personas mayores es a menudo inadecuado, en parte debido a la complejidad de la prescripción, a factores relacionados con la asistencia sanitaria y a las características propias de los pacientes. Datos en pacientes hospitalizados parecen indicar que la edad mayor o igual de 85 años, la polifarmacia y el número de comorbilidades pueden contribuir al incremento de acontecimientos adversos2.
Se entiende por medicamento potencialmente inadecuado (PIM) en el paciente anciano, aquel que presenta un riesgo significativo de causar un evento adverso en este segmento de población, bien porque existen alternativas terapéuticas más seguras, bien porque está prescrito a dosis inapropiadas, duración excesiva o muestra especial tendencia a interaccionar con otros fármacos o con la propia patología del paciente3.
En los últimos años se han desarrollado diversas herramientas para evaluar y mejorar la calidad de la prescripción y el uso de medicamentos en ancianos utilizando dos tipos de criterios: los implícitos, fundamentados en el juicio clínico y los explícitos, basados en criterios objetivos obtenidos a partir de técnicas de consenso y opiniones de expertos4.
Los criterios explícitos detectan sobre todo prescripción inadecuada (fármacos que deben evitarse o que no están indicados para determinadas condiciones o patologías).
Los más conocidos y de uso más extendido son los criterios de Beers, realizados en Estados Unidos5, y los de McLeod, de Canadá6. Ambos se centran en detallar en listados los medicamentos a evitar en cualquier circunstancia, las dosis de determinados fármacos que no se deben superar, y fármacos a evitar en determinadas patologías.
Los criterios Beers, además de las características antes comentadas, se pueden aplicar a todos los ancianos, independientemente de si viven en la comunidad o están ingresados o institucionalizados. Se han utilizado igualmente tanto con fines clínicos como para evaluar epidemiológica y económicamente planes de salud. No tienen en cuenta las posibles interacciones entre medicamentos, ni las duplicidades ni la inframedicación. Los criterios de McLeod, por su parte, son muy similares a los de Beers, pero contemplan además las interacciones fármacos-enfermedades. Sin embargo, están desfasados (por ejemplo, recoge como contraindicado en los pacientes ancianos con insuficiencia cardíaca congestiva el uso de betabloqueantes), por lo que están en desuso.
En los últimos años, se han desarrollado otros métodos explícitos más sencillos. Por un lado, un equipo de geriatras irlandeses ha elaborado una herramienta de cribado consistente en dos instrumentos: el Screening Tool to Alert Doctors to Right Treatment (START) («Right» sería traducido como «adecuado»), que consiste en un listado de 22 indicadores de prescripción basado en la evidencia de medicamentos para enfermedades prevalentes en la edad anciana, y el Screening Tool of Older Persons Prescriptions (STOPP), que es un listado de 65 criterios clínicamente relevantes de medicamentos de prescripción potencialmente inapropiada, ordenado por sistemas fisiológicos. Se centra en problemas potenciales asociados con las medicaciones en un contexto de la comorbilidad propia de la edad anciana7,8. Además, se ha publicado su versión española9.
Por otro lado, un grupo de expertos norteamericanos de la corporación RAND ha desarrollado un paquete de estándares de mínimos, generados en base a datos de revisiones sistemáticas y a opiniones de expertos, cuyo fin es garantizar la calidad de la atención a los ancianos vulnerables. Un grupo de estos indicadores está dedicado a la medicación, en el que definen varios indicadores de calidad de prescripción que detectan tanto prescripción inadecuada como sobreutilización e infrautilización. Este método se conoce como ACOVE (Assessing Care of Vulnerable Elderly)10. La tercera actualización del método ACOVE incluye 392 indicadores de calidad sobre 26 diferentes condiciones clínicas.
Recientemente han sido publicados por un grupo de autores alemanes y basándose en revisiones de la literatura científica y en el método Delphi los criterios PRISCUS11, una lista consensuada de fármacos potencialmente inapropiados para personas mayores acompañados de una serie de consejos prácticos, adaptados al medio alemán, que pueden ayudar a tomar decisiones terapéuticas individualizadas para los pacientes.
Otras herramientas destacables son, los indicadores de calidad para optimizar la prescripción en mayores de 70 años12 y la relación de medicamentos inapropiados por el riesgo de caídas en la población anciana13.
A nivel nacional, destaca también el listado de indicadores de riesgo de morbilidad prevenible causada por medicamentos14
El presente estudio tiene como objetivo determinar la prevalencia y tipo de medicación potencialmente inapropiada en pacientes ancianos polimedicados al ingreso y alta hospitalaria y los factores asociados a su aparición, con la ayuda de criterios explícitos seleccionados de la bibliografía y adaptados a nuestro ámbito.
MétodoEstudio observacional transversal. Se ha desarrollado durante 12 meses (marzo 2010-febrero 2011), sobre pacientes ancianos polimedicados, ingresados en un servicio de Medicina Interna de un hospital perteneciente a un área de gestión sanitaria.
En este área la población asciende a 110.000 habitantes, de los cuales el 18% son mayores de 65 años y un 15% (n: 2.915) pacientes polimedicados (PP).
Se incluyeron los pacientes que cumplían los siguientes criterios: paciente residente en el Área y que ingresa en el Hospital por el servicio de medicina interna; pacientes de edad igual o superior a 65 años; paciente polimedicado: toma más de 6 medicamentos, de forma continuada, durante un periodo de 6 o más meses.
Quedaron excluidos del estudio pacientes que se hospitalizaron por enfermedad aguda muy grave y que no fue debida a reagudización de su proceso crónico, éxitus o pacientes con criterios de terminalidad, pronóstico infausto a corto plazo o incluidos en programa de cuidados paliativos, pacientes con alta hospitalaria en las primeras 48 horas, pacientes con traslado a otro centro hospitalario.
El tamaño muestral de pacientes ingresados necesario para obtener una significación estadística del 95 % y una precisión del 7% siendo la prevalencia mínima descrita de PIM en otros estudios de un 35%15, es de 179 pacientes.
La variable principal fue la prevalencia global de pacientes en tratamiento con PIM al ingreso y al alta y las variables secundarias (independientes): edad y sexo, n° de medicamentos al ingreso y al alta, presencia de pluripatología (según la definición del proceso asistencial integrado de la Consejería de salud, Junta de Andalucía16, índice de comorbilidad de Charlson (versión abreviada)17 y grado de dependencia (Índice de Barthel)18.
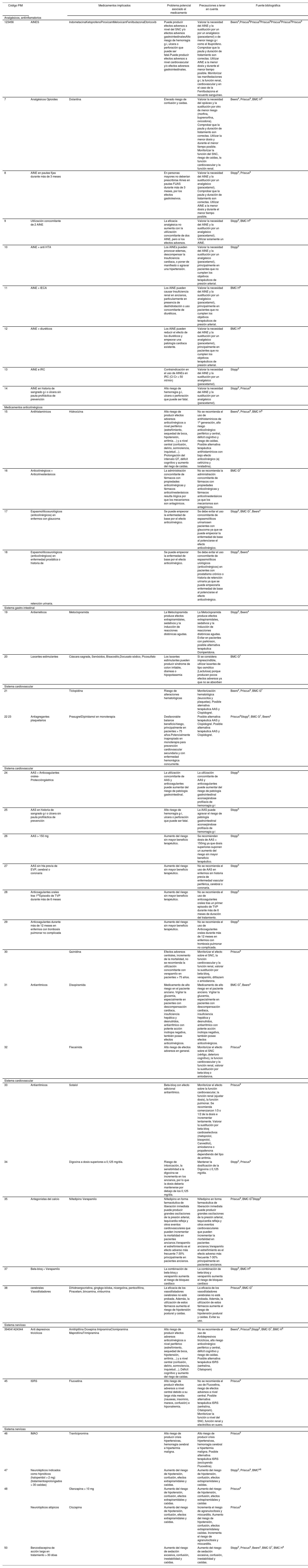
En una primera fase del estudio se definieron los criterios explícitos en nuestro ámbito, mediante técnica Delphi19 y contando con un panel de expertos compuesto por farmacéuticos de hospital y médicos internistas, se elaboró un listado con un total de 84 criterios explícitos, en base a las siguientes directrices: a) los PIM debían estar referenciados en la bibliografía; b) la medicación es de uso común en nuestro entorno y c) potencial iatrogenia descrita en la población de estudio.
Se diseñó una matriz de priorización compuesta por: a) descripción del PIM; b) valoración de la gravedad (de 1 = no supone riesgo a 4 = efectos adversos importantes para el paciente); c) valoración de la frecuencia (de 1 = muy raro a 4 = muy frecuente); d) valoración social (de 1: los profesionales sanitarios no muestran interés a 4 = están muy interesados); e) valoración de la vulnerabilidad del problema (de 0: no tiene solución a 4: tiene solución)20.
Se realizaron dos rondas Delphi, en la primera se envió la plantilla con los 84 PIM iniciales, las instrucciones para la evaluación y las principales referencias bibliográficas de interés. Tras la segunda ronda de votación, se consensuaron 50 criterios (PIM) definitivos del total de 84 iniciales (Anexo 1).
En una segunda fase se detectaron los PIM al ingreso. A través del programa de facturación de recetas de atención primaria, se seleccionaron aquellos pacientes que cumplían los criterios de inclusión y se realizó el cruce entre esta base de datos con el programa de admisión de hospitalización, alertando diariamente de aquellos pacientes que ingresaban en el servicio de Medicina Interna.
Una vez identificados los PP que a diario ingresaban en el servicio de medicina interna, se revisó su historial farmacoterapéutico con el apoyo de la historia de salud digital, en atención primaria y servicio de urgencias hospitalario. Posteriormente y mediante entrevista clínica estructurada, directamente al paciente y/o cuidador se elaboró por parte del servicio de farmacia, un informe de conciliación inicial de la medicación al ingreso que incluyó: alergias conocidas, medicación que tomaba el paciente, discrepancias encontradas con la medicación pautada, medicación potencialmente inadecuada, existencia de cuidador, conocimiento acerca de las indicaciones y forma de administración por parte del cuidador/paciente, adherencia al tratamiento. Este informe queda accesible en la aplicación informática de historias clínicas del hospital, para su revisión por el médico internista responsable del paciente, utilizándolo como herramienta auxiliar para elaborar el plan farmacoterapéutico que el paciente debe seguir al alta hospitalaria.
Por último para detectar los PIM al alta, a diario y de la misma forma, se seleccionaban los PP que habían sido dados de alta por el servicio de medicina interna y se identificaban los PIM recogidos en el informe elaborado por el internista.
Análisis estadísticoSe realizó un análisis descriptivo de la muestra calculando porcentajes y medias con sus intervalos de confianza (IC) del 95%. La relación entre las diferentes variables categóricas se estudió mediante la prueba de Chi cuadrado. Para identificar los factores asociados con la presencia de PIM, se realizó una regresión logística binaria multivariante. El análisis de los datos se efectuó con el programa SPSS 13.0.
ResultadosDescripción de la muestraDe los 247 PP que ingresaron en el servicio de medicina interna durante el período de estudio, se excluyeron 68 porque: tomaban < 6 medicamentos (n = 29), fueron éxitus o con criterios de terminalidad (n = 30), se trasladaron a otro hospital (7) o fueron dados de alta en las primeras 48 h (n = 2).
Las características respecto al sexo fueron: 88 mujeres (49,2%) y 91 varones (50,8%) y la edad media fue de 79,5 años (D.E: 6,61). El 79,9% (143) de los pacientes presentaban pluripatología con una media de índice de Charlson de 2,2 (D.E: 1,15) y con un índice de Barthel de 55,4 (D.E: 31,27). La media de medicamentos al ingreso fue de 11,5 (D.E:2,7), con una media de PIM de 1,6 (D.E:1,60) por paciente, siendo la media de medicamentos al alta 10,4 (D.E:2,80), con una media de PIM de 0,8 (D.E:1,20).
Prevalencia de pacientes en tratamiento con PIMLa prevalencia de pacientes que presentaron PIM al ingreso resultó ser del 71,0% y al alta del 48,0%.
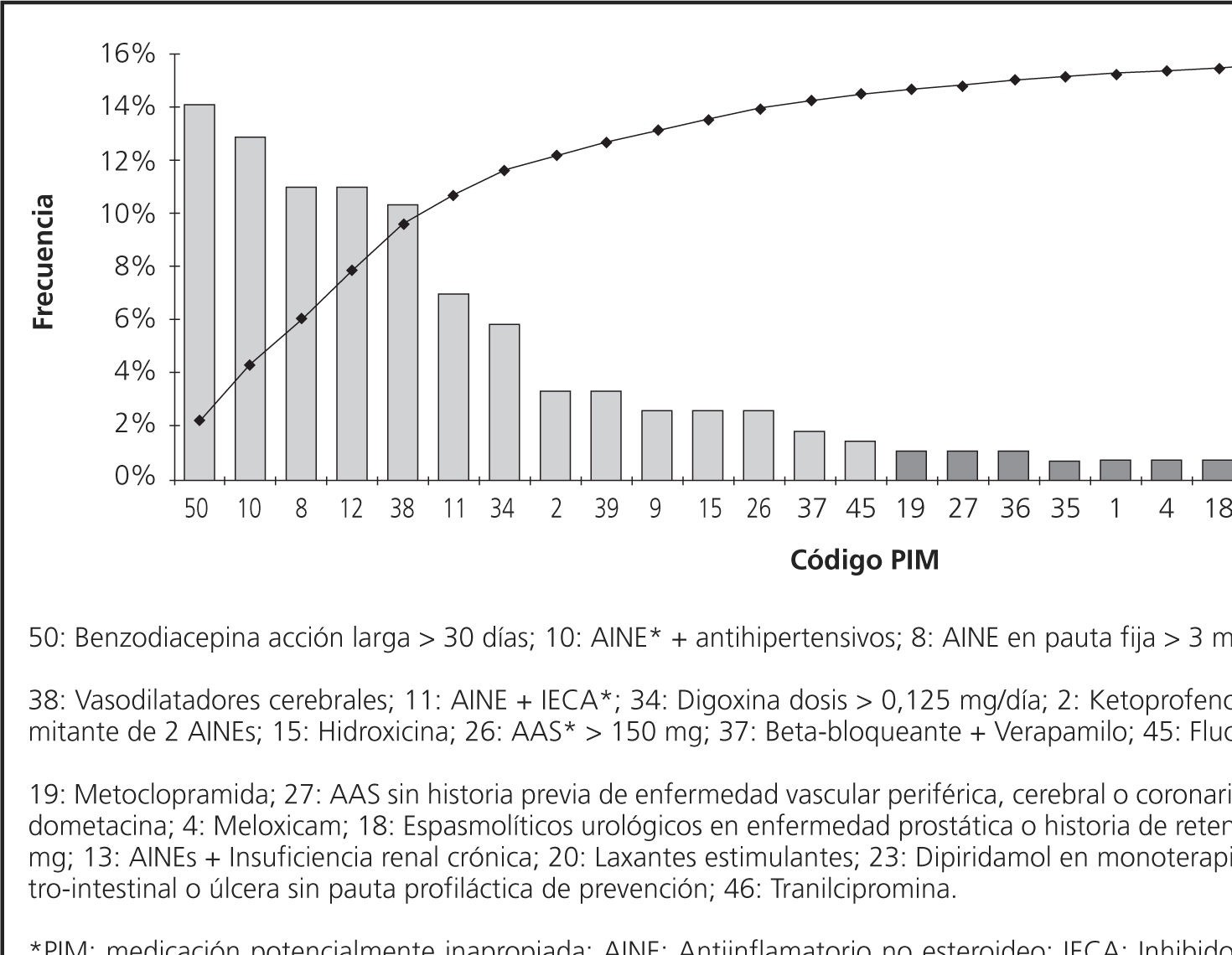
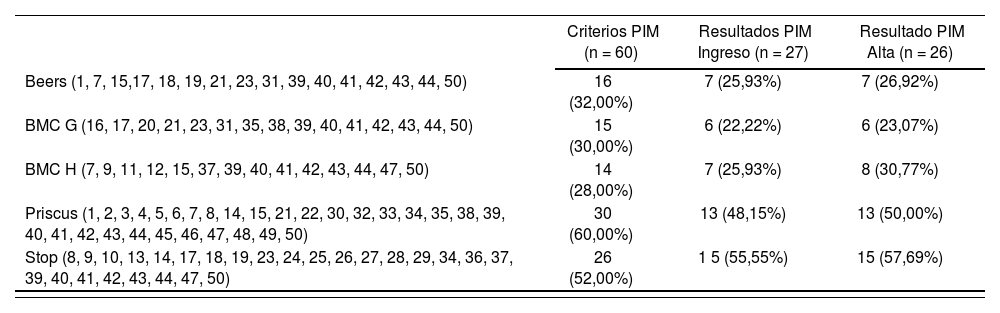
En cuanto a los 50 criterios de referencia evaluados en nuestra población, sólo se han detectado 27 tipos de PIM distintos al ingreso, de los cuales un 55,5% proceden de los listados STOPP y un 25,9% de la lista Beers. Al alta se detectan 26 PIM, 57,7% de los cuales tienen su referencia en la lista STOPP y 26,9% en Beers. En la tabla 1 se describen los porcentajes de PIM que han sido detectados por los distintos criterios explícitos utilizados. Los Figuras 1 y 2 recogen la distribución de frecuencias de los distintos PIM detectados. Al ingreso, 4 criterios distintos explican el 50,0% del total de PIM, siendo estos: Benzodiacepina acción larga > 30 días; AINE + antihipertensivos; AINE en pauta fija durante más de 3 meses; y AINE+diurético (Fig. 1).
PIM* detectados según criterios
| Criterios PIM (n = 60) | Resultados PIM Ingreso (n = 27) | Resultado PIM Alta (n = 26) | |
|---|---|---|---|
| Beers (1, 7, 15,17, 18, 19, 21, 23, 31, 39, 40, 41, 42, 43, 44, 50) | 16 (32,00%) | 7 (25,93%) | 7 (26,92%) |
| BMC G (16, 17, 20, 21, 23, 31, 35, 38, 39, 40, 41, 42, 43, 44, 50) | 15 (30,00%) | 6 (22,22%) | 6 (23,07%) |
| BMC H (7, 9, 11, 12, 15, 37, 39, 40, 41, 42, 43, 44, 47, 50) | 14 (28,00%) | 7 (25,93%) | 8 (30,77%) |
| Priscus (1, 2, 3, 4, 5, 6, 7, 8, 14, 15, 21, 22, 30, 32, 33, 34, 35, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50) | 30 (60,00%) | 13 (48,15%) | 13 (50,00%) |
| Stop (8, 9, 10, 13, 14, 17, 18, 19, 23, 24, 25, 26, 27, 28, 29, 34, 36, 37, 39, 40, 41, 42, 43, 44, 47, 50) | 26 (52,00%) | 1 5 (55,55%) | 15 (57,69%) |
*PIM: Medicación potencialmente inapropiada.
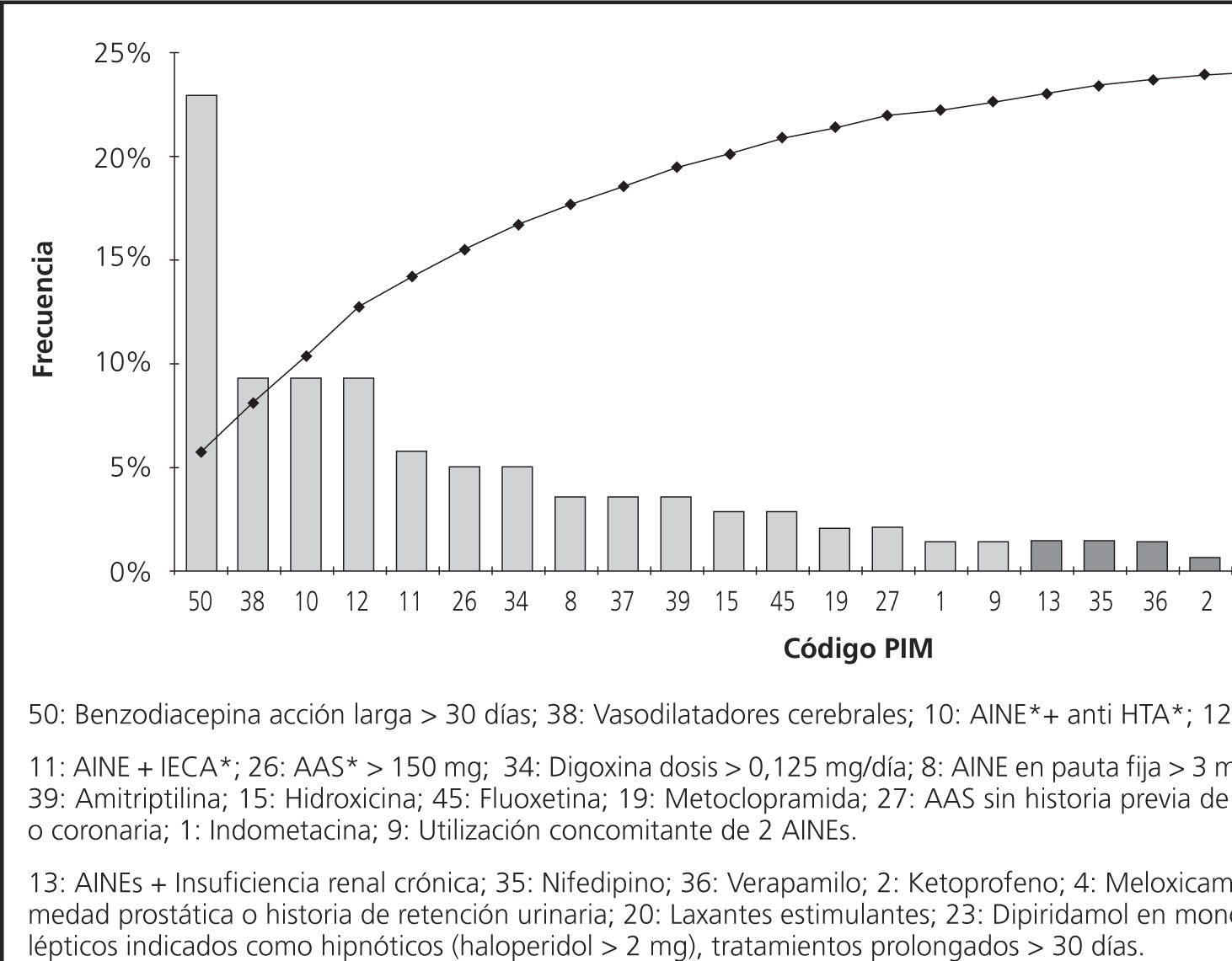
En el caso de los resultados al alta son también 4 los criterios PIM que engloban el 50,0% del total, destacando las benzodiacepinas de acción larga con un 23,0% y la incorporación del grupo de vasodilatadores cerebrales (Fig. 2).
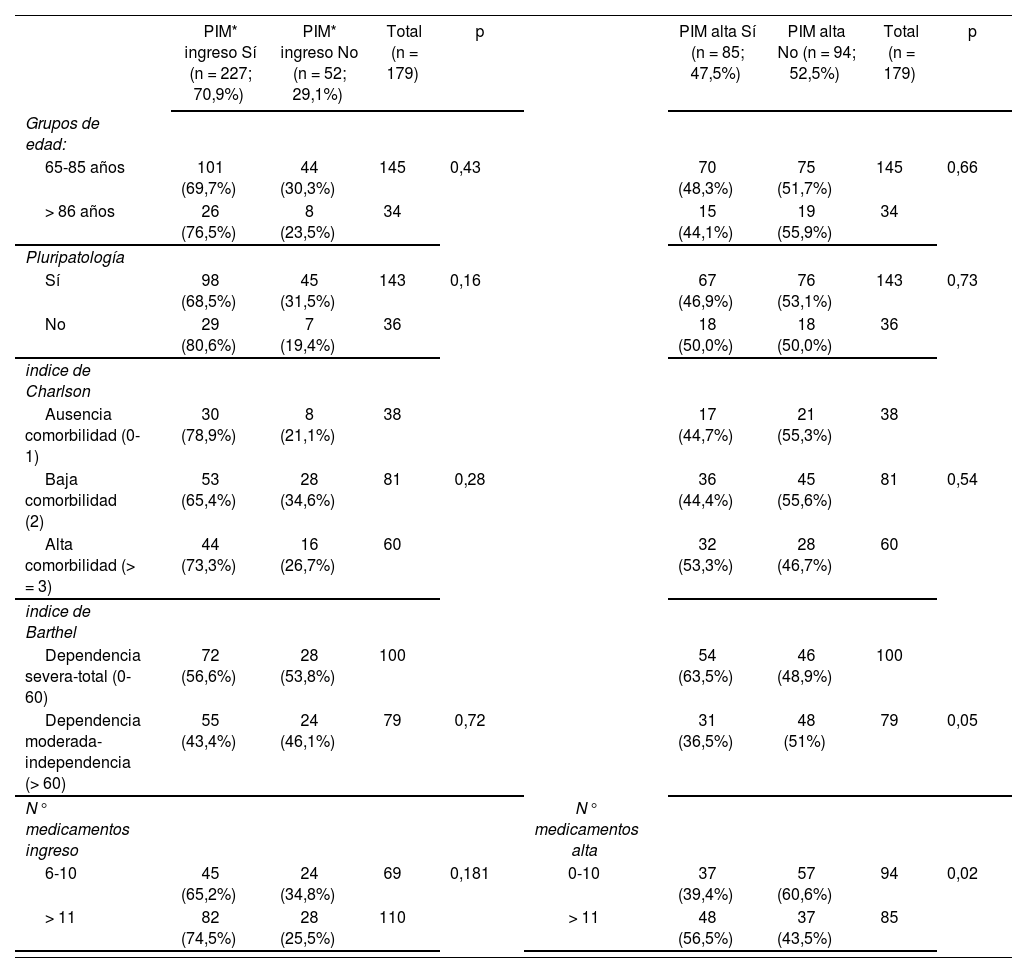
Factores asociadosEn la tabla 2 se muestran los resultados del análisis estadístico de las diferentes variables como posibles factores asociados a la aparición de PIM. Se encontró asociación estadísticamente significativa con la presencia de PIM al alta para la variable número de medicamentos al alta (p = 0,02) y el Índice de Barthel (p = 0,05).
Variables de estudio y asociación con la presencia de PIM
| PIM* ingreso Sí (n = 227; 70,9%) | PIM* ingreso No (n = 52; 29,1%) | Total (n = 179) | p | PIM alta Sí (n = 85; 47,5%) | PIM alta No (n = 94; 52,5%) | Total (n = 179) | p | ||
|---|---|---|---|---|---|---|---|---|---|
| Grupos de edad: | |||||||||
| 65-85 años | 101 (69,7%) | 44 (30,3%) | 145 | 0,43 | 70 (48,3%) | 75 (51,7%) | 145 | 0,66 | |
| > 86 años | 26 (76,5%) | 8 (23,5%) | 34 | 15 (44,1%) | 19 (55,9%) | 34 | |||
| Pluripatología | |||||||||
| Sí | 98 (68,5%) | 45 (31,5%) | 143 | 0,16 | 67 (46,9%) | 76 (53,1%) | 143 | 0,73 | |
| No | 29 (80,6%) | 7 (19,4%) | 36 | 18 (50,0%) | 18 (50,0%) | 36 | |||
| indice de Charlson | |||||||||
| Ausencia comorbilidad (0-1) | 30 (78,9%) | 8 (21,1%) | 38 | 17 (44,7%) | 21 (55,3%) | 38 | |||
| Baja comorbilidad (2) | 53 (65,4%) | 28 (34,6%) | 81 | 0,28 | 36 (44,4%) | 45 (55,6%) | 81 | 0,54 | |
| Alta comorbilidad (> = 3) | 44 (73,3%) | 16 (26,7%) | 60 | 32 (53,3%) | 28 (46,7%) | 60 | |||
| indice de Barthel | |||||||||
| Dependencia severa-total (0-60) | 72 (56,6%) | 28 (53,8%) | 100 | 54 (63,5%) | 46 (48,9%) | 100 | |||
| Dependencia moderada-independencia (> 60) | 55 (43,4%) | 24 (46,1%) | 79 | 0,72 | 31 (36,5%) | 48 (51%) | 79 | 0,05 | |
| N° medicamentos ingreso | N° medicamentos alta | ||||||||
| 6-10 | 45 (65,2%) | 24 (34,8%) | 69 | 0,181 | 0-10 | 37 (39,4%) | 57 (60,6%) | 94 | 0,02 |
| > 11 | 82 (74,5%) | 28 (25,5%) | 110 | > 11 | 48 (56,5%) | 37 (43,5%) | 85 |
*PIM: Medicación potencialmente inapropiada.
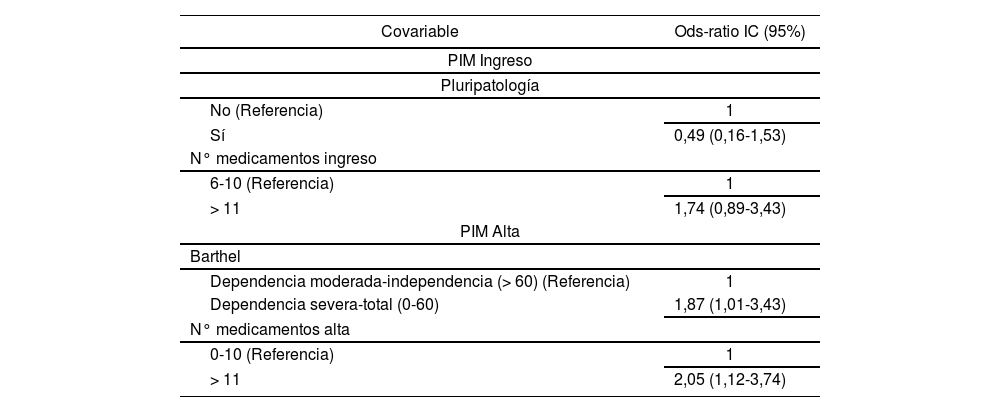
Se realizó un análisis multivariable (Tabla 3), utilizando un modelo de regresión logística, incluyéndose aquellas variables con un grado de significación menor de 0,20 (p < 0,20): para la variable dependiente PIM ingreso se analizó su asociación con la presencia de pluripatología y el n° medicamentos al ingreso, no encontrándose significación estadística en ningún caso. Para la variable PIM alta se analizó el índice de Barthel y el n° de medicamentos al alta mostrando la población con índice de Barthel entre 0 y 60 (dependencia severatotal) un riesgo 1,8 veces superior de presentar PIM al alta respecto a la población con un índice mayor de 60. Así mismo, el riesgo de presentar PIM al alta es 2 veces superior, cuando el paciente toma más de 11 medicamentos.
Resultado del análisis multivariable
| Covariable | Ods-ratio IC (95%) |
|---|---|
| PIM Ingreso | |
| Pluripatología | |
| No (Referencia) | 1 |
| Sí | 0,49 (0,16-1,53) |
| N° medicamentos ingreso | |
| 6-10 (Referencia) | 1 |
| > 11 | 1,74 (0,89-3,43) |
| PIM Alta | |
| Barthel | |
| Dependencia moderada-independencia (> 60) (Referencia) | 1 |
| Dependencia severa-total (0-60) | 1,87 (1,01-3,43) |
| N° medicamentos alta | |
| 0-10 (Referencia) | 1 |
| > 11 | 2,05 (1,12-3,74) |
*PIM: medicación potencialmente inapropiada
Aunque actualmente está en debate la validez de los criterios explícitos como indicadores predictivos positivos de eventos adversos a la medicación prescrita en el paciente anciano21-22, no es menos cierto que son herramientas fiables para su aplicación homogénea en determinadas poblaciones y susceptibles de ser utilizadas en aplicaciones informáticas para la evaluación de la adecuación de la prescripción en grandes muestras de pacientes23. El gran inconveniente, es su falta de validez externa lo que provoca que en cada país se tengan que adaptar dichos criterios para reflejar de la forma más aproximada posible las pautas prescriptoras existentes en un determinado entorno. Como se ha descrito más arriba, distintos países europeos han consensuado la elaboración de listas con PIM, esto no ha sucedido aún en España. Sólo contamos con la versión española de los criterios STOPP/START realizada por Delgado Silveira y cols.9. El listado de criterios seleccionados por nuestro grupo sigue la metodología descrita en la bibliografía19 y consta de 50 items de los cuales han podido ser aplicados en nuestra muestra, 27 al ingreso y 26 al alta hospitalaria. La selección de criterios probablemente esté sesgada por la procedencia o ámbito profesional del panel de expertos.
Aún con las limitaciones expresadas se ha detectado un porcentaje inusualmente alto de PIM en la prescripción de la muestra al ingreso hospitalario. Los valores recogidos en la bibliografía anglosajona revisada en pacientes hospitalarios giran en torno al 44,0%24 utilizando criterios Beers y el 40,0% utilizando una combinación de criterios Beers y McLeod25. En Europa, Gallagher y cols. han utilizado los criterios STOPP y describen una tasa de prevalencia del 51,3% en pacientes ancianos hospitalizados en distintos hospitales, variando entre el 34,7% en Praga, 45.3% en Madrid, hasta un 77,3% en Ginebra15.
En nuestro ámbito Mera y cols describen una prevalencia del 69,2% utilizando una combinación de criterios Beer y STOPP26.
Es cierto que las tasas de detección de PIM están muy influidas por las características de la muestra poblacional y la metodología utilizada y por tanto no son comparables, por lo que sería necesario estandarizar los instrumentos de medida. En nuestro caso la aplicación de criterios STOPP nos permitió detectar aproximadamente un 55,0% de los PIM al ingreso, lo que nos hace coincidir con la tendencia de la bibliografía europea de utilizar estos criterios como referencia para el análisis de la calidad de la prescripción en el paciente anciano27.
La prevalencia de PIM detectada al alta hospitalaria (48,0%) baja a valores más habituales en las publicaciones sobre el tema. Recordemos que en todo el proceso hay una intervención de personal farmacéutico por la cual, se pone a disposición del médico responsable un informe con los PIM detectados en la medicación del paciente al ingreso. El alcance que pueda tener esta intervención sobre la prescripción médica al alta está por evaluar y abre nuevas líneas de actuación e investigación. Como describe García Caballos en su revisión del tema28, las intervenciones al alta sobre el plan farmacoterapéutico del paciente anciano para evitar problemas relacionados con la medicación están aún lejos de ofrecer resultados concluyentes y no son extrapolables a entornos diferentes de los descritos.
Los PIM más frecuentemente detectados tanto al ingreso como al alta hospitalaria fueron benzodiazepinas de acción larga y antiinflamatorios no esteroideos, coincidiendo con otras publicaciones de nuestro entorno29.
Por otro lado, en nuestro estudio, el grado de dependencia severa o total y los esquemas terapéuticos que, al alta, incluyen más de 11 medicamentos, se relacionaron con la presencia de PIM, este hallazgo es novedoso y no se ha encontrado ningún trabajo que haya establecido una posible asociación entre diferentes factores de riesgo y la prescripción de PIM.
Concluimos que en nuestro área la población mayor de 65 años polimedicada presenta una prevalencia elevada de PIM. El listado de criterios explícitos adaptado a nuestro ámbito, nos ha permitido evaluar este tipo de medicación potencialmente inapropiada e identificar aquellos medicamentos de alto riesgo (benzodiacepinas de acción larga, AINEs en pacientes hipertensos, vasodilatadores cerebrales…), con el objeto de implementar líneas estratégicas futuras dirigidas a mejorar la adecuación de los tratamientos principalmente en pacientes grandes polimedicados (más de 11 medicamentos) y con dependencia funcional moderada-severa.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses. No se ha percibido ninguna beca ni ayuda económica para la realización de este trabajo.
| Código PIM | Medicamentos implicados | Problema potencial asociado al medicamento | Precauciones a tener en cuenta | Fuente bibliográfica | |
|---|---|---|---|---|---|
| Analgésicos, antiinflamatorios | |||||
| 123456 | AINES | IndometacinaKetoprofenoPiroxicamMeloxicamFenilbutazonaEtoricoxib | Puede producir efectos adversos a nivel del SNC y/o efectos adversos gastrointestinalesAlto riesgo de hemorragia g-i, ulcera o perforación que puede ser fatal.Puede producir efectos adversos a nivel cardiovascular y/o efectos adversos gastrointestinales. | Valorar la necesidad del AINE y la sustitución por un por un analgésico (paracetamol) o de menor riesgo g-i como el Ibuprofeno. Comprobar que la pauta y duración de tratamiento son correctas. Utilizar AINE a la menor dosis y durante el menor tiempo posible. Monitorizar las manifestaciones g-i, la función renal, cardiovascular y en el caso de la Fenilbutazona el recuento sanguíneo. | Beers4,Priscus9Priscus9Priscus9Priscus9Priscus9Priscus9 |
| 7 | Analgésicos Opioides | Dolantina | Elevado riesgo de confusión y caídas. | Valorar la necesidad del opiáceo y la sustitución por otro de menor riesgo (morfina, buprenorfina, oxicodona). Comprobar que la pauta y duración de tratamiento son correctas. Utilizar la menor dosis y durante el menor tiempo posible. Monltorlzar la función del SNC, riesgo de caídas, la función cardiovascular y la función renal. | Beers4, Priscus9, BMC H8 |
| 8 | AINE en pautas fijas durante más de 3 meses | En personas mayores no deberían prescribirse Aines en pautas FIJAS durante más de 3 meses, por los efectos gastrolesivos. | Valorar la necesidad del AINE y la sustitución por un analgésico (paracetamol). Comprobar que la pauta y duración de tratamiento son correctas. Utilizar AINE a la menor dosis y durante el menor tiempo posible. | Stopp5, Priscus9 | |
| 9 | Utilización concomitante de 2 AINE | La eficacia analgésica no aumenta con la utilización concomitante de dos AINE, pero sí los efectos adversos. | Valorar la necesidad del AINE y la sustitución por un analgésico (paracetamol). Utilizar solamente un AINE. | Stopp5, BMC H8 | |
| 10 | AINE + anti HTA | Los AINEs pueden provocar edemas, descompensar la Insuficiencia cardiaca, o poner de manifiesto o agravar una hipertensión. | Valorar la necesidad del AINE y la sustitución por un analgésico (paracetamol), principalmente en pacientes que no cumplen los objetivos terapéuticos de presión arterial. | Stopp5 | |
| 11 | AINE + IECA | Los AINE pueden causar Insuficiencia renal en ancianos, particularmente en presencia de deshidratación o uso concomitante de diuréticos. | Valorar la necesidad del AINE y la sustitución por un analgésico (paracetamol), principalmente en pacientes que no cumplen los objetivos terapéuticos de presión arterial. | BMC H8 | |
| 12 | AINE + diuréticos | Los AINE pueden reducir el efecto de los diuréticos y empeorar una patología cardiaca existente. | Valorar la necesidad del AINE y la sustitución por un analgésico (paracetamol), principalmente en pacientes que no cumplen los objetivos terapéuticos de presión arterial. | BMC H8 | |
| 13 | AINE e IRC | Contraindicación en el uso de AINEs en IRC (CI Cr < 50 ml/min) | Valorar la necesidad del AINE y la sustitución por un analgésico (paracetamol). | Stopp5 | |
| 14 | AINE en historia de sangrado g-i o úlcera sin pauta profiláctica de prevención | Alto riesgo de hemorragia g-i, ulcera o perforación que puede ser fatal. | Valorar la necesidad del AINE y la sustitución por un analgésico (paracetamol). | Stopp5, Priscus9 | |
| Medicamentos anticolinérgicos | |||||
| 15 | Antihistamínicos | Hidroxizina | Alto riesgo de producir efectos adversos anticolinérgicos a nivel periférico (estreñimiento, sequedad de boca, hipotensión, arritmia…) y a nivel central (confusión, delirio, somnolencia, inquietud…). Prolongación del intervalo QT, déficit cognitivo y aumento del riego de caídas. | No se recomienda el uso de antihistamínicos de 1a generación, alto riesgo anticolinérgico periférico y central, déficit cognitivo y riesgo de caídas. Posible alternativa terapéutica antihistamínicos con bajo efecto anticolinérgico (ej cetirizina y loratadina). | Beers4, Priscus9, BMC H8 |
| 16 | Anticolinérgicos + Anticolinesterásicos | La administración concomitante de fármacos con propiedades anticolinérgicas y fármacos anticolinesterásicos resulta ilógica por que los mecanismos son antagónicos. | No se recomienda la administración concomitante de fármacos con propiedades anticolinérgicas y fármacos anticolinesterásicos ya que los mecanismos son antagónicos. | BMC G7 | |
| 17 | Espasmolíticosurológicos (anticolinérgicos) en enfermos con glaucoma | Se puede empeorar la enfermedad de base por el efecto anticolinérgico. | Se debe evitar el uso concomitante de espasmolíticos urinariosen pacientes con glaucoma ya que se puede empeorar la enfermedad de base al potenciarse el efecto anticolinérgico. | Stopp5, BMC G7, Beers4 | |
| 18 | Espasmolíticosurológicos (anticolinérgicos) en enfermedad prostática o historia de | Se puede empeorar la enfermedad de base por el efecto anticolinérgico. | Se debe evitar el uso concomitante de espasmolíticos urológicos (anticolinérgicos) en pacientes con prostatismo crónico o historia de retención urinaria ya que se puede empeorarla enfermedad de base al potenciarse el efecto anticolinérgico. | Stopp5, Beers4 | |
| retención urinaria. | |||||
| Sistema gastro-intestinal | |||||
| 19 | Antieméticos | Metoclopramida | La Metoclopramida produce efectos extrapiramidales, sedativos y la inducción de reacciones distónicas agudas. | La Metoclopramida produce efectos extrapiramidales, sedativos y la inducción de reacciones distónicas agudas. Evitar en pacientes con parkinson, posible alternativa terapéutica Domperidona. | Stopp5, Beers4 |
| 20 | Laxantes estimulantes | Cáscara sagrada, Senósidos, Bisacodilo,Docusato sódico, Picosulfato | Los laxantes estimulantes pueden producir síndrome de colon irritable, diarreas o hipopotasemia | Si se considera imprescindible, utilizar laxantes de tipo osmótico {Lactulosa) porque producen pocos efectos adversos ya que no se absorben | BMC G7 |
| Sistema cardiovascular | |||||
| 21 | Ticlopidina | Riesgo de alteraciones hematológicas | Monitorización hematológica (leucocitos y plaquetas). Posible aternativa terapéutica AAS y Clopidogrel. | Beers4, Priscus9, BMC G7 | |
| 22 23 | Antiagregantes plaquetarios | PrasugrelDipiridamol en monoterapia | Desfavorable balance beneficio/riesgo, principalmente en pacientes > 75 años.Potencialmente inapropiado en monoterapia para prevención cardiovascular secundaria y con enfermedad hemorrágica concurrente. | Posible alternativa terapéutica AAS y Clopidogrel. Posible alternativa terapéutica AAS y Clopidogrel. | Priscus9Stopp5, BMC G7, Beers4 |
| Sistema cardiovascular | |||||
| 24 | AAS + Anticoagulantes orales-Proteccióngástrica | La utilización concomitante de AAS y anticoagulantes puede aumentar del riesgo de patología gastrointestinal. | La utilización concomitante de AAS y anticoagulantes puede aumentar del riesgo de patología gastrointestinal aconsejándose profilaxis de hemorragia g-i | Stopp5 | |
| 25 | AAS en historia de sangrado g-i o úlcera sin pauta profiláctica de prevención | Alto riesgo de hemorragia g-i, ulcera o perforación que puede ser fatal. | La AAS puede agravar el riesgo de patología gastrointestinal aconsejándose profilaxis de hemorragia g-i | Stopp5 | |
| 26 | AAS > 150 mg | Aumento del riesgo sin mayor beneficio terapéutico. | Se recomiendan dosis de AAS < 150mg ya que dosis superiores suponen un aumento del riesgo sin mayor beneficio terapéutico. | Stopp5 | |
| 27 | AAS sin hta previa de EVP, cerebral o coronaria | Aumento del riesgo sin mayor beneficio terapéutico. | No se recomienda el uso de AAS en enfermos sin historia previa de enfermedad vascular periférica, cerebral o coronaria. | Stopp5 | |
| 28 | Anticoagulantes orales tras 1erEpisodio de TVP durante más de 6 meses | Aumento del riesgo sin mayor beneficio terapéutico. | No se recomienda el uso de anticoagulantes orales tras un primer episodio de TVP durante más de 6 meses de duración del tratamiento. | Stopp5 | |
| 29 | Anticoagulantes durante más de 12 meses en enfermos con trombosis pulmonar no complicada | Aumento del riesgo sin mayor beneficio terapéutico. | No se recomienda el uso de Anticoagulantes orales durante más de 12 meses en enfermos con trombosis pulmonar no complicada. | Stopp5 | |
| 30 | Quinidina | Efectos adversos centrales, incremento de la mortalidad, no se recomienda la utilización concomitante con verapamilo en pacientes > 75 años. | Monitorizar el efecto sobre el SNC, la función cardiovascular y la función renal, valorar la sustitución por beta-bloq, verapamilo, diltiazem o amiodarona. | Priscus9 | |
| 31 | Antiarritmicos | Disopiramida | Medicamento de alto riesgo en el paciente anciano. Vigilar la glucemia, especialmente en pacientes con descompensación cardiaca, insuficiencia hepática y desnutridos, antiarrítmico con potente acción inotropa negativa, también posee efectos anticolinérgicos. | Medicamento de alto riesgo en el paciente anciano. Vigilar la glucemia, especialmente en pacientes con descompensación cardiaca, insuficiencia hepática y desnutridos, antiarritmíco con potente acción inotropa negativa, también posee efectos anticolinérgicos. | BMC G7, Beers4 |
| 32 | Flecainida | Alto riesgo de efectos adversos en general. | Monitorizar el efecto sobre el SNC (vértigo, deterioro cognitivo), la funcion cardiovascular y la función renal, valorar la sustitución por beta-bloq o amiodarona. | Priscus9 | |
| Sistema cardiovascular | |||||
| 33 | Antiarritmicos | Sotalol | Beta-bloq con efecto adicional antiarritmico. | Monitorizar el efecto sobre la función cardiovascular, la función renal (ajustar dosis), la función pulmonar. Se recomienda comenzarcon 1/3 o 1/2 de la dosis e incrementar lentamente. Valorar la sustitución por beta-bloq cardioselectivos (metoprolol, bisoprolol, Carvedilol), amiodarona o propafenona dependiendo del tipo de arritmia. | Priscus9 |
| 34 | Digoxina a dosis superiores a 0,125 mg/día. | Riesgo de intoxicación, la sensibilidad a la digoxina se incrementa en los ancianos, por lo que la dosis debería mantenerse por debajo de los 0,125 mg/día. | Mantener la dosificación de la Digoxina ≤ 0,125 mg/día. | Stopp5, Priscus9 | |
| 35 | Antagonistas del calcio | Nifedipino Verapamilo | Nifedipino en forma farmacéutica de liberación inmediata puede producir grandes oscilaciones de la presión arterial, taquicardia refleja y otros eventos cardiovasculares que pueden incrementar la mortalidad en pacientes ancianos.Verapamilo el estreñimiento es el efecto adverso más frecuente 7-30% principalmente en pacientes ancianos. | Nifedipino en forma farmacéutica de liberación inmediata puede producir grandes oscilaciones de la presión arterial, taquicardia refleja y otros eventos cardiovasculares que pueden incrementar la mortalidad en pacientes ancianos.Verapamilo el estreñimiento es el efecto adverso más frecuente 7-30% principalmente en pacientes ancianos. | Priscus9, BMC G7Stopp5 |
| 37 | Beta-bloq + Verapamilo | La combinación de beta-bloq y verapamilo aumenta el riesgo de bloqueo cardíaco | La combinación de beta-bloq y verapamilo aumenta el riesgo de bloqueo cardíaco | Stopp5, BMC H8 | |
| 38 | cerebrales Vasodilatadores | Dihidroergocristina, gingkgo-biloba, nicergolina, pentoxifilina, Piracetam, bincamina, vinburnina | La eficacia de los vasodilatadores cerebrales no está probada. Además, la utilización de estos fármacos aumenta el riesgo de hipotensión postural y caídas. | La eficacia de los vasodilatadores cerebrales no está probada. Además, la utilización de estos fármacos aumenta el riesgo de hipotensión postural y caídas. Evitar su uso. | Priscus9, BMC G7 |
| Sistema nervioso | |||||
| 394041424344 | Anti depresivos tricíclicos | Amitriptilina Doxepina ImipraminaClomipramina MaprotilinaTrimipramina | Alto riesgo de producir efectos adversos anticolinérgicos a nivel periférico (estreñimiento, sequedad de boca, hipotensión, arritmia…) y a nivel central (confusión, delirio, somnolencia, inquietud…). Déficit cognitivo y aumento del riego de caídas. | No se recomienda el uso de Antidepresivos tricíclicos, alto riesgo anticolinérgico periférico y central, déficit cognitivo y riesgo de caídas. Posible alternativa terapéutica ISRS (sertralina, Citalopram) | Beers4, Priscus9,Stopp5, BMC G7, BMC H8 |
| 45 | ISRS | Fluoxetina | Alto riesgo de producir efectos adversos a nivel central debido a su larga vida media (nauseas, insomnio, mareos, confusión) e hiponatremia. | No se recomienda el uso de Fluoxetina, riesgo de efectos adversos a nivel central. Posible alternativa terapéutica ISRS (sertralina, Citalopram). Monitorizar la función a nivel del SNC, función renal y electrolitos en suero. | Priscus9 |
| Sistema nervioso | |||||
| 46 | IMAO | Tranilcipromina | Alto riesgo de producir crisis hipertensivas, hemorragia cerebral e hipertermia maligna. | Alto riesgo de producir crisis hipertensivas, hemorragia cerebral e hipertermia maligna. Posible alternativa terapéutica ISRS (excluyendo Fluoxetina). | Priscus9 |
| 47 | Neurolépticos indicados como hipnóticos (haloperidol > 2 mg) (tratamientosprolongados > 30 caódas) | Aumento del riesgo de hipotensión, confusión, efectos extrapiramidales y caódas. | Aumento del riesgo de hipotensión, confusión, efectos extrapiramidales y caódas. | Stopp5, Priscus9, BMCH8 | |
| 48 | Olanzapina > 10 mg | Aumento del riesgo de hipotensión, confusión, efectos extrapiramidales y caódas. | Aumento del riesgo de hipotensión, confusión, efectos extrapiramidales y caódas | Priscus9 | |
| Neurolópticos atópicos | Clozapina | Aumento del riesgo de hipotensión, confusión, efectos extrapiramidales y caódas. | Incrementa el riesgo de agranulocitosis y miocarditis. Aumento del riesgo de hipotensión, confusión, efectos extrapiramidalesy caódas. Incrementa el riesgo de agranulocitosis y miocarditis. | Priscus9 | |
| 50 | Benzodiacepina de acción larga en tratamiento > 30 dóas | Aumento del riesgo de sedación excesiva, confusión, inestabilidad y caódas. | Aumento del riesgo de sedación excesiva, confusión, inestabilidad y caódas. | Stopp5, Priscus9, Beers4, BMC G7, BMC H8 | |
Prevalence of potentially inappropriate medication in hospitalized elderly patients by using explicit criteria