Señordirector:
Laconcentración de las formas farmacéuticaslíquidas es un dato indispensable en la información yetiquetado de una especialidad farmacéutica para conseguirsu correcta dosificación y administración. Estainformación es aún más importante en el casode que se trate de un inyectable intravenoso puesto que la dosisadministrada llega íntegra y directamente al torrentesanguíneo sin sufrir efectos de distribución ymetabolización que disminuyan la dosis. Y aúnmás, si el fármaco en cuestión es uncitotóxico, donde en algunos casos pequeñasdiferencias de volumen podría conducir a unavariación de dosis que a su vez diera lugar amanifestaciones con repercusión clínica.
En lapráctica diaria hemos observado que en el prospecto dealgunas especialidades farmacéuticas de medicamentoscitotóxicos no se indica cual es su concentración.Cuando el medicamento se presenta como un liofilizado que precisaser reconstituido previamente a su administración, estehecho representa una dificultad, ya que en algunos casos el volumenque se obtiene al reconstruir el vial, siguiendo lasrecomendaciones del fabricante para su reconstitución, es enalgunos casos superior al añadido y en otros casos esigual.
El objetivo delpresente trabajo fue comprobar si la información que aportanlos prospectos de los medicamentos citotóxicos utilizados ennuestro hospital indica la concentración del medicamento yestudiar la variación de volúmenes que experimentanalgunos de estos medicamentos al ser reconstituidos. Paraello:
1. Sellevó a cabo la revisión de la información de41 prospectos de medicamentos citotóxicos con el fin decomprobar si en ellos se indicaba la concentración delmedicamento.
2. Serealizó un estudio sobre la variación devolúmenes que experimentan algunos medicamentoscitotóxicos al ser reconstituidos en la unidad decitotóxicos del hospital. Se estudiaron 14 medicamentoscitotóxicos liofilizados incluidos en la guíafarmacoterapéutica, realizándose un control sobre lamedida del volumen obtenido postreconstitución. Cuatroenfermeras diferentes realizaron 238 medidas sobre los medicamentosliofilizados solicitados a la unidad durante dos meses alreconstituir estos citostáticos en su trabajohabitual.
En larevisión de la información de los prospectos seobservó que:
-- En el 24% delos casos (10 medicamentos) el dato de concentración esconocido puesto que se trata de viales reconstituidos.
-- El 37% de loscasos (15 medicamentos) son viales liofilizados en cuyos prospectosse indica la concentración en mg/ml del producto una vezreconstituido siguiendo las indicaciones del fabricante.
-- El 39%restante (16 medicamentos) son viales liofilizados en los que laconcentración del producto reconstituido no estáreflejada en el prospecto, indicándose únicamente elnúmero de miligramos que contiene el vial.
En el caso delos medicamentos extranjeros se observa la presencia del valor deconcentración en todos los prospectos revisados.
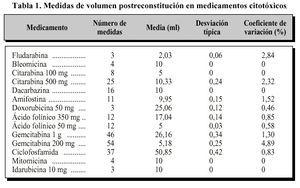
Los resultadosobtenidos en el estudio sobre la variación devolúmenes que experimentan algunos medicamentoscitotóxicos al ser reconstiuidos se detallan en la tabla 1 y fueron los siguientes:
-- En el 21% delos casos (tres medicamentos) al reconstituir los viales el volumenobtenido es superior al de los mililitros de disolventeintroducidos debido al volumen que ocupa el liofilizado. Este hechose advierte en el prospecto del medicamento.
-- En el 14% delas especialidades (dos medicamentos) también se produceeste aumento de volumen, aunque el fabricante no lo advierte en elprospecto, lo que puede dar lugar a la administración dedosis erróneas.
-- En el 35%restante (nueve medicamentos) el volumen introducido parareconstituir los viales fue exactamente el mismo que el que seextrajo, por lo que aunque en la mayoría de los casos en elprospecto de estos medicamentos no se indica suconcentración en mg/ml este dato puede ser fácilmentecalculado.
Los dosmedicamentos que aumentan el volumen sin advertencia en elprospecto son ciclofosfamida y citarabina. En el caso deciclofosfamida 1 g (1) se observó al reconstituirlo con sudisolvente que se recuperaba un volumen medio de 50,85 ml trasrealizar 37 medidas, con un coeficiente de variación de0,83, por lo que se deduce que el polvo liofilizado produce undesplazamiento de 0,85 ml. Esta desviación da lugar a que ladosis administrada pueda ser el 98,3% de la dosis prescrita. Esteerror no se produce si se utiliza el vial entero, pero lo habitual,puesto que los citostáticos se dosifican en funciónde la superficie corporal del paciente, es utilizar los vialesfraccionados. En el caso de citarabina 500 mg (2) el volumen mediomedido al reconstituirlo con su disolvente fue de 10,30 mldespués de realizar 25 medidas con un coeficiente devariación de 2,32, por lo que el polvo liofilizado originaun desplazamiento de 0,30 ml y se produce un error dedosificación al fraccionar el vial administrándoseúnicamente el 97,08% de la dosis.
Si bien en elcaso de estos dos medicamentos la diferencia entre la dosisadministrada y la que se debería de administrar no supera el5% y, por tanto, no tiene trascendecia clínica, ladosificación no es correcta.
De formaanáloga a los casos descritos para ciclofosfamida 1 g ycitarabina 500 mg, aparece en la literatura un problema similar conviales de gemcitabina de 1 g y 200 mg (3). En este caso lareconstitución del medicamento producía undesplazamiento de volumen, de forma que la concentraciónreal era de 38 mg/ml; sin embargo, la indicada en el prospecto porel laboratorio fabricante era de 40 mg/ml. Esta discrepancia seencuentra actualmente corregida en el material de acondicionamientodel producto.
El valor de laconcentración en mg/ml es un dato que debe ser incluido enel prospecto del medicamento. Este hecho aparece recogido en laOrden de 15 de julio de 1982, BOE de 5 de agosto, por la quese regula el material de acondicionamiento de las especialidadesfarmacéuticas de uso humano no publicitarias. En dicha Ordense especifica que en la fórmula cuantitativa del medicamentola cantidad con que cada componente interviene en laformulación vendrá expresada en gramos, miligramos ounidades de actividad por cada unidad de dosis para inyectablesmonodosis o por mililitro para inyectables multidosis.
Nos pareceimportante notificar este hecho para evitar la dosificacióninexacta de estos medicamentos, así como llamar laatención de los laboratorios fabricantes para que elmaterial de acondicionamiento de estas especialidades seamodificado de acuerdo a la legislación vigente.
M. L.Suárez Gea,
R. Luque Infantes,
T. Requena Caturla
Servicio deFarmacia.
Hospital Universitario Príncipe de Asturias. Alcaláde Henares (Madrid).